广西水牛奶与荷斯坦牛奶工艺学特性比较
2011-10-19姚春杰李全阳黄忠闯
姚春杰,李全阳,黄忠闯
(广西大学轻工与食品工程学院,广西南宁530004)
广西水牛奶与荷斯坦牛奶工艺学特性比较
姚春杰,李全阳,黄忠闯
(广西大学轻工与食品工程学院,广西南宁530004)
为了探索、比较广西水牛奶与荷斯坦牛奶的工艺学特性,对二者的缓冲容量、表面张力、粒度分布、稳定系数进行了比较分析。结果表明,广西水牛奶的缓冲容量和粒径分别是荷斯坦牛奶的1.1倍和2倍。在研究范围内,广西水牛奶在pH值为6.8时缓冲容量最大,温度50℃时表面张力最小,pH值为4.7时稳定系数最小;而荷斯坦牛奶在pH值为6.6时缓冲容量最大,温度为50℃时表面张力最小,pH值为4.6时稳定系数最小。广西水牛奶的粒径分布在91.28~458.7 nm之间,荷斯坦牛奶的粒径主要分布为91.28~190.1 nm之间,因此,认为两种牛奶的工艺学参数存在多方面的差异。
水牛奶;荷斯坦牛奶;缓冲容量;粒度分布;表面张力
0 引言
水牛奶营养价值明显高于荷斯坦牛奶,根据广西水牛研究所的检测资料显示,1 kg水牛奶相当于荷斯坦牛奶1.5~2.0 kg[1,2]。蛋白质、氨基酸等分别是荷斯坦奶牛1~2倍,铁、锌和维生素则高于荷斯坦奶牛几十倍[3]。因此,近年来多国学者对水牛奶的重视程度显著提高[4-6]。Sarfraz Ahmad等对摩拉水牛奶和荷斯坦牛奶的理化特性进行了对比研究[7]。Cinzia Benincasa等人对两种牛奶的元素组成进行了探讨[8]。国内许小刚等人利用粒径分析法对水牛奶的稳定性进行了研究[9]。郭本恒等人指出初乳的粘度与乳的总干物质含量和温度有关[10]。而对水牛奶和荷斯坦牛奶的缓冲容量、表面张力、粒度分布等特性的对比研究还鲜有报道。因此,本实验开展此方面的研究,探索水牛奶与荷斯坦牛奶的工艺学特性。
1 实验
1.1 材料与设备
荷斯坦牛奶;广西水牛奶(为广西本地水牛与巴基斯坦摩拉水牛杂交后代所产牛奶,文中简称为水牛奶)。磷酸二氢钠;磷酸氢二钠。
Zetasizer NanoS纳米粒度分析仪,JYW-200A自动界面张力仪,721型分光光度计,BME100S高剪切混合乳化机,TDZ4-WS低速自动平衡离心机,阿贝折光仪。
1.2 方法
1.2.1 缓冲容量的测定
使1 L或1 mL牛乳的pH值改变一个单位(ΔpH=±1)所需加入的强酸或强碱的物质的量[11]。
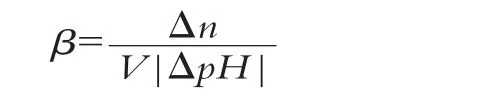
(β:缓冲容量;Δn:强酸或强碱的物质的量;ΔpH:pH值改变量;V:牛乳的体积)。
1.2.2 表面张力的测定
将样品倒入玻璃杯中,液面高度20~25 mm,将玻璃杯放入托盘中间位置,调零后,按上升键,使铂金环深入到液体中5~7 mm处,按停止键。再按下降键,托盘和被测液体开始下降,显示值逐渐增大,最终保持在最大值,该最大值就是表面张力值P,然后按停止键,测量3次取平均值[12,13](精度±0.01)。
(1)牛奶表面张力与温度的关系:分别在30,40,50,60,70,80,90℃测量牛乳的表面张力。
(2)牛奶表面张力与浓度的关系:将牛奶分别稀释0,2,4,6,8倍,然后测量牛乳的表面张力(20℃±1℃)。
(3)牛奶表面张力与pH值的关系:用磷酸缓冲溶液将样品的pH值分别调节为5.4,5.8,6.2,6.6,7.0,然后测量牛奶的表面张力(20℃±1℃)。
1.2.3 粒度分布的测定
Zetasizer NanoS纳米激光粒度分析仪的相关参数:水牛奶的折射率为1.354,荷斯坦牛奶的折射率为1.347,颗粒吸收率为0.01,分散剂为水,分散剂折射率为1.330,进样时温度25℃,样品稀释50倍[9]。
1.2.4 稳定系数的测定
取适量样品置于10 mL离心管中,以3 600 r/min离心5 min后,用721分光光度计于780 nm波长下测定样品离心前后的吸光度A,以稳定系数R值(经验公式R=A后/A前)大小评价样品稳定性高低。R值越接近1,表示其稳定性越高[14,15]。
(1)牛奶稳定系数与浓度的关系:用纯净水将牛奶分别稀释0,2,4,6,8倍,然后测量牛奶样品的稳定系数(20℃±1℃)。
(2)牛奶稳定系数与pH的关系:用磷酸缓冲溶液将样品的pH值调节在4.2~7.0范围内,间隔0.4,然后测量牛奶样品的稳定系数(20℃±1℃)。
2 结果与分析
2.1 缓冲容量的测定结果
不同pH值牛奶样品缓冲容量的测定结果如图1所示。

图1 样品缓冲容量与pH值的关系
由图1可以看出,荷斯坦牛奶缓冲容量在pH值为6.6时出现最大值,而水牛奶的则是6.8,说明两种牛奶的pKa(酸度系数)是不同的,两种牛奶体系中带电颗粒的电荷数是有差异的。从缓冲容量的绝对值看,水牛奶明显高于荷斯坦牛奶,在本研究的酸度范围内,荷斯坦牛奶的最大缓冲浓度为0.0387 mol/L(pH值为6.6),与水牛奶的最小值0.0367 mol/L(pH值为5.4)相差不大,说明水牛奶对酸碱度变化的缓冲能力明显要强,因此可以推断,在利用水牛奶生产酸乳制品时,与采用荷斯坦牛奶相比,乳酸菌发酵的时间要长一些。由于水牛奶出现最大缓冲容量的pH值在6.8,因此新鲜水牛奶的pH值要比相应新鲜的荷斯坦牛奶的pH值要高。
2.2 表面张力的测定结果
(1)不同温度下,牛奶样品表面张力的测定结果如图2所示。
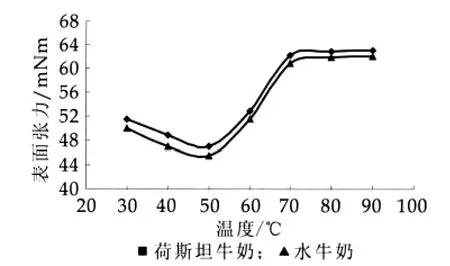
图2 样品表面张力与温度的关系
由图2可以看出,在30~90℃温度范围内,荷斯坦牛奶和水牛奶表面张力出现最小值的温度都是50℃,分别为46.99 mN/m和45.54 mN/m,此温度下体系的稳定性最好,因此,从理论上讲该温度下对样品进行均质处理设备负载最小,效果最好。温度从50℃继续升高到90℃时,表面张力又升高。由图2还可以看出,二者表面张力随温度的变化规律相似,在同一温度下荷斯坦牛奶的表面张力要大于水牛奶的表面张力。
(2)不同稀释倍数下牛奶样品表面张力的测定结果如图3所示。
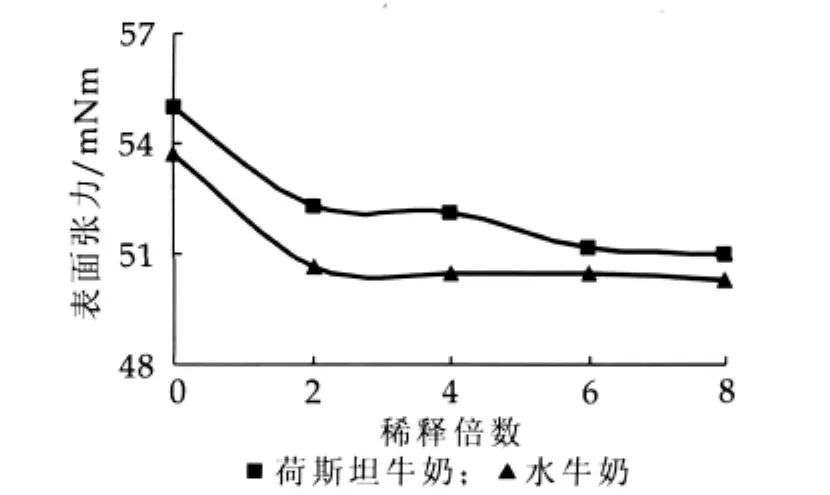
图3 样品表面张力与稀释倍数的关系
由图3可以看出,样品的表面张力随浓度的降低而减小,在稀释2倍时,水牛奶的表面张力从53.69 mN/m降低到50.88 mN/m,荷斯坦牛奶的表面张力从54.98 mN/m降低到52.32 mN/m。由此可以看出,当牛奶受到水的稀释时,开始时水牛奶样品的表面张力值下降较快。随着稀释程度的增加,二者的表面张力值降低速度变慢。在2~8倍的稀释范围内,水牛奶表面张力值在50 mN/m左右,荷斯坦牛奶表面张力值在51 mN/m左右。
(3)不同pH值下牛奶样品表面张力的测定结果如图4所示。
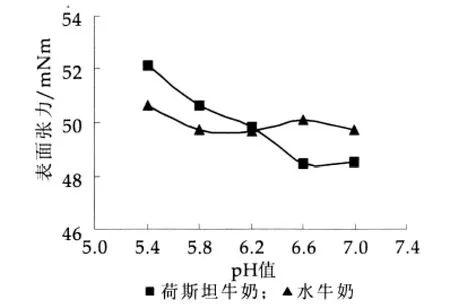
图4 样品表面张力与pH值关系
由图4可以看出,牛奶样品的表面张力随pH值的变化而变化,水牛奶和荷斯坦牛奶的变化趋势有明显差别。在本研究的检测范围内,水牛奶的表面张力随着pH值的升高,先减小再缓慢增大而后又减小,在pH值为6.2时表面张力最小(49.66 mN/m),荷斯坦牛奶的表面张力随着pH值的升高有一个较大范围的下降过程,直到pH值6.6时有一个最小值(48.47 mN/m),而后又缓慢上升。两条曲线在pH值约为6.25时出现交叉,这时二者的表面张力约为49.74 mN/m。由表面张力的概念可以知道,其数值越小体系的稳定性越好,因此可以看出水牛奶和荷斯坦牛奶分别在pH值为6.2和pH值为6.6时稳定性最好。在pH值约为6.25时,二者的表面张力相同,因此判断在此条件下,二者的稳定性是相同的。
2.3 粒度分布的测定结果
水牛奶和荷斯坦牛奶样品经纯净水稀释50倍后,采用纳米粒度分析仪对其粒度分布进行分析,实验结果如图5和图6所示。
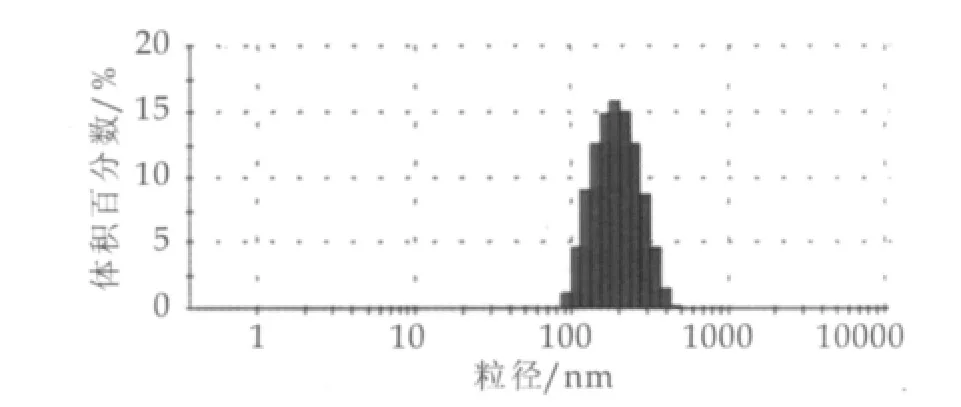
图5 水牛奶粒度分布

图6 荷斯坦牛奶粒度分布
由图5和图6可以看出,样品稀释同样倍数后,荷斯坦牛奶的粒径分布在91.28~190.10 nm之间,而水牛奶的粒径分布91.28~458.70 nm之间,有88.41%的水牛奶粒径分布在122.40~295.30 nm之间。二者的最小粒径相同,但水牛奶的最大粒径是458.70 nm,荷斯坦牛奶的最大粒径为190.10 nm,因此可以看出,水牛奶的粒径显著高于荷斯坦牛奶的粒径。由此可知,水牛奶高质量分数的脂肪不是通过增加脂肪球数量,而是通过增加脂肪球大小来达到脂肪质量分数增加的。
2.4 稳定系数的测定结果
在乳制品中稳定性是一个重要的指标,探讨原料的稳定性条件对保持乳制品稳定性具有重要的意义。为了研究样品的稳定特性,对不同pH值下水牛奶和荷斯坦牛奶样品的稳定性进行了测定,结果如图7所示。
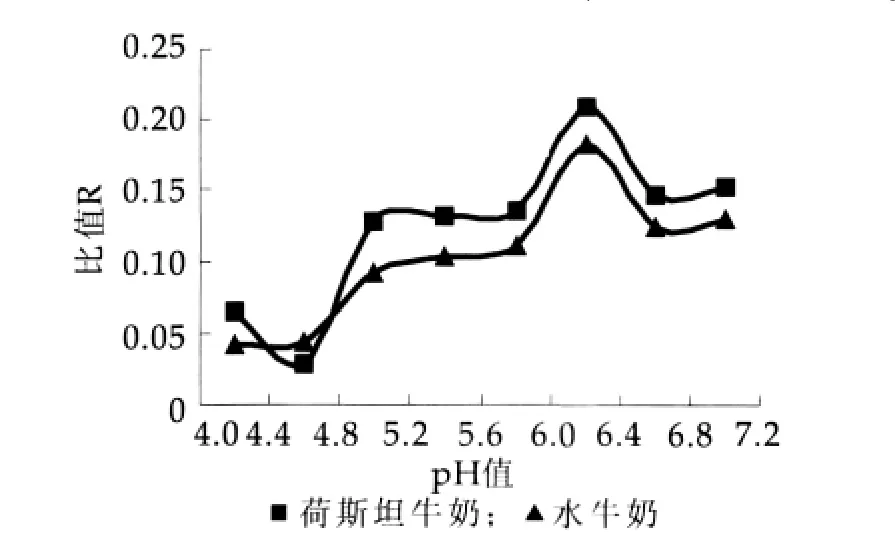
图7 样品稳定性与pH值的关系
图7结果显示,牛奶样品的稳定性随pH值的变化会发生显著的变化,水牛奶和荷斯坦牛奶的变化趋势大致一样。在pH值为4.2~7.0变化范围内,水牛奶的稳定性随着pH值的升高先缓慢减小后增大,一直到pH值为4.7左右时比值R最小(0.0153),pH值为6.2左右时比值R最大(0.209)。荷斯坦牛奶的稳定性随pH值的升高先减小后增大,在pH值为4.6时比值R最小(0.0292),pH值为6.2左右时比值R最大(0.184)。两条曲线在pH值大约为4.55和4.62时相交,比值R分别为0.0440和0.0300。由稳定性的定义可知,比值R越大说明体系的稳定性越好,因此可以看出水牛奶和荷斯坦牛奶在pH值为6.2左右时沉淀量最小,稳定性最好。
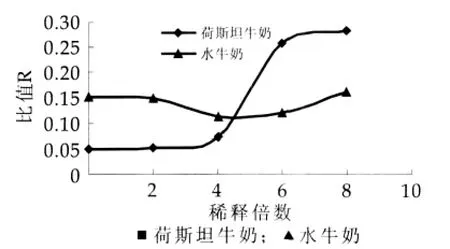
图8 样品稳定性与稀释倍数的关系
稳定系数R是样品离心后和离心前吸光度的比值,大小评价样品稳定性高低。R值越接近1,表示其稳定性越高。图8结果显示,牛奶样品的R值随着稀释倍数的不同而变化,水牛奶和荷斯坦牛奶的R值变化趋势有明显的不同。在实验稀释的范围内,水牛奶的R值随稀释倍数的增加,先略有降低然后又逐渐增大。荷斯坦牛奶稀释倍数从0倍到2倍数,R值变化很小,这与水牛奶的变化趋势基本相同,当稀释倍数从2倍到4倍时,二者变化趋势相反,荷斯坦牛奶的R值逐渐增加,而水牛奶的逐渐下降,当稀释倍数从4倍到6倍时,荷斯坦牛奶的R值急剧增加,从0.072变为0.257,而水牛奶的R值则变化很小,从0.113到0.121,因此两条曲线出现了交叉。两条曲线在稀释大约4.3倍时出现交叉,R值越大,样品的稳定性越好,因此可以看出荷斯坦牛奶的稳定性在稀释后变化显著,而水牛奶变化不显著。
3 讨论
实验结果显示:广西水牛奶和荷斯坦牛奶相比,二者在缓冲容量、表面张力、粒度分布和稳定系数方面都存在差别。在pH值为5.0~7.0的范围内,广西水牛奶的缓冲容量比荷斯坦牛奶的缓冲容量明显要大,在相同pH值下广西水牛奶缓冲容量一般是荷斯坦牛奶的1.2~1.3倍。Sarfraz Ahmad和Salaun等人对摩拉水牛奶进行了研究,在pH值为3.5~6.5的范围内,摩拉水牛奶的缓冲容量约是黑白花牛奶缓冲容量的1.3倍[16]。说明中国水牛杂种后代所产牛奶与摩拉水牛的特性是有差异的。
实验对广西水牛奶和和斯坦牛奶的表面张力与温度、浓度和pH值的关系进行了研究,指出在相同浓度下,广西水牛奶的表面张力小于荷斯坦牛奶的表面张力。在pH值为5.4~7.0研究范围内,广西水牛奶在pH值为6.2时表面张力最小,荷斯坦牛奶在pH值为6.6时表面张力最小。
陆则坚对中、澳两国两种牛奶的流变学特性进行了研究,指出牛奶的流变学特性受浓度、温度和牛奶品种的影响[17]。Lina Chianese等人对地中海牛奶中的酪蛋白进行了报道[18],M.A.Brescia等人对印度水牛奶原料及其成品奶酪的指纹图谱进行了探索[19]。陈瑞芳等人对水牛初乳中免疫因子和生长因子质量浓度进行了研究,结果表明水牛泌乳最初的1~2 d内初乳含有丰富的IgG,IgA和IGF-I[20]。徐丽等人对和斯坦牛奶的牛初乳和常乳中可的松和氢化可的松进行了研究[21]。而本研究首次对两种牛奶的稳定性进行了研究,发现在相同pH值下,广西水牛奶的稳定系数要小于荷斯坦牛奶的稳定系数。这提示我们水牛奶和荷斯坦牛奶的加工艺是不能采用相同的技术参数的,水牛乳制品的加工设备和工艺参数需要结合其自身特点进行研发,而不是照搬。
4 结论
(1)水牛奶的缓冲容量比荷斯坦牛奶的缓冲容量大。在pH值为5.0~7.0范围内,二者随pH值的增加而增大。水牛奶在pH值为6.8时缓冲浓度最大(0.0445 mol/L),荷斯坦牛奶在pH值为6.6时缓冲浓度最大(0.0387 mol/L)。
(2)水牛奶的表面张力小于荷斯坦牛奶的表面张力。二者在50℃时有最小值,分别为45.54 mN/m和46.99 mN/m;随着浓度的降低,表面张力值降低,在稀释2倍时表面张力值降低最快,浓度相同时水牛奶的表面张力值变化更快,随着稀释倍数的增加,二者的表面张力值降低趋于平缓。水牛奶表面张力值在50 mN/m左右,荷斯坦牛奶表面张力值在51 mN/m左右;水牛奶和荷斯坦牛奶样品在pH值为6.2时表面张力最小(49.66 mN/m),而在pH值为6.6时表面张力最小(48.47 mN/m)。
(3)水牛奶的平均粒径大于荷斯坦牛奶的平均粒径。前者在91.28~458.7 nm之间,质量分数为88.41%的水牛奶粒径分布在122.4~295.3 nm之间,而后者主要分布在91.28~190.1 nm之间。
(4)在pH值为4.2~7.0研究范围内,水牛奶的稳定系数要小于荷斯坦牛奶的稳定系数。水牛奶在pH值为4.7时沉淀率最大、稳定性最差,荷斯坦牛奶在pH值为4.6时沉淀率最大、稳定性最差;二者在pH值为6.2左右时沉淀量最小,稳定性最好。样品稀释4倍左右时,稳定性较好,荷斯坦牛奶的稳定性在稀释后变化显著,而水牛奶变化不显著。
[1] 曾寿瀛.现代乳与乳制品加工技术[M].中国农业出版社,2003.
[2] 梁明振,杨炳壮,苏安伟,等.水牛奶营养价值评价[J].广西畜牧兽医,2007,23(3):124-126.
[3] 韩刚.水牛奶的理化特性及其奶制品[J].乳品工业,1994(3):54.
[4] HAN B Z,MENG Y,LI M,et al.A Survey on the Microbiological and Chemical Composition of Buffalo Milk in China[J].Food Control,2007,18:742-746.
[5] LADISLAS C,MARCO T,SUSANN T,et al.Characterization and Biological Activity of Gangliosides in buffalo Milk[J].Biochimica et Biophysica Acta,2003,1631:94-106.
[6] GIUSEPPINA A,ENRICO T,ANDREA M.Characterization of Buffalo Milk by Pnuclear Magnetic Resonance Spectroscopy[J].Journal of Food Composition and Analysis,2006,19:843-849.
[7] SARFRAZ A,ISABELLE G,FLERENCE R,et al.Effects of Acidification on Physico-Chemical Characteristics of Buffalo Milk:A Comparison with Cow’s Milk[J].Food Chemistry,2008,106:11-17.
[8] CINZIA B,JOHN L,GIOVANNI S,et al.The Use of Multi Element Profiling to Differentiate between Cow and Buffalo Milk[J].Food Chemistry,2008,110:257-262.
[9] 许小刚,周雪松,曾建新.粒径分析法快速判定均质工艺对水牛奶稳定性的影响[J].中国乳品工业,2009,37(1):42-44.
[10] 郭本恒,骆承库,张书义.初乳的流变学特性研究[J].中国畜产与食品,2000,7(2):51-52.
[11] 王有龙.缓冲容量的实验验证[J].井冈山医专学报,2003,6:102-103.
[12] 赵红玲,李全阳,王婷婷,等.乳化剂对乳体系稳定性的影响[J].食品与发酵工业,2009,35(8):160-163.
[13] 赵正涛,李全阳,王秀菊,等.不同酸度条件下牛乳乳清蛋白的稳定性[J].食品与发酵工业,2009(8):156-159.
[14]赵法仍.营养百科[M].北京:中国大百科全书出版社,1990:316-332.
[15] 何长志.食品知识手册[M].北京:轻工业出版社,1991:312-349.
[16] SALAUN F,MIETTON B,GAUCHERON F.Buffering Capacity of Dairy Products[J].International Dairy Journal,2005,15:95–109.
[17] 陆则坚.牛奶检验与喷雾干燥中的粘度分析[J].农业工程学报,1995,11(4):144—148.
[18] LINA C,MARIA Q.Occurrence of Genetic Polymorphism at the αs1-casein Locus in Mediterranean Water Buffalo Milk[J].International Dairy Journal,2009,9:10-16.
[19] BRESCIA M A,MONFREDA M.Characterisation of the Geographical Origin of Buffalo Milk and Mozzarella Cheese by Means of Analytical and Spectroscopic Determinations[J].Food Chemistry,2005,89:139-147.
[20] 陈瑞芳,王世长,李兴芳,等.水牛初乳中免疫因子和生长因子质量浓度的研究[J].中国乳品工业,2010(3):19-21.
[21] 徐丽,张玉梅,张英华,等.牛初乳中可的松和氢化可的松质量分数变化[J].中国乳品工业,2009(11):18-20.
Comparison on technology characteristics of Guangxi buffalo milk and Holstein milk
YAO Chun-jie,LI Quan-yang,HUANG Zhong-chuang
(College of Light Industry and Food Engineering,Guangxi University,Nanning 530004,China)
In order to investigate the technology characteristics of Guangxi Buffalo milk and Holstein milk,the buffer capacity,surface tension,the distribution of particle size and stability factor were analysised and compared respectively in this paper.The results indicated that:the buffer capacity and the distribution of Buffalo milk particle size were 1.1 times and 2 times of Holstein milk respectively.For Buffalo milk,the maximum buffer capacity was at pH6.8,the minimum surface tension was at 50℃,and the most unstability state was at pH4.7;while for Holstein milk,the data of the same features are pH6.6,50℃and pH4.6.The distribution range of Buffalo milk particle size was 91.28~458.7 nm,the Holstein milk’s range was 91.28~190.1 nm.Therefor,there were many differences between the Buffalo milk and Holstein milk the technology characteristics.
buffalo milk;holstein milk;buffer capacity;distribution of particle size;surface tension
S823.9+1
A
1001-2230(2011)03-0030-04
2010-07-09
广西大学人才资助项目(XGZ090325)。
姚春杰(1984-),女,硕士,研究方向乳制品科学与技术。通讯作者:李全阳
