河南产尾叶香茶菜叶部位化学成分的分离与纯化*
2011-09-18吴月霞李继成杨丽嘉
吴月霞,张 伟,刘 娜,李继成,杨丽嘉
郑州大学药学院郑州450001
(2011-01-13收稿 责任编辑 徐春燕)
多年生草本植物尾叶香茶菜[Rabdosia excisus(Maxim.)H.Hara]系唇形科罗勒亚科香茶菜属,广泛分布于我国的东北地区、日本、朝鲜及俄罗斯远东地区[1]。在民间,全草入药具有清热解毒、活血破瘀、抗菌消炎及保肝抗癌等作用。实验[2]证明,尾叶香茶菜具有抑制人宫颈癌细胞生长的作用。目前有关尾叶香茶菜的化学成分已有报道,但考虑到不同产地的同一植物次生代谢产物很可能有差异,作者对产自河南省鲁山县地区的该种植物进行了研究,共计从尾叶香茶菜叶部位的粗提物石油醚和乙酸乙酯部分分离了10个化学成分,并通过各种波谱技术分析鉴定了所有化合物的结构。
1 材料与方法
1.1 材料 Rabdosia excisa叶于2009年8月采自河南省鲁山县,放置阴凉处自然晾干。原植物由郑州大学药学院李继成教授和河南省中医学院董诚明副教授鉴定,标本保存于郑州大学药学院标本馆。
1.2 仪器 DPX-400 400 MHz超导核磁共振仪(瑞士Bruker Avance),控温型XT4A显微熔点测定仪(北京科仪电光仪器厂),柱层析用硅胶(200~300目)和薄层层析用硅胶(GF254)由青岛海洋化工厂生产。
1.3 提取分离方法 取尾叶香茶菜干叶1.5 kg,用体积分数95%乙醇回流提取2次,每次1.5 h,减压浓缩得浸膏,将浸膏用甲醇溶解,加活性炭脱色后减压浓缩除去甲醇,用500 mL水分散浸膏,再分别用石油醚和乙酸乙酯萃取。浓缩石油醚和乙酸乙酯萃取液,得到橙黄色萃取物。分别将萃取物用甲醇溶解,拌200~300目硅胶进行硅胶柱层析,以石油醚-丙酮(体积比 9.5-0.5,9-1,8-2,7-3,6-4,5-5)、丙酮、甲醇,进行梯度洗脱,将粗分所得组分经过氯仿-甲醇(体积比同上)系统反复进行梯度洗脱,共得到10个化合物。
1.4 鉴定方法 通过核磁共振(1H-NMR,13CNMR)等波谱技术分析鉴定,并与标准品熔点(MP)及薄层层析作对比,与文献资料对照确定化合物的结构。
2 结果
化合物Ⅰ~Ⅹ的结构见图1。
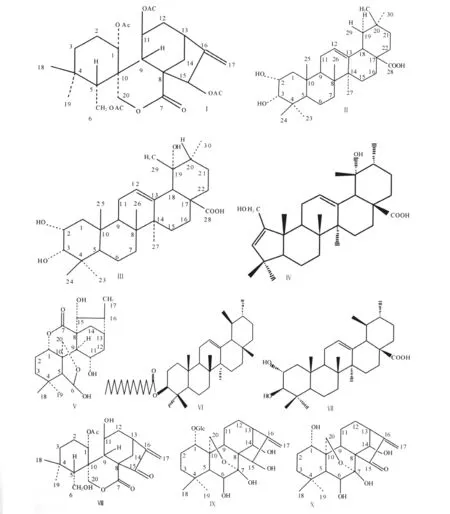
图1 化合物Ⅰ~Ⅹ的结构
化合物Ⅰ:针状结晶(石油醚-丙酮),MP 230~232 ℃。1H-NMR(400 MHz,CDCl3)δ 5.61(1H,t,J=2.5 Hz,H-15α),5.22(1H,d,J=1.6 Hz,H-17),5.02(1H,s,H-17),4.86(1H,d,J=11.6 Hz,H-11α),4.79 和 4.30(2H,ABd,J=11.9 Hz,H2-20),4.65(1H,dd,J=11.5,3.3 Hz,H-1β),4.43 和4.22(2H,dd,J=12.6,5.7 Hz,H2-6),3.26(1H,d,J=11.8 Hz,H-9β),2.84(1H,m,H-12α),2.54(1H,s,H-5β),2.26(1H,m,H-14α),22.6、2.09、2.04和1.99(each3H,s,4 × OAc),1.92(1H,d,J=13.1 Hz,H-2α),1.86(1H,m,H-2α),1.70(1H,d,J=13.0 Hz,H-14b),1.61(1H,m,H-2b),1.42(1H,dt,J=17.5,8.6 Hz,H-3α),1.21(1H,dd,J=13.1,9.2 Hz,H-3b),1.05(3H,s,Me-18),0.96(3H,s,Me-19);13C-NMR(100 MHz,CDCl3)δ 76.4(C-1),23.3(C-2),39.9(C-3),34.0(C-4),48.9(C-5),62.1(C-6),172.3(C-7),50.6(C-8),39.0(C-9),43.0(C-10),68.4(C-11),40.1(C-12),34.9(C-13),31.0(C-14),82.9(C-15),153.3(C-16),111.4(C-17),34.0(C-18),23.8(C-19),66.4(C-20)。OAc:170.5,169.6,169.5,168.9,21.3,21.2,21.1,21.1,20.9。以上波谱数据与文献[3]基本一致,确定为 1α,6,11β,15β-四乙酰基-6,7-断裂-7,20-内酯-对映-贝壳杉-16-烯(rabdosinate)。
化合物Ⅱ:白色粉末状物质(丙酮),Libermarm-Burchard反应阳性,说明可能为三萜类化合物,不饱和度为7。1H-NMR(400 MHz,Acetone)δ 5.25(1H,s,H-12),3.65(1H,m,H-2α),3.48(1H,d,J=9.2 Hz,H-3β),1.18(3H,s),1.02(3H,s),1.00(3H,s),0.95(3H,s),0.92(3H,s),0.82(3H,s),0.81(3H,s);13C-NMR(100 MHz,Acetone)δ47.6(C-1),68.0(C-2),83.1(C-3),39.3(C-4),55.3(C-5),18.2(C-6),33.6(C-7),38.9(C-8),48.0(C-9),38.0(C-10),23.3(C-11),122.0(C-12),144.14(C-13),41.7(C-14),27.5(C-15),22.9(C-16),46.7(C-17),41.3(C-18),45.9(C-19),30.4(C-20),34.2(C-21),33.2(C-22),29.3(C-23),16.8(C-24),16.5(C-25),17.6(C-26),25.4(C-27),177.9(C-28),32.7(C-29),22.9(C-30)。上述数据与参考文献[4]一致,鉴定该化合物为2α-羟基齐墩果酸。
化合物Ⅲ:白色粉末(氯仿),MP 268~270℃,Libermarm-Burchard反应阳性。1H-NMR(400 MHz,Acetone)δ 5.30(1H,brs,H-12),3.93(1H,d,J=12.8 Hz,H-2α),3.33(2H,d,J=5.6 Hz,H-3α),2.64(1H,td,J=13.3,4.6 Hz,H-18),1.36(3H,s),1.22(3H,s),1.00(3H,s),0.98(3H,s),0.95(3H,s),0.86(3H,s),0.77(d,J=11.6 Hz,3H);13CNMR(100 MHz,Acetone)δ41.7(C-1),65.4(C-2),78.6(C-3),39.9(C-4),48.0(C-5),18.0(C-6),32.9(C-7),41.4(C-8),47.4(C-9),38.0(C-10),23.8(C-11),127.9(C-12),138.8(C-13),42.2(C-14),26.4(C-15),26.11(C-16),48.0(C-17),53.6(C-18),72.4 C-19),42.5(C-20),25.5(C-21),37.6(C-22),29.4(C-23),16.5(C-24),15.9(C-25),15.7(C-26),23.4(C-27),178.3(C-28),26.4(C-29),15.6(C-30)。以上数据与文献[5]对照基本一致,确定化合物为 2α,3α,19-三羟基-12-烯-28-乌索酸(2α,3α,19-trihydroxy-urs-12-en-28-oic acid)。
化合物Ⅳ:白色粉末(丙酮),MP 208~210℃,Libermarm-Burchard反应阳性。1H-NMR(400 MHz,CDCl3)δ0.84(3H,s),0.94(3H,s),1.02(3H,s),1.14(3H,s),1.22(3H,s),1.36(3H,s),0.96(3H,d,J=5.6 Hz,Me-30),4.12 和 4.18(each1H,ABd,J=12.0 Hz,H-1a/b),5.27(1H,brs,H-12),5.39(1H,brs,H-3);13C-NMRδppm(100 MHz,CDCl3)60.2(C-1),155.7(C-2),133.3(C-3),41.4(C-4),63.1(C-5),17.1(C-6),34.1(C-7),41.6(C-8),41.7(C-9),50.4(C-10),26.1(C-11),128.1(C-12),138.9(C-13),41.8(C-14),29.3(C-15),26.5(C-16),47.4(C-17),53.8(C-18),72.3(C-19),43.0(C-20),26.3(C-21),37.6(C-22),29.5(C-23),21.0(C-24),18.3(C-25),18.1(C-26),25.5(C-27),178.3(C-28),26.3(C-29),15.7(C-30)。以上数据与文献[6]报道的hyptadienic acid一致。
化合物Ⅴ:无色针状结晶(石油醚-丙酮),易溶于氯仿、丙酮及甲醇等有机溶剂,MP 240~242℃。1H-NMR(400 MHz,MeOD)δ 5.26(1H,s,H-6α),5.17 和 5.16(2H,s,H2-17),4.96(1H,t,J=2.7 Hz,H-15β),4.70(1H,dd,J=11.4、6.1 Hz,H-1β),4.16(1H,m,H-11β),3.90 和 3.82(each 1H,ABd,J=8.9 Hz,H2-20),1.05(3H,s,Me-18),1.00(3H,s,Me-19);13C-NMR(100 MHz,MeOD)δ77.1(C-1),23.4(C-2),36.5(C-3),31.1(C-4),50.1(C-5),107.8(C-6),175.6(C-7),53.6(C-8),45.1(C-9),52.5(C-10),62.4(C-11),44.0(C-12),37.5(C-13),35.0(C-14),76.2(C-15),156.6(C-16),101.5(C-17),31.9(C-18),22.0(C-19),72.4(C-20)。以上数据与文献[7]相一致,确定该化合物为 epinodosinol。
化合物Ⅵ:白色粉末(石油醚),MP 75~76℃;1H-NMR(400 MHz,CDCl3)δ0.80(3H,s),0.83(3H,s),0.87(3H,s),0.88(3H,s),0.89(3H,s),0.91(3H,s),0.98(3H,s),1.01(3H,s),1.07(3H,s),4.50(1H,dd,J=5.6、6.8 Hz,H-3),5.12(1H,s,H-12);13C-NMRδppm(100 MHz,CDCl3)38.5(C-1),25.2(C-2),80.6(C-3),37.7(C-4),55.3(C-5),18.3(C-6),32.9(C-7),40.0(C-8),47.6(C-9),36.8(C-10),23.2(C-11),124.3(C-12),139.6(C-13),42.1(C-14),23.7(C-15),26.6(C-16),33.7(C-17),59.0(C-18),39.7(C-19),39.6(C-20),31.3(C-21),41.6(C-22),28.1(C-23),16.9(C-24),15.6(C-25),16.9(C-26),23.2(C-27),28.7(C-28),17.5(C-29),21.3(C-30),173.6(C-1’),34.9(C-2’),31.9(C-3’),29.2 ~ 19.7(C-4’~ C-13’),28.1(C-14’),22.6(C-15’),14.0(C-16’)。以上数据与文献[8]报道的α-香树脂醇棕榈酸酯(α-amyrin palmitate)一致。
化合物Ⅶ:白色粉末(甲醇),MP 270~272℃,Libermarm-Burchard反应阳性。1H-NMR(400 MHz,Acetone)δ 5.24(1H,s,H-12),3.93(1H,d,J=10.9 Hz,H-2β),3.31(1H,s,H-3β),2.24(1H,d,J=11.5 Hz,H-18),1.14(s,3H),1.08(3H,s),0.99(3H,s),0.98(3H,s),0.89(d,J=6.5 Hz,3H),0.85(3H,s),0.83(3H,s);13C-NMR(100 MHz,Acetone)δ39.7(C-1),65.4(C-2),78.5(C-3),38.9(C-4),47.4(C-5),17.8(C-6),32.95(C-7),39.1(C-8),36.7(C-9),37.9(C-10),24.1(C-11),125.3(C-12),138.5(C-13),42.0(C-14),27.8(C-15),23.1(C-16),47.9(C-17),52.9(C-18),39.7(C-19),38.1(C-20),30.6(C-21),37.0(C-22),30.5(C-23),23.3(C-24),16.0(C-25),16.7(C-26),20.6(C-27),177.8(C-28),33.5(C-29),16.9(C-30)。将以上数据与文献[9]报道值相比较,确定该化合物为2α,3α-二羟基乌苏-12-烯-28-酸。
化合物Ⅷ:无色针状结晶(氯仿),易溶于氯仿、丙酮等溶剂,MP 250~252 ℃。1H-NMR(400 MHz,CDCl3)δ6.08(1H,s,H-17a),5.57(1H,s,H-17b),5.13(1H,dd,J=9.9、5.1 Hz,H-1β),4.94(1H,d,J=12.4 Hz,H-20a),4.38(1H,d,J=12.4 Hz,H-20b),3.97(1H,dd,J=17.9、10.0 Hz,H-14α),3.75(2H,brs,H2-6),3.10(1H,dd,J=9.5、4.7 Hz,H-13α),2.67(1H,ddd,J=13.8、9.5、7.2 Hz,H-12α),2.62(1H,dd,J=4.8、12.0 Hz,H14β),2.55(1H,dd,J=9.2、14.2 Hz,H-12β),2.04(3H,s,OAc),1.96(1H,d,J=12.7 Hz,H-5β),1.88(2H,m,H-2β 和 H-12α),1.35-1.27(2H,m,H2-3),1.07(3H,s,Me-18),0.88(3H,s,Me-19);13CNMR(100 MHz,CDCl3)δ76.4(C-1),24.3(C-2),39.2(C-3),33.9(C-4),52.8(C-5),59.7(C-6),170.2(C-7),58.0(C-8),46.6(C-9),44.2(C-10),65.9(C-11),41.6(C-12),34.2(C-13),29.3(C-14),200.7(C-15),149.6(C-16),119.8(C-17),33.8(C-18),23.9(C-19),67.5(C-20),OAc169.72,21.5。以上数据与文献[10]对照,确定化合物为maoyecrystal E。
化合物Ⅸ:无色针状结晶(氯仿-甲醇),溶于丙酮、甲醇等有机溶剂。1H NMR(400 MHz,MeOD)δ5.15(1H,s,H-17 a),5.12(1H,d,J=2.3 Hz,H-17 b),4.89(1H,d,J=2.3 Hz,H-14α),4.54(1H,s,H-6α),4.33 和 4.03(each1H,d,J=10.3 Hz,H-20),4.28(1H,d,J=7.7 Hz,Glu 端基),3.60(1H,t,J=8.0 Hz,H-1β),1.11(3H,s,H-18),0.99(3H, s,-19);13C-NMR(100 MHz,MeOD)δ83.7(C-1),27.5(C-2),38.3(C-3),32.9(C-4),57.6(C-5),72.1(C-6),98.4(C-7),52.5(C-8),44.6(C-9),40.7(C-10),17.8(C-11),31.9(C-12),45.6(C-13),74.2(C-14),70.2(C-15),159.12(C-16),108.3(C-17),31.6(C-18),20.6(C-19),61.4(C-20),103.33(C’-1),74.4(C’-2),77.1(C’-3),70.8(C’-4),76.3(C’-5),63.0(C’-6)。以上数据与文献[11]对照基本一致,确定该化合物为enmenol-glucoside。
化合物Ⅹ:无色针状结晶(氯仿-甲醇),MP 248~250℃;易溶于丙酮、甲醇等有机溶剂。1HNMR(400 MHz,Acetone)δ6.21 和5.51(each1H,s,H2-17)6.03 ~ 5.99(2H,brs,OH),5.21(1H,s,H-14α),4.24 和 3.98(1H,ABd,J=10.2、1.4 Hz,H2-20),3.50(1H,t,J=5.0 Hz,H-1β),3.01(1H,d,J=9.8 Hz,H-6),1.09(3H,s,H-18),1.06(3H,s,H-19);13C-NMR(100 MHz,Acetone)δ74.0(C-1),30.4(C-2),38.7(C-3),33.4(C-4),60.0(C-5),72.9(C-6),97.4(C-7),62.9(C-8),54.0(C-9),41.1(C-10),21.4(C-11),30.8(C-12),43.3(C-13),72.73(C-14),208.2(C-15),152.7(C-16),118.2(C-17),32.4(C-18),19.6(C-19),62.20(C-20)。以上数据与文献[12]对照,确定该化合物为冬凌草甲素(oridonol)。
3 讨论
通过波谱技术分析鉴定,并与标准品熔点及薄层层析作对比及文献资料对照,确定化合物的结构,鉴定了从尾叶香茶菜叶中分离到的10个化合物。化合物Ⅰ~Ⅸ均为首次从尾叶香茶菜中得到,化合物冬凌草甲素(Ⅹ)从香茶菜属植物中曾分离得到。
[1]那微,鲍建材,刘刚,等.中药尾叶香茶菜研究现状及药用前景展望[J].人参研究,2006,18(1):13
[2]刘亚男,金永日,钟加藤,等.尾叶香茶菜二萜类化合物B对人体宫颈癌细胞的生长抑制作用及其机制[J].吉林大学学报:医学版,2010,36(1):54
[3]丁兰,王玮,汪涛,等.甘肃产蓝萼香茶菜二萜化学成分研究[J].广西植物,2008,28(2):265
[4]吴晓萍.小叶榕叶的活性成分及质量标准研究[D].广州:广州中医药大学,2007.
[5]任风芝,栾新慧,屈会化,等.紫珠叶的化学成分研究(Ⅱ)[J].中国药学杂志,2001,36(7):445
[6] Taniguchi S,Imayoshi Y,Kobayashi E,et al.Production of bioactive triterpenes by Eriobotrya japonica calli[J].Phytochemistry,2002,59(3):315
[7]丁兰,景宏伟,王涛,等.甘肃产毛叶香茶菜二萜成分及其化感潜能评估[J].西北师范大学学报:自然科学版,2010,46(2):88
[8]吴弢,程志红,刘和平,等.中药枸骨叶脂溶性化学成分的研究[J].中国药学杂志,2005,40(19):1460
[9]刘赟,周欣,龚小见,等.鬼箭羽化学成分的研究(Ⅲ)[J].中草药,2010,41(11):1780
[10]Han QB,Zhang JX,Shen YH,et al.Diterpenoids from Isodon japonicus[J].Chin J Nat Med,2003,1(1):16
[11]蔡明磊,高慧媛,黄健,等.冬凌草地上部分的化学成分[J].沈阳药科大学学报,2008,25(11):871
[12]确生,赵玉英,周勇,等.藏药小叶毛球莸中对映-贝壳杉烯型二萜类成分研究[J].中国中药杂志,2009,34(12):1523