高效液相色谱法测定普瑞巴林胶囊的含量
2011-09-17曹杨远
肖 健,曹杨远
(福建卫生职业技术学院食品药品研究所,福建 福州 350101)
普瑞巴林(pregabalin,PGB)的化学名为 (S)-(+)-3-氨甲基-5-甲基己酸,是美国辉瑞公司研究开发的一种γ-氨基丁酸(GABA)受体阻滞剂,用于治疗部分癫痫发作,其作用机制是通过抑制中枢神经系统电压依赖性钙通道的一种α2-σ亚基蛋白,减少神经末梢的去极化,减少Ca2+内流,从而减少兴奋性神经递质的释放[1]。普瑞巴林的治疗指数高,不良反应少,是一种市场潜力巨大、安全有效的抗癫痫药物。目前普瑞巴林的含量测定方法有紫外光谱法和荧光光谱法[2]、高效液相色谱紫外检测法[3-6]、高效液相色谱荧光检测法[7]以及高效液相色谱-质谱法[8]。笔者采用高效液相色谱法紫外检测法测定了普瑞巴林胶囊的含量,现报道如下。
1 仪器与试药
Agilent 1100型高效液相色谱仪,N2000型色谱工作站(浙江大学智能信息工程研究所)。普瑞巴林对照品(美国辉瑞公司提供,批号为20080908);普瑞巴林胶囊(美国辉瑞公司,规格为50 mg/粒,批号为 20090125,20090314,20090316,20090318);试验用甲醇、乙腈为色谱纯,磷酸盐为分析纯,水为二次蒸馏水。
2 方法与结果
2.1 色谱条件与系统适用性试验
色谱柱:C18柱(150 mm ×4.6 mm,5 μm);流动相:甲醇 - 乙腈-pH=7.0的20 mmol/L磷酸盐缓冲液(400∶150∶450);流速:1.0 mL/min;检测波长:210 nm;进样量:20 μL;柱温:35℃。称取普瑞巴林对照品24.7 mg,置25 mL量瓶中,加10%流动相溶解并稀释至刻度,摇匀,取20 μL进样测定。结果其保留时间为3.440 min(见图1),理论板数为9 829.6,拖尾因子为1.14,可满足测定要求。

图1 普瑞巴林色谱图
2.2 方法学考察
标准曲线绘制:精密称取普瑞巴林对照品199.6 mg,置100 mL量瓶中,用流动相溶解并稀释到刻度,摇匀,配成对照品贮备液。再分别精密量取 3.0,4.0,5.0,6.0,7.0 mL 置 10 mL 量瓶中,用流动相稀释至刻度,分别取20 μL进样,测定峰面积,以峰面积(A)对质量浓度(C,μg/mL)进行线性回归,得标准曲线 A=17 462.9 C+540.7,r=0.999 7(n=5)。结果表明,普瑞巴林质量浓度在598.8~1 397.2 μg/mL范围内与峰面积呈良好的线性关系。
最低检测限:取普瑞巴林对照品适量,加流动相溶解并逐级稀释,进样20μL测定。按3倍信噪比计算,普瑞巴林最低检测质量浓度为 4.94 μg/mL。
进样精密度:精密称取普瑞巴林对照品25.1 mg,置25 mL量瓶中,用流动相溶解并稀释至刻度,摇匀,连续进样6次。结果的RSD为0.92%,表明方法进样精密度良好。
中间精密度:分别取样品胶囊(批号为20090125)内容物细粉适量(约相当于普瑞巴林25 mg),精密称定,由不同的操作者,使用不同的仪器,于不同的时间,照含量测定项下方法操作,测定并计算普瑞巴林胶囊的含量。结果平均含量为101.1%,RSD=0.89%,表明方法的中间精密度良好。
重复性:取本品胶囊(批号为20090125)内容物细粉适量(约相当于普瑞巴林25 mg),共6份,精密称定,分别置25 mL量瓶中,加流动相至3/4量瓶,超声5 min,加流动相至刻度,摇匀,过滤,取续滤液作为供试品溶液,取20 μL进样测定,用标准曲线法计算普瑞巴林的含量。结果平均含量为100.1%,RSD=1.05%(n=6),表明方法的重复性较好。
加样回收试验:取已知含量(99.6%)的胶囊内容物适量(约相当于普瑞巴林12.5 mg),共9份,3份为1组,精密称定,分别置25 mL量瓶中;分别精密加入对照品贮备液(1.996 g/L)5.0,6.2,7.5 mL制成低、中、高3种不同质量浓度的溶液(各3份,每份平行操作2份),加流动相稀释至刻度,精密量取20 μL进样,测定含量并计算普瑞巴林的回收率。结果见表1。
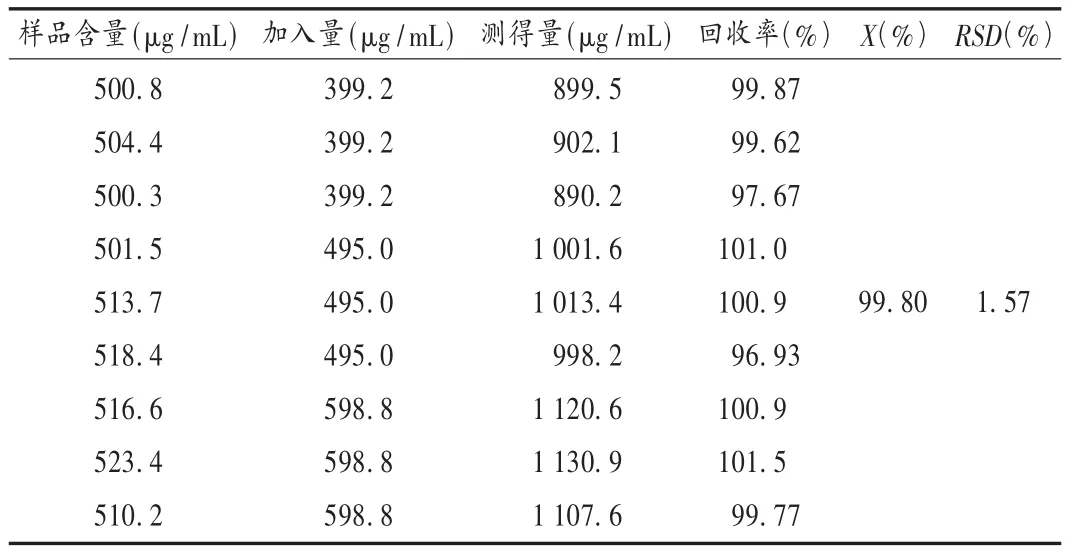
表1 普瑞巴林加样回收试验测定结果(n=9)
2.3 含量测定
取装量差异项下胶囊内容物细粉适量(约相当于普瑞巴林50 mg),置50 mL量瓶中,加流动相至约3/4量瓶,超声5 min,加流动相至刻度,摇匀,过滤,取续滤液作为供试品溶液(1 g/L),另取普瑞巴林对照品(约25 mg),精密称定,置25 mL量瓶中,加流动相稀释至刻度,摇匀,配成质量浓度为1 g/L的溶液作为对照品溶液。分别取对照品溶液和供试品溶液各20 μL进样测定,记录峰面积,按外标法以峰面积计算标示量的百分含量。结果批号为20090314,20090316,20090318的样品中普瑞巴林含量分别为标示量的99.6%,101.1%,100.7%(n=3),3批样品的含量均符合规定。
3 讨论
采用高效液相色谱法紫外检测法测定普瑞巴林胶囊的含量,方法准确度高、精密度好,适用于其质量控制。
[1]赵立波,谢代鑫.抗癫痫新药普瑞巴林[J].临床神经电生理学杂志,2008,17(3):177-178.
[2]Armagan ǒnal,Olcay Sagirli.Spectrophotometric and spectrofluorimetric methods for the determination of pregabalin in bulk and pharmaceutical preparation[J].Spectrochimica Acta Part A,2009,72:68 -71.
[3]JadhavAS,Pathare DB,Shingare MS.Validated enantioselective LC method with precolumn derivatization with Marfey's reagent for analysis of the antiepileptic drug pregabalin in bulk drug samples[J].Chromatographia,2007,65(3/4):253 -256.
[4]吴琼珠,陈 润,乔善磊,柱前手性衍生化-HPLC法测定普瑞巴林的光学纯度[J].中国药科大学学报,2007,38(6):523-526.
[5]张道林,邓 杰,陈晓晖.柱前衍生化高效液相色谱法测定普瑞巴林中的光学异构体[J].药物分析杂志,2007,27(12):1 884-1 886.
[6]Berry David,Millington Christopher.Analysis of Pregabalin at Therapeutic Concentrations in Human Plasma/Serum by Reversed-Phase HPLC[J].Therapeutic Drug Monitoring,2005,27(4):451 - 456.
[7]VermeijTAC,Edelbroek PM.Simultaneous high-performance liquid chromatographic analysis of pregabalin,gabapentin and vigabatrin in human serum byprecolumn derivatization with o-phtaldialdehydeand fluorescence detection[J].JournalofChromatography B,2004,810:297-303.
[8]Yizhong Zhang,Christopher Holliman,Daniel Tang.Development and validation of a direct enantiomeric separation of pregabalin to support isolated perfused ratkidneystudies[J].JournalofChromatographyB,2008,875:148 -153.
