肝动脉化学栓塞联合多极射频消融治疗大肝癌的疗效
2011-08-02梁明辉齐齐哈尔医学院黑龙江齐齐哈尔161006
梁明辉 (齐齐哈尔医学院,黑龙江 齐齐哈尔 161006)
原发性肝癌由于起病隐匿,患者就诊时大多数已属中晚期,肿瘤巨大,因此,肝癌患者手术切除率很低,往往失去最佳治疗时机。以往临床对大肝癌的治疗多采用经导管动脉化学栓塞(transcatheter arterial chemoemblization,TACE);近年来,由于仪器性能的完善以及治疗技术的娴熟,经皮射频消融术(radiofrequency ablation,RFA)等局部热凝固已被用于治疗肝癌并取得较好疗效〔1〕;临床证实采用优化的计算治疗方案以及综合治疗等方法可进一步提高大肝癌疗效〔2〕。但对肿瘤邻近大血管及血管丰富的大肿瘤治疗,仍易发生残留,是一个亟待解决的研究课题〔3〕。本研究对血供丰富的大肝癌行TACE后RFA治疗,并与单纯RFA及单纯TACE治疗大肝癌的效果进行比较,探讨RFA联合TACE对大肝癌的治疗意义。
1 资料与方法
1.1 研究对象 2004年2月至2006年7月,共计78例经病理确诊(65例)或临床诊断〔至少两种影像学检查,结合甲胎蛋白(AFP)>400 ng/ml,13例〕为原发性肝癌者进入本研究。肿瘤最大径5.2~10.1 cm,平均(6.5±0.7)cm。男63例,女15例,年龄45~75〔平均(60.3±9.6)〕岁。患者因高龄,心、肺功能障碍,肿瘤大小、位置等原因不适宜手术治疗。31例病人(57个病灶)先行TACE治疗后再行RFA治疗(综合组);23例(32个病灶)行单纯RFA治疗(RFA组),24例(47个病灶)行单纯TACE治疗(TACE组)。治疗前全部病例行血常规、AFP、全套肝功能检查,并做Child-Pugh分级。三组病例的平均年龄、病灶大小以及肝功能分级(Child-Pugh法),见表1,图1,图2。
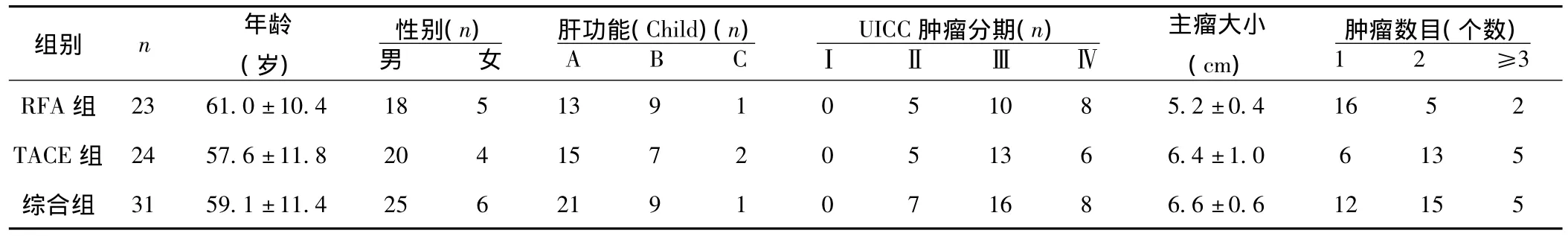
表1 47例原发性肝癌患者三种治疗方法病例资料
1.2 仪器与方法
1.2.1 RFA组 在CT引导下进行,采用经皮途径。WE7568多电极射频消融治疗仪,输出功率为100~150 W。消融针为带侧孔的14G的WHK-4多极消融套针,内套针顶端设有9根细电极针,伸展通电后可形成5.0 cm球形热凝固灶。本组病例采用正棱柱法布针5~8个点或3层重叠法布针12个点,以取得覆盖灭活大癌灶的治疗效果,具体布针方法参照文献〔2〕。
1.2.2 TACE组 运用Seldinger技术,经皮股动脉穿刺导管尽可能超选至肿瘤供血动脉再进行化学栓塞术。应用化疗药物为表阿霉素(EPI-ADM)30~50 mg,羟基喜树碱(HCPT)15~20 mg。栓塞剂为超液化碘油15~30 ml和明胶海绵,一般治疗3~7次。
1.2.3 综合组 先行TACE治疗,方法及使用药物同前。视患者肝功能情况及全身反应的轻重,行1~3次TACE治疗。本组病例均为治疗后经CT或数字减影血管造影检查评价未取得彻底灭活疗效,在TACE后1 w左右再接受RFA治疗。
1.2.4 临床观察 所有患者及时记录TACE和RFA并发症;术后1 w复查AFP、血常规和肝肾功能;术后1个月采用增强CT评价肿瘤坏死情况,增强CT显示肿瘤区无活性、参考AFP下降接近或达正常可确认肿瘤完全坏死;以后每隔2~3个月复查AFP、增强CT监测局部复发情况,并评价肿瘤大小变化,肿瘤长径缩小10%以上判定为肿瘤缩小。随访期间发现肿瘤局部表现活性可追加介入化疗栓塞或射频治疗。
1.3 统计学分析 应用SPSS10.0统计软件,连续变量资料采用表示,采用独立样本t检验比较肿瘤大小及平均年龄。采用χ2检验和Fisher检验比较计数资料的分布差异。采用Kaplan-Meier法计算预期生存率并预测平均生存期。
2 结果
综合组治疗后肿瘤完全性坏死率、肿瘤缩小率明显优于单纯RFA组、TACE组(P<0.05,P<0.01)。局部复发率三组无明显差异;术后平均生存期综合组大于单纯RFA组及TACE组(P<0.05,P<0.01)。平均治疗次数为 RFA组1.7次/例,TACE组为3.5次/例;综合组TACE平均为2.6次/例,RFA平均1.4次/例。见表2,表3。
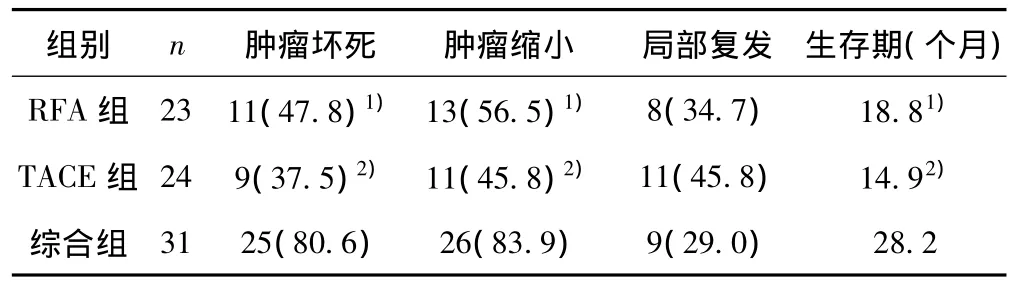
表2 78例原发性肝癌三种治疗方法疗效比较〔n(%)〕
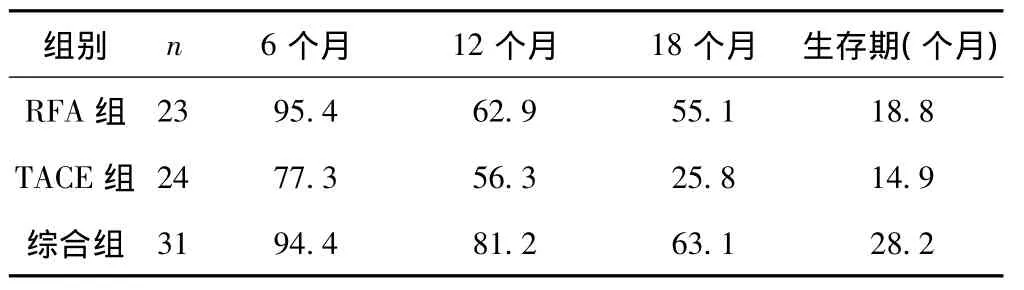
表3 78例原发性肝癌三种治疗方法术后生存时间比较(%)
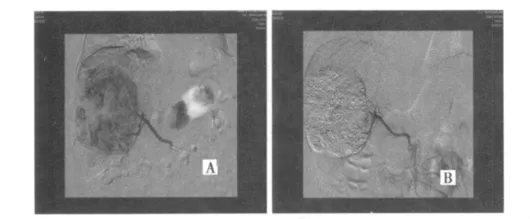
图1 原发性肝癌TACE治疗前后DSA造影
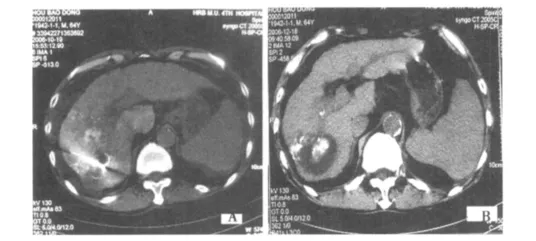
图2 增强CT示原发性肝癌(6.3 cm)单纯化疗栓塞后肿瘤仍残存活性
3 讨论
肝癌是死亡率最高的癌症之一,肝癌的治疗目前首推手术切除,但在我国其切除率一般不足20%。经导管动脉栓塞治疗肝癌是非手术疗法的首选方法,对延长中晚期肝癌患者的生存期取得了良好效果,疗效肯定,但对大肝癌此方法依然存在不能完全杀灭肿瘤的缺点〔3〕。RFA是一种安全可靠的局部肝癌治疗方法,对直径 <3.0 cm 肝癌的疗效已得到充分肯定〔1,3〕。随着射频设备及治疗技术的进步,包括采用注射盐水、多支射频针和以数学球体覆盖公式设计治疗方案等,有效热凝治疗范围能扩大至7.0 cm左右。因此,在临床上RFA已开始应用于大肝癌治疗,并已有疗效良好的报道〔4,5〕。但文献报道单纯RFA治疗大肝癌存在易残留和复发率较高等问题,对>5 cm肝癌肿瘤完全坏死率24% ~41%,肿瘤局部复发率达36.6% ~47.8% ,说明单纯 RFA 治疗大肝癌疗效仍欠佳〔4,5,7,10〕;故应采用综合治疗方法,进一步提高RFA治疗大肝癌疗效。
本研究通过对血供丰富的大肝癌行TACE联合RFA综合治疗,并与单纯RFA及单纯TACE治疗大肝癌的结果进行对照分析,结果显示综合组术后肿瘤完全坏死率明显高于单纯TACE组及单纯RFA组,与文献报道相近〔1,3〕。单纯RFA治疗大肝癌,可能在三维空间上存在消融灶之间热凝固遗漏区;或由于肿瘤形态不规整、呈浸润性生长、与大血管或重要脏器毗邻等因素,导致肿瘤消融灭活范围不足。有报道证实,血流对RFA的范围有较大的负面影响,即血流对RFA治疗有冷却作用,而TACE后血管闭塞可减少瘤区的血流,从而减少对RFA疗效的影响〔3〕。
采用单纯TACE治疗大肝癌,肿瘤完全坏死率低,根治疗效不理想〔3,5,6~8〕。本组研究栓塞一般约需进行 3 ~7 次治疗,由于化疗药物的毒副作用,反复TACE治疗常引起肝功能衰竭等并发症,甚至造成死亡。
肿瘤组织的灭活与温度密切相关。有研究报道,RFA前行TACE治疗时用碘化油及明胶海绵微粒栓塞,注入的碘化油通过多重动门脉交通填充至肿瘤周围的门脉终支,可短暂减少肿瘤周围血运,从而也减少了血运的冷却作用,使射频电极有效升温,提高肿瘤的凝固坏死〔11〕。此外,大肝癌先行TACE治疗,在取得肿瘤部分坏死、缩小后再行RFA治疗,有利于肿瘤边缘组织纳入有效热凝覆盖范围,从而获得彻底灭活。文献报道在化疗有效降低肿瘤组织耐氧力的状态下,可提高热疗肿瘤组织坏死率;高温则能进一步增强化疗药物对肿瘤细胞的杀伤力〔8,9〕。故在TACE后再行RFA治疗,使肿瘤更易发生完全凝固坏死;另外,TACE联合RFA治疗大肝癌的处置方法与疗效相关〔3〕。倘若先行RFA治疗可造成肿瘤主要营养血管闭塞,不利于栓塞剂和化疗药物经荷瘤血管进入肿瘤区域而影响TACE治疗效果,故一般主张先行TACE再行RFA治疗。
综合组肿瘤复发率虽低于单一方法治疗,但差异无统计学意义。笔者考虑综合组复发率低的原因可能为TACE治疗抑制瘤内瘤周血供以及在肿瘤缩小后联合RFA治疗,提高了肿瘤坏死率;此外,TACE还可能有利于对RFA术前未能发现的微小子灶和肿瘤周围的微血管浸润进行有效治疗而抑制肝内转移、复发。综合组平均TACE治疗次数为2.6次/例,少于单纯TACE组的平均3.5次/例,而术后生存时间明显优于单纯TACE组。提示综合治疗可减少TACE治疗次数,从而保护肝储备功能,并有效提高肿瘤治疗水平,延长生存期。
1 张智坚,吴孟超,陈 汉,等.经皮肝穿刺射频热凝与肝动脉化疗栓塞联合治疗肝细胞癌〔J〕.中华外科杂志,2002;40(11):826-9.
2 杨 薇,陈敏华,严 昆,等.射频消融对较大肝肿瘤治疗范围与布针方案计算的研究〔J〕.中华超声影像学杂志,2002;11:244-7.
3 吴沛宏,张福君,赵 明,等.肝动脉栓塞化疗联合CT导向射频消融术治疗中、晚期肝癌的评价〔J〕.中华放射学杂志,2003;37(10):901-4.
4 张利辉,崔 忠,赵清涛,等.射频联合肝动脉栓塞化疗及无水酒精注射治疗不能手术切除肝癌〔J〕.中国普通外科杂志,2002;11(9):525-7.
5 Buscarini L,Buscarini E,Distasi M,et al.Percutaneous radiofrequency thermal ablation combined with transcatheter arterial embolization in the treatment of large hepatocellular carcinoma〔J〕.Ultraschall Med,1999;20(2):47-53.
6 Livraghi T,Goldberg SN,Lazzaroni S,et al.Hepatocellular carcinoma:radio-frequency ablation of medium and large lesions〔J〕.Radiology,2000;214(3):761-8.
7 Ryu M,Shmamura Y,Kinoshita T,et al.Therapeutic results of resection,transcatheter arterial embolization and percutaneous transhepatic ethanol injection in 3225 patients with hepatocellular carcinoma:a retrospective multicenter study〔J〕.Jpn J Clin Oncol,1997;27(4):251-7.
8 Machi J,Uchida S,Sumida K,et al.Ultrasound-guided radiofrequency thermal ablation of liver tumor:percutaneous,laparoscopic,and open surgical approaches〔J〕.J Gastrointest Surg,2001;5(5):477-89.
9 Seegenchmiedt MH,Brady LW,Sauer R.Interstitial thermoradiotherapy:review on technical and clinical aspects〔J〕.Am J Clin Oncol,1990;13(4):352-63.
10 Veltri A,Moretto P,Doriguzzi A,et al.Radiofrequency thermal ablation(RFA)after transarterial chemoembolization(TACE)as a combined therapy for unresectable non-early hepatocellular carcinoma(HCC)〔J〕.Eur Radiol,2006;16(3):661-9.
11 Sugimori K,Nozawa A,Morimoto M,et al.Extension of radiofrequency ablation of the liver by transcatheter arterial embolization with iodized oil and gelatin sponge:results in a pig model〔J〕.J Vasc Interv Radiol,2005;16(6):849-56.
