一锅法制备三降达玛烷型三萜*
2011-07-26赵声定苑家鑫解宇环唐丽萍朱华结
张 滢,赵声定,邹 澄△,赵 庆,苑家鑫,解宇环,唐丽萍,朱华结
(1.昆明医学院药学院,云南昆明 650500;2.云南中医学院中药学院,云南昆明 650500;3.中国科学院昆明植物研究所,云南昆明 650204)
丰产易得天然产物结构改造可以高效率地制备衍生物库供活性筛选[1]。三七位居云南名药之首,资源丰富,活性成分皂苷含量高[2],药农愿栽,制药企业积极生产,但三七的研发以皂苷提取分离为主,对皂苷元的结构改造研究与开发很有限,且主要集中在 C30型碳骨架的达玛烷三萜上[3,4]。三七皂苷抗肿瘤活性有苷元>单糖苷>双糖苷>三糖苷>四糖苷的特点[5],故研究三七皂苷元结构改造具有重要意义。
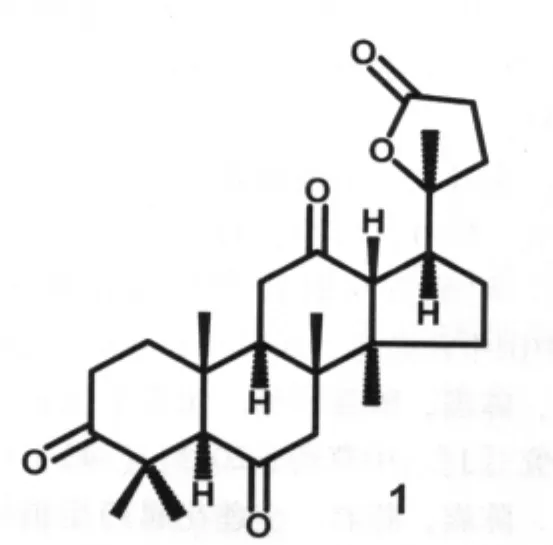
图1 产物化合物1
三七皂苷元的结构修饰一般采用皂苷水解后分离苷元再衍生化的方法,操作比较复杂,且只得到C30型苷元衍生物。我们用原人参二醇型总皂苷为原料“一锅法”制备了C27型和 C24型苷元衍生物[6]。本文报道对三七原人参三醇型总皂苷直接用琼斯氧化,即将水解反应与氧化反应合并为“一锅”,简明得到一个三降达玛烷型三萜 (C27型)衍生物。
1 实验部分
1.1 试剂与仪器
三氧化铬 (AR);硫酸 (AR);丙酮 (AR);氯仿 (AR);石油醚 (AR);乙酸乙酯 (AR);层析硅胶 (青岛海洋化工厂);高效硅胶G板 (青岛海洋化工厂);显色剂 (V(硫酸)∶V(乙醇)=100∶5);原人参三醇型总皂苷购自云南昆明圣火制药厂。
瑞士AM-400型核磁共振波谱仪 (中国科学院昆明植物研究所仪器测定中心)。
1.2 Jones试剂的制备
称取三氧化铬固体26.72g,加入适量蒸馏水使其溶解,再分批加入23mL浓硫酸,并不断搅拌,最后加入适量水稀释至100mL。
1.3 原人参三醇型总皂苷的琼斯氧化
取原人参三醇型总皂苷6g,加入约50mL水和约50mL的丙酮充分溶解,再加入56mL琼斯试剂,置室温下搅拌反应1h后,加入0.5倍液体体积的水后,用氯仿萃取3次,合并回收得3.5g反应物。反应物经硅胶H柱层析分离,用石油醚:乙酸乙酯 (2:3)洗脱,经浓缩、重结晶得到化合物1,无色结晶,重480mg(见图1)。
1.4 光谱数据
1 C27H38O5为无色结晶。=+52.5(c=7.65mg/mL,CD3CI);
MS:442+, 442(30), 385(12), 343(17),181(38),163(20),124(25),109(27),99(100);
IR(KBr): νmax3435,2980,1771,1706,1455, 1385, 1257, 1209, 1163, 1088, 916,621cm-1;
13C - NMR(400MHz,CD3OD),δ:40.5(t,C -1);33.5(t,C -2);209.3(s,C -3);55.2(s,C -4);64.6(s,C -5);208.6(s,C-6);42.7(s,C -7);45.9(s,C -8);39.5(d,C -9);42.7(s,C -10);51.6(t,C -11);213.4(s,C - 12);56.3(s,C - 13);46.9(s,C - 14);32.2(t,C - 15);24.0(d,C-16);53.3(d,C-17);16.6(q,C-18);15.9(q,C -19);88.2(s,C -20);21.5(q,C -21);31.5(t,C -22);28.8(t,C -23);176.7(s,C -24);24.0(q,C -25);25.0(q,C-26);16.3(q,C-27)。
2 结果与讨论
谱图分析:红外光谱表明,3000cm-1以上无峰,说明不含双键。1771cm-1,1706cm-1,为两个羰基峰。质谱 (EIMS)给出分子量为442。13CDEPT谱显示共有27个碳,包括6个 CH3,8个CH2,4个CH,8个季碳,累计为C27H38。其中还有4个羰基信号,其中176.7单峰应该为新生成的季碳上的羰基。
化合物的生成机理为:
6、20位糖链在反应条件下脱去,6位羟基与3、12位羟基被氧化成酮;24、25位双键先被氧化成邻二羟基,再继续氧化断链脱去25、26、27三个碳原子 (碳架因而改变),24位碳氧化成羧酸,与20位羟基脱水生成γ-内酯 (见图2)。
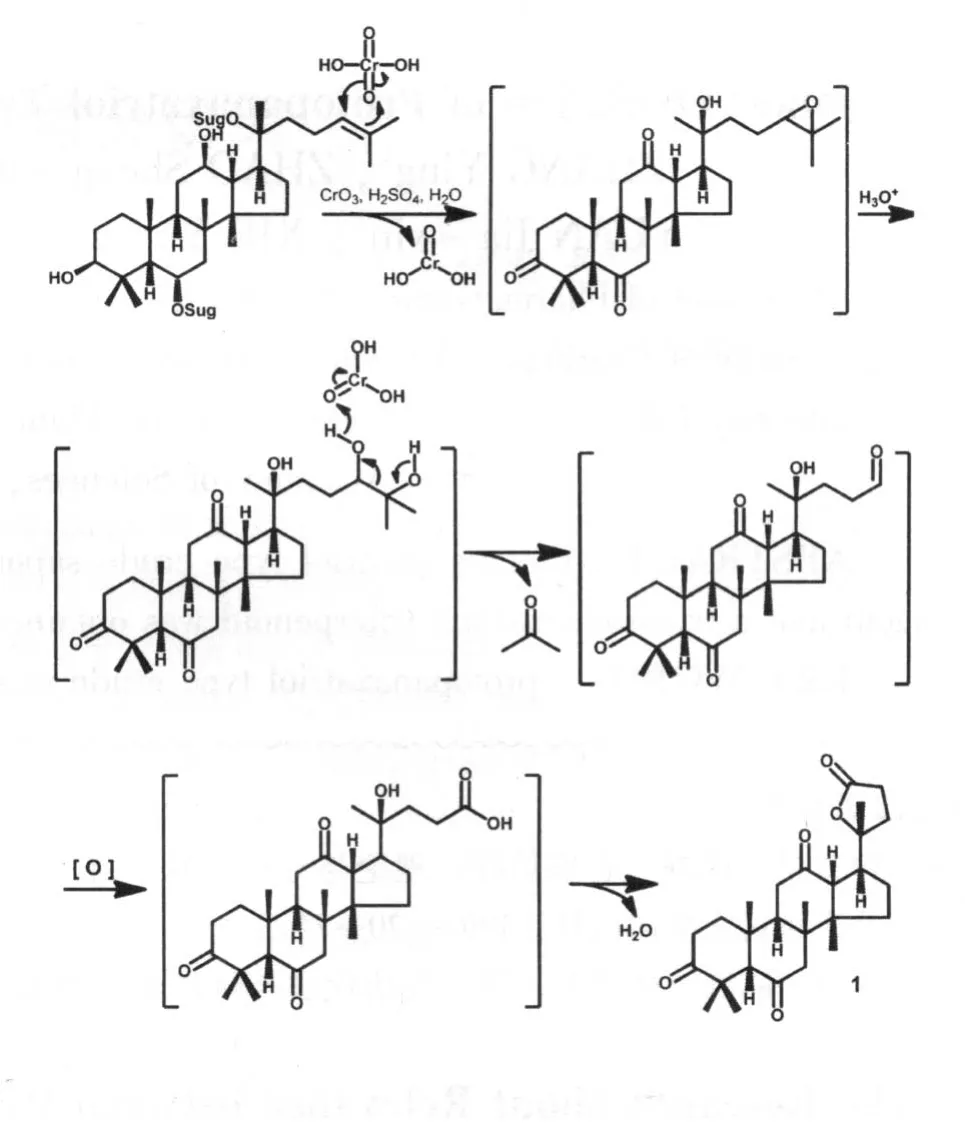
图2 生成机理
由于该化合物简明易得,除值得研究其本身的生物活性外,更可以方便地用作进一步结构改造的原料,新碳架的生成意味着可以制备大量新衍生物供活性研究。
[1]邹澄,赵庆,郝小江,等.丰产易得天然产物结构改造值得重视 [J].中国民族民间医药杂志,2004,68:135-137.
[2]浦湘渝,张荣平,邹澄.不同产地三七总皂甙的含量研究 [J].云南中医中药杂志,2001,22(4):36.
[3]Wei J X,Chen W S,BreitmaierE,Two new dammaran sapogenins from leaves of Panax notoginseng[J].Planta Medica,1982,45(3):167 -171.
[4]Wei J X,Chen W S,Breitmaier E,et al,An oxepane derivative of panaxadiol from the leaves of Panax notoginseng [J].Planta Medica,1984,48(1):47-52.
[5]陈英杰,王红燕,徐绥绪,等.人参化学成分及其抗癌抗心律失常构效关系的研究 [J].中国科学基金,1995,(4):46-48.
[6]邵曰凤,赵庆,邹澄,等.三七原人参二醇型总皂苷的琼斯氧化 [J].中国民族民间医药,2009,18(17):33-34.
