α-MnO2纳米线的制备及其电化学性能研究
2011-07-25刘小军刘耀鹏闫晓前
刘小军,刘耀鹏,闫晓前
(陕西国防工业职业技术学院,陕西 西安 710302)
MnO2是一种常温下非常稳定的黑色或棕黑色粉末状固体,作为一种两性过渡金属氧化物主要存在于软锰矿中。MnO2性能独特,应用广泛[1],不同结构和形貌的MnO2纳米材料因其特殊的物理和化学性质,在离子筛、分子筛、催化材料、锂离子二次电池的正极材料和新型磁性材料等催化、电化学、吸附和磁性质等领域显示了广阔的应用前景[2~4]。
近年来,研究者运用水热法、溶剂热法、模板法和气相沉积法等技术制备了大量不同晶型和形貌的MnO2纳米材料。Yuan等[5]通过热分解Mn(NO3)2溶液合成了二维结构的六角星β-MnO2;Xi 等[6]通过高温煅烧γ-MnOOH纳米棒合成了β-MnO2纳米棒;Li 等[7]在低温条件下合成了α-MnO2空心刺猬球;Zhang等[8]在HCl 溶液中以不同方式处理层状氧化锰,制备了纳米四棱柱形貌β-MnO2纳米卷。迄今,人们对MnO2纳米材料的合成已进行了大量研究,但关于在酸性条件下制备α-MnO2纳米线研究较少。为此,作者以KMnO4为锰源,采用水热反应在HCl溶液中成功制备了α-MnO2纳米线,并对其电化学性质进行了初步探索。
1 实验
1.1 α-MnO2纳米线的制备
称取不同质量(按浓度计算)的KMnO4固体于50 mL 聚四氟乙烯内衬高压釜中,加入40 mL 0.5 mol·L-1的HCl溶液,室温搅拌数分钟至溶液为紫红色。旋紧釜盖,置于240℃均相反应器中反应24 h。反应结束后,取出反应釜,自然冷却至室温,打开釜盖后过滤溶液,所得产物以去离子水洗涤数次,并于50℃空气干燥12 h,获得α-MnO2纳米线。
1.2 α-MnO2纳米线结构表征
采用日本 Rigalcu D/Max-3c+/PC 型粉末衍射仪对样品进行XRD测试,Cu 靶κα线,电压35 kV,电流40 mA,扫描速度8°·min-1,扫描范围 (2θ) 3°~70°;采用荷兰 Philips-FEI公司Quanta 200型环境扫描电镜(SEM)观察样品形貌。
1.3 α-MnO2纳米线的电化学性能测试
按一定比例称取α-MnO2纳米线、石墨、乙炔黑,混合均匀,加5%(质量分数)的聚氟乙烯(60%),调成糊状;将上述物质均匀涂在泡沫镍上,80℃干燥后,在15 MPa 下压1 min,制得工作电极,然后组装成扣式电池。用蓝电电池测试系统(CT2001A)在1.0 mol·L-1LiPF6的EC (碳酸乙烯酯)+DEC (碳酸二乙酯)(体积比为1∶1)溶液中研究α-MnO2纳米线恒电流充放电行为。
2 结果与讨论
2.1 水热反应时间对产物晶型和形貌的影响
图1是水热反应不同时间所得产物的XRD图。
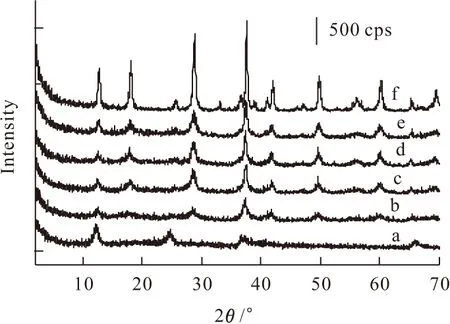
水热反应时间(h),a~f:1,5,9,12,24,48
从图1可以看出,当水热反应时间为1 h时,所得产物为典型的层状氧化锰(图1a);随着水热反应时间的延长,产物的晶型逐渐发生变化,当水热反应时间为5 h时,产物开始向隧道型氧化锰转变(图1b),是一个过渡阶段[9];当水热反应时间延长至9 h时,产物已完全转化为隧道型氧化锰(图1c);继续延长水热反应时间,产物晶型不再发生变化,只是结晶度在不断提高(图1d、1e);当水热反应时间为48 h时,晶型最好(图1f),晶体生长得更加规则。
图2是水热反应不同时间所得产物的SEM图。

水热反应时间(h),a~f:1,5,9,12,24,48
从图2可以看出,水热反应时间对产物形貌有很重要的影响。当水热反应时间为1 h时,产物呈棉团状,且相互交联(图2a),这是层状氧化锰的典型形貌,与XRD结果一致;当水热反应时间延长至5 h时,球状棉团形貌开始破坏,呈分散趋势(图2b);当水热反应时间为9 h时,棉团状形貌已被严重破坏,呈现疏松的状态(图2c);继续延长水热反应时间至12 h时,纳米线形貌已基本形成(图2d);当水热反应时间为24 h时,大部分纳米线已经形成(图2e);继续延长水热反应时间至48 h,得到了舒展均匀的纳米线(图2f)。
2.2 水热反应温度对产物晶型和形貌的影响
图3是不同温度下水热反应24 h所得产物的XRD图。
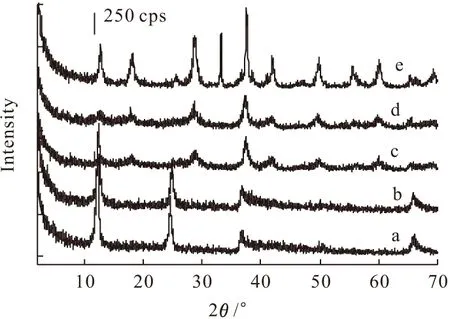
水热反应温度(℃),a~e:150,180,200,220,240
从图3可以看出,水热反应温度低于180℃,所制备产物的晶型为K+-birnessite层状结构(图3a);随着水热反应温度的升高,产物晶型开始向隧道型氧化锰转变(图3b);200℃和220℃是层状结构向隧道型氧化锰转变的一个中间过程(图3c、3d);当水热反应温度升高至240℃时,产物已完全转变为隧道型氧化锰,且产物的结晶度也不断提高(图3e)[10]。
图4是不同温度下水热反应24 h所得产物的SEM图。

水热反应温度(℃),a~e:150,180,200,220,240
从图4可以看出,水热反应温度对产物形貌有着重要的影响。随着水热反应温度的升高,所得产物由棉团状(图4a,4b)逐渐转变为舒展的纳米线(图4e)。
2.3 α-MnO2纳米线的充放电和循环放电曲线
图5为α-MnO2纳米线在1.5~4.5 V、20 mA·g-1电流密度下的第二次充放电曲线。
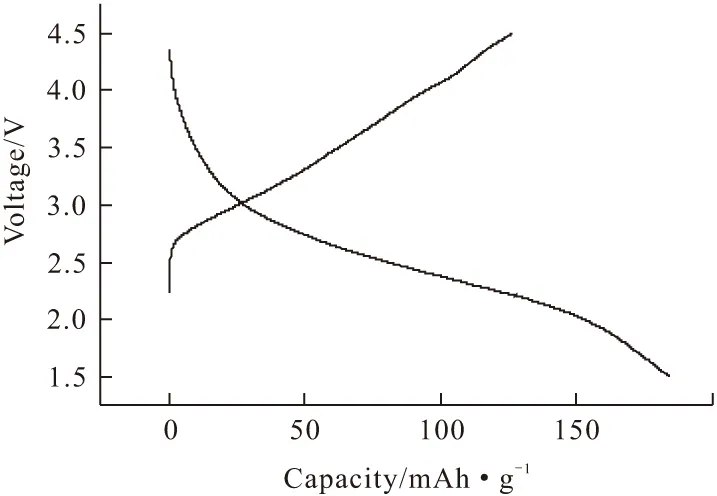
图5 α-MnO2纳米线在20 mA·g-1电流密度下的第二次充放电曲线
从图5可以看出,α-MnO2纳米线第二次放电的电容量为184.5 mAh·g-1,表明其具有较高的比容量和较好的充放电性能。
图6为α-MnO2纳米线的循环放电曲线。

图6 α-MnO2纳米线在20 mA·g-1电流密度下的循环放电曲线
从图6可以看出,起始放电容量接近200 mAh·g-1。循环30次后,α-MnO2纳米线的放电容量衰减到160.7 mAh·g-1,容量保持率为87.1%,即循环30次以内,α-MnO2的稳定性较好;循环50次后,放电容量衰减到112.3 mAh·g-1,容量保持率仅为60.9%,这说明循环次数多时,α-MnO2的稳定性下降。因此,α-MnO2纳米线的电化学循环性能有待进一步提高。
3 结论
以KMnO4为锰源,采用水热反应在HCl溶液中制备α-MnO2纳米线,通过控制水热反应时间、水热反应温度能很好地控制材料的结构及形貌,最佳水热反应时间为24 h、最佳水热反应温度为240℃。α-MnO2纳米线具有良好的电化学性能,在1.5~4.5 V、20 mA·g-1电流密度下其第二次放电的电容量为184.5 mAh·g-1。
[1] Wang X,Li Y D.Selected-control hydrothermal synthesis ofα-andβ-MnO2single crystal nanowires[J].J Am Chem Soc,2002,124(12):2880-2881.
[2] 李素梅,朱琦,尚屹,等.纳米二氧化锰制备及在环境治理方面应用的研究进展[J].环境保护,2009,(4):75-77.
[3] 陈冬梅,杨华.液相法制备纳米二氧化锰[J].贵州大学学报(自然科学版),2009,26(4):20-23.
[4] Wang Y H,Liu H,Sun X L,et al.Manganese dioxide-carbon nanotube nanocomposites for electrodes of electrochemical supercapacitors[J].Scripta Materialia,2009,61(11):1079-1082.
[5] Yuan J Q,Liu Z H,Qiao S F,et al.Fabrication of MnO2-pillared layered manganese oxide through an exfoliation/reassembling and oxidation process[J].J Power Sources,2009,189(2):1278-1283.
[6] Xi G C,Peng Y Y,Zhu Y C,et al.Preparation ofβ-MnO2nanorods through aγ-MnOOH precursor route[J].Mater Res Bull,2004,39(11):1641-1648.
[7] Li B,Rong G,Xie Y,et al.Low-temperature synthesis ofα-MnO2hollow urchins and their application in rechargeable Li+batteries[J].Inorg Chem,2006,45(16):6404-6410.
[8] Zhang L C,Liu Z H,Tang X H,et al.Synthesis and characterization ofβ-MnO2single crystals with novel tetragonous morphology[J].Mater Res Bull,2007,42(8):1432-1439.
[9] Zhang L C,Liu Z H,Lv H,et al.Shape-controllable synthesis and electrochemical properties of nanostructured manganese oxides[J].J Phys Chem C,2007,111(24):8418-8423.
[10] Jaisi Deb P,Dong H L,Plymale A E,et al.Reduction and long-term immobilization of technetium by Fe(Ⅱ) associated with clay mineral nontronite[J].Chemical Geology,2009,264(1-4):127-138.
