ACL TOP 全自动血凝仪抗干扰能力评价
2011-05-30陆学军张将
陆学军,张将
1.卫生部北京医院 检验科,北京100730;2.中南大学湘雅医学院 检验系,湖南 长沙 410013
0 前言
1 材料和方法
全自动血凝仪已广泛应用于临床,具有高效、准确、简便的优点,为手术前检查、血栓与止血疾病诊治、预后分析提供了较可靠的实验指标,且较大地提高了工作效率[16,22]。但在日常工作中,我们会遇到外观异常的标本,如溶血、脂血、黄疸标本,这些异常会干扰检测,对检验结果造成一定的影响。为此,本实验用干扰物对我科引进的Beckman-Coulter ACL-TOP血凝仪抗干扰能力进行评价。
1.1 材料
1.1.1 仪器
美国Beckman Coulter公司ACL TOP全自动血凝分析仪,Sysmex xs-800i全自动血细胞分析仪,日本奥林巴斯公司AU5400生化分析仪。
1.1.2 试剂
美国Beckman Coulter公司提供。① 凝血酶原时间测定试剂PT-FIB(批号0020003000);部分凝血活酶时间APTT及Cacl2(批号0020006800);③ 凝血酶时间TT(批号 0008469110)。
1.1.3 血浆
收集40名体检健康人抗凝静脉血各5mL,3000r/min离心10min,40份血浆等量混合后作为试验血浆。正常值质控血浆(批号0020003110)和通用定标血浆(批号0020003700)由Beckman Coulter公司原装进口。
1.1.4 干扰物
① 脂血:脂肪乳(主要成分为甘油三酯,华瑞制药有限公司生产,批号:0510019),经已校准过的AU5400生化分析仪测定;② 黄疸:胆红素标准品(上海科华公司生产,批号:GF62K),以总胆红素含量表示,经已校准过的AU5400生化分析仪测定;③ 血红蛋白:洗绦压积红细胞用蒸馏水稀释,离心去除细胞碎片,保留血红蛋白层,经已校准过的xs-800i血细胞分析仪测定。
1.2 方法
1.2.1 精密度试验
从混合好的体检健康人试验血浆中取20份(每份500μL),于4h内在ACL TOP 血凝仪上参照仪器操作SOP文件测定PT、APTT、TT、FIB[1-4],观察其批内精密度;采用当月工作日内正常值质控血浆质控数据作日间精密度试验结果。
1.2.2 准确性试验
取l份定标(靶值)血浆重复测定5次。取平均值即为测定值。
1.2.3 干扰性试验
根据美国国家临床检验标准化委员会制定的“临床化学干扰试验”指南的要求,采取在体外添加干扰物于正常血浆中的方法制备待测标本[5-6,31]。为减少基质效应,3种干扰物分别用体检健康人混合血浆配置(见表4)。终浓度分别为甘油三酯(TG)0~10.86mmol/L;总胆红素(TBIL)0~416μmol/L;血红蛋白(Hb)0~7.1g/L。在ACL TOP 血凝仪上测定PT、FIB、TT、APTT各2次,取平均值。记录加入前后测定值的变化,以未加干扰物的混合血浆测定值为标准,计算出影响度,以影响度作为评价指标。影响度=[(加干扰物混合血浆测定值-未加干扰物混合血浆测定值)/未加干扰物混合血浆测定值]×100 %[12,33]。
1.2.4 测定方法
凝固(浊度)法测定;发色(吸光度)法测定;免疫学测定。
1.3 统计学分析
定标血浆与靶值比较采用单样本t检验(SPSS 10.0统计软件处理)。
2 结果
2.1 精密度试验
测定PT、APTT、TT、FIB,结果见表l~2。(x±s)的批内精密度CV<4.0%,日间精密度CV <4.0%。

表1 PT、APTT、TT、FIB批内重复性试验结果(x±s)
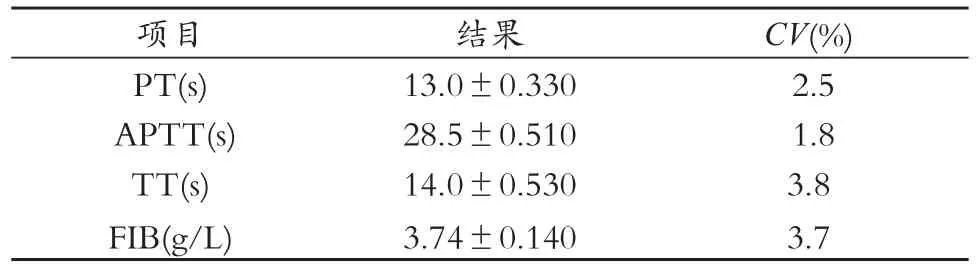
表2 PT、APTT、TT、FIB日间精密度试验结果(x±s)
2.2 准确性试验
测定标血浆5次,测定值与靶值差异无统计学意义(p>0.05),见表 3。
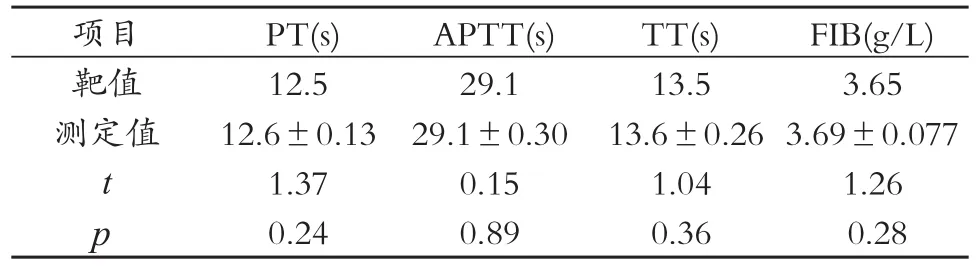
表3 PT、APTT、TT、FIB准确性试验结果(x±s)
2.3 干扰性试验
ACL TOP测定加入各类不同浓度干扰物的试验血浆PT、APTT、TT、FIB结果,与干扰物对照浓度(%)对比,HB、TBIL为干扰物时测得PT、APTT、TT、FIB的影响范围在±8%之内。TG为干扰物时测得TT、FIB的影响范围在±6%之内。TG在0~4.34mmol/L时,PT影响度为0~-13.5%;TG在6.52~10.86mmol/L时,PT影响度为-16.2%~-18.9%。TG在0~2.17mmol/L时,APTT影响度为0~-10.4%;TG在4.34~10.86mmol/L时,APTT影响度为-16.5%~-26.3%。详见表4~7。
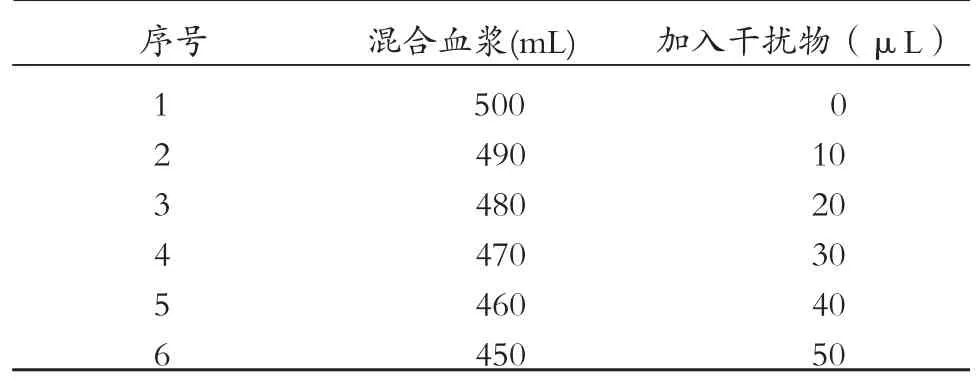
表4 各浓度干扰物混合血浆待测物配制法
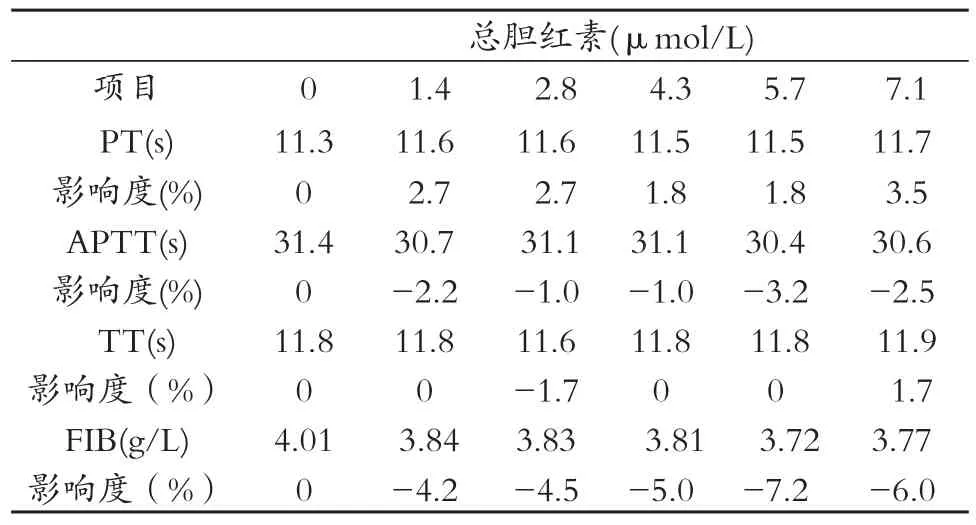
表5 不同浓度血红蛋白(Hb)对ACL TOP血凝仪测定结果的影响
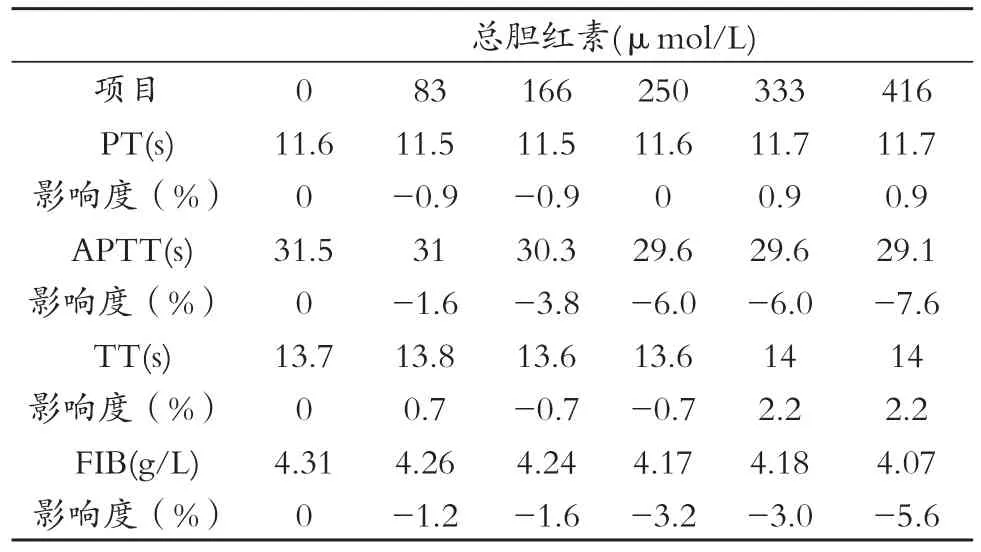
表6 不同浓度总胆红素(TBIL)对ACL TOP血凝仪测定结果的影响
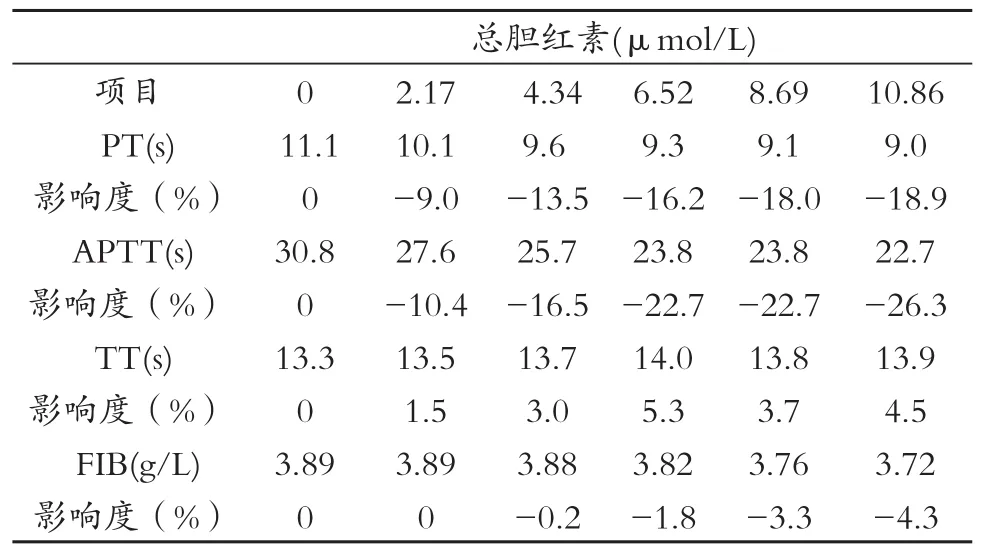
表7 不同浓度甘油三酯(TG)对ACL TOP血凝仪测定结果的影响
3 讨论
PT、APTT、TT和FIB是临床凝血功能判断的常规测定项目;是外科手术前凝血功能异常筛查的必查项目;是血栓前状态的检查、弥漫性血管内凝血出血疾病(DIC)的实验诊断,以及对各种抗凝治疗者的用药指导和预后估计等的诊断项目,在临床疾病诊疗中具有重要的价值[2,4,33]。目前市场已有多种凝血仪和试剂盒提供,使凝血功能检测简便、快速、实用,在临床得到广泛应用。当代最先进的血液凝固分析仪,能同时应用不同的实验原理,对大量的标本进行多项指标的检测;同时,仪器对标本和试剂的需求量比手工方法用量几乎少一半,大大地降低了检测的成本[7-8,12]。ACL TOP 血凝分析仪是一个可随时加入标本进行检测且专为血栓实验室用于体外诊断而设计的平台式全自动分析仪。它不仅具有高度自动化、快速检测和操控界面先进的特点,还可同时采用凝固法、免疫比浊法和发色底物法检测20多个凝血相关指标。检测能力可达到360个PT测试/h或320个APTT测试/h或330个PT/APTT组合测试/h(165个APTT和165个PT测试)。它的高效率、大样本分析能力,可为临床提供凝血、抗凝、纤溶系统各项指标的分析检测。可用于出血与血栓性疾病的诊断、抗凝药剂量监测及预后分析[1,3,9,10]。
ACL TOP血凝仪使用于正常外观血浆标本,测定PT、APTT、TT和FIB时变异系数都<4%,效果较理想。但在实际工作中会经常涉及到异常外观血浆标本,如血浆中深浅不一的溶血和黄疸色泽、食糜含脂类或蛋白引起的混浊等干扰物质的物理性质影响血凝仪对血液凝固终点的判别,对测定方法起干扰效应[13-14]。为此,本人做了干扰性试验,采用日本临床化学学会的日本工业规格(Japanse industrialstandard,JIS)制定的“干扰物质的影响测试法”,并借鉴国际临床化学委员会(IFCC)的“临床化学中药剂的影响”的方法和美国国立临床检验标准化委员会(National Committee for Clinical Lab—Oratory Standard,NCCLS)制定的“临床化学中干扰性测试指南”的检测方法。试验采取体外干扰物质影响试验—添加试验法。添加干扰物的最高浓度包括引起干扰影响物质的最高浓度。我们选用干扰物最终浓度为:Hb7.1g/L;TG10.86mmol/L;TBIL416μmol/L。为了在添加干扰物后使原试验血浆的基质变化保持在最小限度,最好使添加干扰物的量与原试验血浆相比保持在最低。IFCC认为,添加干扰物溶液量:原实验血浆量为1:9 ;NCCLS则认为1:20 ;日本临床化学学会则为1:9 ;本人采用1:9,各干扰物原始浓度为测试浓度的10倍。原试验血浆9份加1份生理盐水作为0干扰浓度,制成包括0浓度在内的6个不同梯度的添加干扰物质浓度,进行同步测定,实验结果以测定秒值或mg/L值及影响度(%)评价[5-6,11,31]。为了排除含不同浓度的干扰物对原试验血浆各项结果的影响,我们采用的干扰物为血清,而不是血浆。因血清中不含FIB,经检测PT、APTT均延长超出检测范围,可认为不含凝血因子,而0干扰血浆加等量的生理盐水。ACL TOP血凝分析仪采用先进光电散射光法同时配合本底扫描及免疫浊度测定原理,根据待检样品在凝固过程中散射光的变化并扣去原始血浆标本中原有色泽或浊度的百分比法来确定凝固终点的检测方法,血浆同试剂快速离心混匀,在混合的瞬间,散射光最弱,从有散射光变化时将散射光强度置为0;随着血浆纤维蛋白原转变成纤维蛋白,标本散射光强度也逐渐增加,当标本凝固完全以后,散射光的强度就稳定下来,此时散射光最强,光变化完全停止时将散射光强度确定为100[15-16,18]。如血浆含色泽或浊度时,其0的基线点会自动抬高;遇低纤维蛋白原血症,则0的基线点会自动降低[3,9,17]。
试验结果表明,ACL TOP血凝分析仪精密度较理想,批内和日间PT、APTT、TT、FIB的CV均<4.0%,具有良好的重复性和稳定性,满足实验室检测要求,避免了手工操作所造成的误差和不可靠性。血浆测定值与靶值相比较,差异无统计学意义(p>0.05),表明仪器测定的准确性良好。
对于干扰性试验: ① 干扰物为Hb时,测定PT、APTT、 TT影响度在±3.5%之内,FIB影响度为0~-7.2%,远小于美国CLIA'88提出的常见血凝仪分析指标质量要求(PT、APTT:靶值±15 % ;FIB:靶值±25 %)的标准[27-28]。② 干扰物为TBIL时,测定PT、TT、FIB影响度在±6%之内,APTT影响度为0~-7.6%,也较为理想。由①、②得知ACL TOP 血凝仪对溶血、黄疸标本有很强的抗干扰能力。③ 干扰物为TG时,测得TT、FIB的影响范围在±6%之内。TG在0~4.34mmol/L时,PT影响度为0~-13.5%;TG在6.52~10.86mmol/L时,PT影响度为-16.2%~-18.9%,超出美国CLIA'88质量要求(PT:靶值±15 %)标准的范围。TG在0~2.17mmol/L时,APTT影响度为0~-10.4%;TG在4.34~10.86mmol/L时,APTT影响度为-16.5%~-26.3%,超出美国CLIA'88质量要求(APTT:靶值±15 %)标准的范围。由③得知TG对TT、FIB无干扰,而高浓度的TG干扰PT、APTT的检测, PT、APTT随TG浓度的升高愈加降低,影响度愈大。关于各检测项目的干扰情况:TBIL对PT影响度(±0.9%)最小,Hb对APTT、TT影响度(前者为0~-3.2%,后者为±1.7%)最小,TG对FIB影响度(0~-4.3%)最小。
从测定结果可以看出,高脂肪乳糜对ACL TOP血凝分析仪测定PT、APTT的结果有明显的影响,可使PT、APTT测定结果偏低,导致影响度增大且呈非规则的递增性波动,对测定方法起干扰效应。这是由于:① 脂肪乳糜使血浆浊度过高,干扰测定过程,超过仪器检测范围时,导致仪器判定终点发生偏差不能检测出结果或检验数据不准确。②本试验主要测试的是对ACL TOP试剂的干扰,ACL TOP血凝分析仪配套试剂一个显著的改变就是PT 、APTT试剂中的磷脂由人工合成, PT试剂中的组织因子采用基因工程重组技术制备[1,10,17],推测TG可能会影响其中某些成分干扰测定[19-22]。常温下采用高速离心(13000r/min,离心10 min)去除脂肪乳糜对血浆中凝血因子活性无影响。因此,常温高速离心是一种简便、易行的消除高脂肪乳糜对血凝分析仪测定结果的影响的方法[24,26,32]。另外,为减少脂血干扰误差,对于抗凝药物治疗监测APTT的患者应空腹或固定的时间采集标本[25,30]。
综上所述,ACL TOP 血凝仪对溶血、黄疸标本有很强的抗干扰能力。含低浓度TG(300μmol/L以下)的乳糜标本,对测定的影响度小,属于在正常范围内波动;但含有较高或高浓度TG的乳糜标本,对PT、APTT测定过程和结果的影响度较大,反映ACL TOP在一定浓度范围内具有良好的抗乳糜干扰能力。这一结果不但给临床医生对病人的治疗、判断及预后提供了有效的血液凝固指标,而且为设定新的止血和血栓指标奠定了基础[29]。
[1]Appert A,Fischer F,Jambou D,et al.Evaluation and performance characteristics of the automated coagulation analyzer ACL TOP[J].Thrombosis,2007,120:733-743.
[2]Dorn A,Dempfle C,Bertsch T,et al.Evaluation of the automated coagulation analyzer Sysmex CA-7000[J].Thrombosis,2005,116:171-179.
[3]Eschwege V,Catillon C,Robert A.Evaluation of the automated coagulation analyzer ACL TOP[J].Annales de Biologie Clinique,2006,64:259-264.
[4]Flanders M,Crist R,Safapour S,et al.Evaluation and performance characteristics of the STA-R coagulation analyzer [J].Clinical Chemistry, 2002,48:1622-1624.
[5]National Committee for Clinical Laboratory Standards.One-Stage Prothrombin Time (PT)Test and Activated Partial Thromboplastin Time (APTT)Test;Approved Guideline[S].NCCLS Document H47-A(ISBN 1-56238-301-9).Wayne,PA:NCCLS,1996.
[6]National Committee for Clinical Laboratory Standards.Procedure for the Determination of Fibrinogen in Plasma;Approved Guideline- Second Edition[S].NCCLS Document H30-A2(ISBN 1-56238-439-2).Wayne,PA: NCCLS,2001.
[7]Walenga JM,Fareed J.Automation and quality control in the coagulation laboratory[J].Clin Lab Med,1994,14:709-728.
[8]Fischer F,Appert A,Jambou D,et al.Evaluation of the automated coagulation analyzer Sysmex® CA 7000[J].Thromb Res,2006,117:721-729.
[9]Barnes PW,Eby CS.An evaluation of the performance characteristics of the ACL TOP® coagulation system[J].Clin Chem,2004;50(S6):A184.
[10]Ho DK,Lollo M,Reyes M,Garvey MB.A preliminary experience with the ACL TOP Hemostasis Testing System[J].Presentation at the ISLH XVIIIth International Symposium,San Francisco,CA,USA,May 2005.
[11]Clinical and Laboratory Standards Institute(formly National Committee for Clinical Laboratory Standards)[J].A framework for NCCLS evaluation protocols:A report.NCCLS document EP19-R.Wayne,PA:NCCLS,2002.
[12]程大卫,李敏霞,张威,等.CA 1500 型血液凝固分析仪的抗干扰功能[J]. 中华医学检测杂志,1999,22(5):309-311.
[13]Barnes PW,Eby CS.An evaluation of the performance characteristics of the ACL TOP Hemostasis Testing System.presentation at the AACC Meeting[M].Los Angeles,CA,USA,July 2004.
[14]Ziems J,Schulte M,Demant T.Clinical evaluation of the ACL TOP Hemostasis Testing System.Presentation at the 49th Congress of the German Society for Thrombosis and Hemostasis Research[J].February 2005,Mannheim,Germany.
[15]郝建华,吕斌斌,高旭红,等.Stago Compact型血液凝固分析仪的抗干扰功能[J].国外医学临床生物化学与检验学分册,2002; 23(3):185-186.
[16]黄彬,陈茶,钟武平.Sysmex CA 6000全自动血凝仪实验性能评价[J].临床检验杂志(特刊),2003,21:82-83.
[17]Milos M,Herak D,Kuric L,et al.Evaluation and performance characteristics of the coagulation system:ACL TOP analyzer-HemosIL reagents[J].Lab Hematol,2009,31(1):26-35.
[18]Curtin N,Highe G,Harris M,et al.Extensive evaluation of the insrumentation laboratory IL test D-Dimer immunoturbidimetric assay on the ACL 9000 determines the D-Dimer cutoff value for reliable exclusion of venous thromboembolism[J].Lab Hematol,2004,10(2):88-94.
[19]Quehenberger P,Kapiotis S,Handler S,et al.Evaluation of the automated coagulation analyzer SYSMEX CA 6000[J].Thromb Res,1999,96(1):65-71.
[20]Wehrum MJ,Hines JF,Hayes EB,et al.Comparative assessment of hypercoagulability in women with and without gynecologic malignancies using the thromboelastograph coagulation analyzer[J].Blood Coagul Fibrinolysis,2010,21(2):140-143.
[21]Nam MH,Roh KH,Pak HN,et al.Evaluation of the Roche CoaguChek XS handheld coagulation analyzer in a cardiac outpatient clinic[J].Ann Clin Lab Sci,2008,38(1):37-40.
[22]施金俏.ACL 200 型血凝仪抗干扰能力探讨[J].上海医学检验杂志,2000,15(4):242.
[23]彭黎明,陆小军.自动血凝仪的选型与评价[J].上海医学检验杂志,2002,17(1):58.
[24]王春新,谢国强.ACL 200血凝仪的应用评价[J].国外医学临床生物化学与检验学分册,2005,26(3):189.
[25]陈丽,曹海芬.ACL 6000 全自动血凝仪的使用评价[J].江西检验医学,2002;20(3):181-182.
[26]马永能,张鹏,潘淑,等.ACL 8000型凝血分析仪的抗干扰功能[J].现代检验医学杂志,2007;22(4):46-48.
[27]National Committee for Clinical Laboratory Standards.Interference Testing in Clinical Chemistry; Approved Guideline [S].NCCLS document EP7- A [ ISBN 1-56238-480 -5 ].NCCLS.940 West Valley Road,Suite 1400,Wayne,Pennsylvania 19087 -1898,USA,2002.
[28]National Committee for Clinical Laboratory Standards.Evaluation of Precision Performance of Quantitative Measurement Methods;Approved Guideline-Second Edition[S].940 West Valley Road,Suite 1400,Wayne,Pennsylvania 19087-1898,USA,2004.
[29]唐宁,曹文静,夏汛生,等.ACL TOP 全自动血凝分析系统的性能评价[J].医疗设备信息,2007,22(2):48-51.
[30]郑卫东,范小斌,唐红艳.STA-R全自动血凝仪性能评价[J].实用医学杂志,2005,21(5):533-534.
[31]National Committee for Clinical Laboratory Standards.Interference Testing in Clinical Chemistry .Proposed Guideline[D].EP7.Pennsylvania:NCCLS,1986,6:332-335.
[32]崔冬生,耿玉兰,贺信祥,等.临床乳糜血对凝血检测项目的影响及处理[J].中国血液流变学杂志,2003,13(1):40-41.
[33]熊立凡,等.Sysmex CA1500 血液凝固仪的评价[J].中华医学检验杂志,1999,22(6):383-384.
