中兽药散剂中非法添加利巴韦林的检测方法研究
2011-05-29崔成富陈创华林海丹黄宝珠邓国东
崔成富,陈创华,林海丹,黄宝珠,邓国东
(广东省兽药与饲料监察总所,广州 510230)
利巴韦林(Ribavirin),又称病毒唑或三氮唑核苷,为广谱抗病毒药物,对多种病毒有抑制作用。该药曾在畜牧业和水产养殖业广泛应用,用于预防和治疗病毒性疾病。但其作为人用抗病毒药移植兽用,缺乏科学规范、安全有效实验数据;用于动物病毒性疫病不但给动物疫病控制带来不良后果,而且影响国家动物疫病防控政策的实施[1];不规范使用可导致动物中毒[2],在动物性食品中的残留对人体具有潜在危害,可引起变态反应和造血系统功能障碍[3],因此农业部公告第560号已规定取消其在动物疾病预防控制上的使用。但目前仍有部分兽药生产企业为了提高某些中兽药散剂的所谓抗病毒疗效,在中兽药散剂中非法添加了利巴韦林,致使饲养户在不知情的情况下使用了这些产品,从而容易导致药物在动物源性食品中残留,严重影响动物产品的质量安全,进而危害人体健康。目前我国尚无中兽药散剂中利巴韦林的检测方法,对此类违法行为缺乏有效的监测手段。本研究在对中兽药散剂中利巴韦林显微特征进行观察的基础上,建立一种简便、灵敏、准确的高效液相色谱法,对中兽药散剂中非法添加的利巴韦林进行定性定量测定。
1 材料与方法
1.1 仪器与设备 卡尔·蔡司显微镜:Standard25ICS;高效液相色谱仪:Aglient 1200型,配二极管阵列检测器,美国 Aglient公司;电子天平:CPA225D型,德国 Sartorius公司;制超纯水机:F3PN33491型,美国Millipore公司。
1.2 药品与试剂
1.2.1 对照品 利巴韦林对照品,批号629-200202,含量100.0%,由中国药品生物制品检定所提供。
1.2.2 供试品
1.2.2.1 阴性对照散剂 清瘟败毒散:广州绿州生物技术有限公司;苍术香连散:广州市和生堂动物药业有限公司。以上两种中兽药散剂经检测均不含利巴韦林。
1.2.2.2 阳性添加散剂 分别按照0.05%、0.1%和0.2%的比例在阴性对照散剂中添加利巴韦林对照品,混匀。
1.2.2.3 试剂 甘油,超纯水。
1.2.2.4 标准储备液配制(2.5 mg/mL)精密称取利巴韦林对照品125 mg于50 mL量瓶中,用超纯水溶解并稀释至刻度,摇匀,制成浓度为2.5 mg/mL标准储备液。
1.3 测定方法
1.3.1 显微检查法 取利巴韦林对照品、两种中兽药散剂的阴性样品以及阳性添加样品少许,置载玻片上,滴加甘油2~3滴,搅匀,封片,置显微镜下观察。利巴韦林的显微特征为无色或淡黄绿色结晶,呈棒形或一端或两端呈梭形,长短不一,表面有纵裂纹或裂缝纹。
1.3.2 高效液相色谱法
1.3.2.1 色谱条件 色谱柱为 Ultimate XB-C18(150 mm ×4.6 mm,5μm),流动相为超纯水,检测波长207 nm,流速1.0 mL/min,进样量10 μL,柱温25℃。
1.3.2.2 样品测定 精密称取中兽药散剂约2.5 g,置具塞锥形瓶中,精密加入50 mL超纯水摇匀,超声15 min,静置,滤过,取续滤液10 μL,注入液相色谱仪,记录色谱图。
1.3.2.3 标准曲线绘制 精密量取标准储备液,用超纯水分别稀释为 1、5、25、50、100、150 μg/mL浓度的系列标准溶液,取10 μL注入液相色谱仪,记录色谱图。
2 结果
2.1 显微图 按1.3.1项方法,对利巴韦林对照品、两种中兽药散剂的阴性样品以及阳性添加样品进行观察。显微图谱如图1所示。
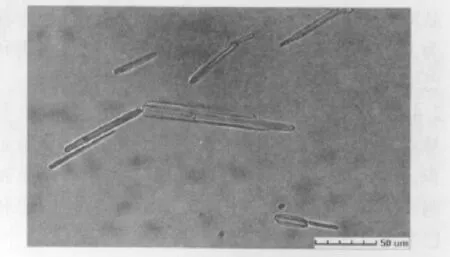
图1 利巴韦林对照品显微图谱
2.2 色谱图 在1.3.2.1项的色谱条件下,对利巴韦林对照品溶液、两种中兽药散剂的阴性样品溶液以及阳性添加样品溶液采用峰面积法进行测定。利巴韦林与样品中其他成分能够很好地分离,利巴韦林的保留时间约为5.9 min,其峰形良好。利巴韦林对照品溶液光谱及色谱图、两种中兽药散剂的阴性样品溶液及阳性样品溶液色谱图如图2~图4所示。

图2 利巴韦林对照品溶液(50 μg/mL)光谱图和色谱图
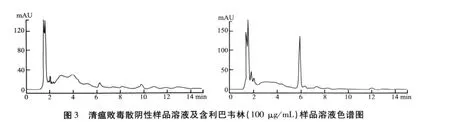

2.3 标准曲线 以利巴韦林色谱峰面积Y与对照品溶液浓度C(μg/mL)作线性回归,得到线性方程为 Y=26.058C+0.5228(r=1.00000),结果表明利巴韦林在1~150 μg/mL范围内呈良好线性关系。
2.4 精密度试验 取每1 mL含50 μg的利巴韦林对照品溶液重复进样6次,每次10 μL,记录峰面积,计算变异系数RSD,结果如表1所示。结果表明6次重复进样的RSD为0.02%,外标法测定利巴韦林具有良好的重现性。

表1 连续进样精密度试验结果(n=6)
2.5 最低检测限 在上述色谱条件下,将利巴韦林对照品溶液加入阴性散剂中,并逐步减少对照品溶液的量,按1.3.2.2制备进样,以信噪比的3倍为最低检出限,测得苍术香连散的最低检出浓度为0.1 μg/mL,最低检测限为 2 mg/kg;清瘟败毒散的最低检出浓度为0.05 μg/mL,最低检测限为 1 mg/kg。
2.6 重复性试验 精密称取已添加利巴韦林的苍术香连散与清瘟败毒散(0.1%添加量)各6份,按1.3.2.2项方法测定,计算利巴韦林的含量,考察方法重复性。结果表明方法重复性良好,其RSD分别为 1.04%和 1.32%。
2.7 稳定性试验 取上述2.6项下制备的供试液,分别于0、2、4、6、8、12、24 h 进样测定,记录色谱峰面积。结果表明样品溶液在24 h稳定性良好。
2.8 回收率 取上述两种中兽药的散剂按表2添加不同浓度的利巴韦林制成阳性散剂,按照1.3.2.2项方法测定,计算回收率及其变异系数。每个散剂的每个添加浓度进行6次重复测定。结果如表2所示。结果显示,两种中兽药散剂的添加平均回收率在91.74% ~98.50%之间,变异系数在0.08% ~0.58%之间。考虑到中药散剂成分的复杂性,测试数据表明该方法回收率较好,准确度高。

表2 中兽药散剂中利巴韦林添加回收率及其变异系数
3 讨论
3.1 中兽药散剂种类的选择 清瘟败毒散具有泻火解毒、凉血功效,主治热毒发斑、高热神昏。苍术香连散具有清热燥湿的功效,主治肠黄、下痢、湿热泄泻。这两种散剂均有一定的预防和治疗肠道感染的作用。利巴韦林因对DNA和RNA病毒均有效,对肠病毒等引起的感染有显著疗效,故在畜禽养殖中极有可能被非法添加到上述两种中兽药散剂中,用于治疗和预防肠道感染。因此本研究选取了清瘟败毒散和苍术香连散作为检测的对象。
3.2 快速筛选方法的建立 因液相法相对检测周期长,成本高,本方法首先使用显微检查方法对样本进行快速筛选。显微检查中若检出如图1中所示结晶物质,则表明可能非法添加利巴韦林;对阳性样品再利用高效液相色谱法,通过与对照品色谱图保留时间、光谱图的比对,可实现对两种中兽药散剂中的利巴韦林进行大批量的快速定性判定和定量测定。
3.3 显微试液的选择 对利巴韦林特征进行显微观察时,分别用水合氯醛、甘油醋酸、甘油乙醇和甘油试液进行了试验。结果表明用水合氯醛、甘油醋酸和甘油乙醇试液时,因利巴韦林溶于水、微溶于乙醇,在显微镜下观察不到利巴韦林的显微特征;而用甘油试液则可以很好地观察到其显微特征,选择甘油试液可以在显微镜下观察到中兽药散剂中添加0.05%的利巴韦林的显微特征。所以最终以甘油作为利巴韦林显微观察的试剂。
3.4 提取溶剂、流动相的选择 考虑到中兽药散剂中多种成分溶于有机溶剂,可能干扰利巴韦林的检测,而利巴韦林溶于水,故排除用有机溶剂作提取液,而采用超纯水作为提取溶剂[3]。通过调节超纯水的pH值(pH 6~8)实验,发现pH值对利巴韦林的出峰时间和峰形无明显影响,故用普通超纯水作流动相。
3.5 色谱柱的选择 在用超纯水作流动相[3]时,曾用Zorbax Eclipse XDB-C18(Aglient)为色谱柱,发现出峰时间比较短,与杂峰分离度不佳,且出峰保留时间不一致,重复性不好。改用亲水性色谱柱Ultimate XB-C18(Welch Materials)后,与杂峰分离较好,特别是保留时间重复性改善,故使用亲水性色谱柱Ultimate XB-C18(Welch Materials)来测定利巴韦林。
3.6 添加回收率试验浓度的选择 根据两种中药散剂在预防和治疗畜禽的用量及临床中利巴韦林的预防和治疗用量,选择在中兽药散剂中分别添加0.05%、0.1%和 0.2%利巴韦林作为阳性对照,测定其回收率及变异系数,可以更符合非法添加利巴韦林的实际情况。
4 结论
本文建立的显微检查初筛、再用高效液相色谱进行定性及定量的分析方法可快速、准确地鉴定和测定清瘟败毒散和苍术香连散两种中兽药散剂中违法添加的利巴韦林,对更好地控制产品质量具有一定的实用价值。
[1]杨春莲.一起猪利巴韦林中毒的诊治[J].黑龙江畜牧兽医,2010,5:94.
[2]张 俊,闫 炜,何振凤,等.利巴韦林不良反应综述[J].临床药物治疗杂志,2004,1:61 -62.
[3]国家药典委员会.中华人民共和国药典二○○○年版(二部)[M].北京:化学工业出版社,2000:302.
