乳腺癌保乳术后切线野照射与瘤床同步整合补量调强放射治疗的剂量学区别
2011-05-25李楠李光赵欣宇张硕夏兵王志宇
李楠,李光,赵欣宇,张硕,夏兵,王志宇
(中国医科大学1.附属第一医院放疗科,沈阳 110001;2.94期七年制临床医学专业,沈阳 110001)
近年来,调强放射治疗(intensity modulated radiation therapy,IMRT)技术被越来越多的应用于乳腺癌保乳术后放射治疗中,许多研究表明IMRT可以降低心、肺、对侧乳腺的受照射体积及剂量,并能够提高靶区内剂量分布均匀性。但以往国内外对IMRT如何进行瘤床补量研究的报道较少,而在早期浸润性乳腺癌的治疗中,瘤床补量有助于提高肿瘤的局部控制率[1]。本研究利用三维治疗计划系统比较保乳术后瘤床同步整合补量的调强放射治疗(simultaneous integrated boost intensity-modulated radiation therapy,SIB-IMRT)技术,与切线野照射后程电子束补量技术在靶区剂量学方面的差异,评估SIB-IMRT在乳腺癌保乳术后放射治疗中的意义。
1 材料与方法
1.1 病例选择
2007年3 月~2009年1月间中国医科大学附属第一医院放疗科收治的45例乳腺癌保乳术后患者。年龄42~68岁,中位年龄54岁。病理类型:导管内癌3例,浸润性导管癌39例,粘液腺癌3例。根据2002年AJCC(第6版)乳腺癌分期标准,Tis3例,T1 30例,T2 12例。肿瘤原发部位:24例患者位于左侧乳房,其中6例位于外上象限,6例位于内上象限,11例位于外下象限,1例位于内下象限;21例患者位于右侧,其中13例位于外上象限,2例位于外下象限,6例位于内上象限。所有病例均于术后一个月内1~2个周期化疗后开始放疗。
1.2 放射治疗定位和图像采集
患者仰卧位固定于乳腺托架及真空垫上,两臂180°上举,握住乳腺托架。体表用金属标记定位点、患侧乳腺范围及手术疤痕范围。平静呼吸状态下使用螺旋CT进行扫描,层厚5 mm,扫描范围包括双侧全肺和乳腺,上界包含锁骨上区,通过网络传输到ADACpinnacle3治疗计划系统。
1.3 临床靶区、计划靶区及危及器官的定义
将术后完整乳腺组织、胸肌间淋巴结和乳房下的胸壁淋巴引流区定义为低危临床靶区(CTV1),前界在皮肤表面下0.5 cm,后界包括腺体下胸壁;将瘤床区定义为高危临床靶区(CTV2),即CT扫描时所显示的银夹标记的瘤床范围,对于术中未行银夹标记瘤床区的患者,按术前肿瘤解剖位置、CT扫描显示的术后残腔及手术疤痕来确定CTV2。PTV1为CTV1在头脚方向、乳腺内侧向胸骨方向、外侧向腋窝方向各外放1 cm,胸壁内侧向肺方向外放0.5 cm,皮肤方向不进行外放获得;PTV2为CTV2在各方向外放1 cm获得。将同侧肺、对侧乳腺及左侧乳腺癌患者的心脏作为危及器官(OARs),勾画出对侧乳腺及心脏的外轮廓,利用系统软件自动生成双肺轮廓。
1.4 治疗计划的制定
利用ADAC公司pinnacle3治疗计划系统,进行切线野后程电子线补量治疗计划和逆向SIB-IMRT治疗计划的设计。在2种计划中,CTV1处方剂量为50 Gy,单次 2.0 Gy;CTV2 处方剂量为 60 Gy,单次剂量2.4 Gy。切线野治疗计划采用乳腺对穿切线野源皮距方式照射:旋转机架找到最合适的切线野入射角度,调整准直器角度,使PTV1在射野方向观上投射的体积最小,调整射野大小,使射野在PTV1上下及后方各扩大1 cm,前界在乳腺皮肤表面外再露空1.5 cm,外加15°楔形板,使靶区内剂量均匀,两射野中心点连线的中点定义为剂量参考点;后程电子线补量采用单野照射,机架角垂直于瘤床,使射线束通过乳腺的路径最小,射野中心轴与瘤床后界的交点定义为电子线补量的剂量参考点,根据病人瘤床深度选择9~12MeV电子线照射。SIB-IMRT计划设计采用非共面的三野等中心照射,转换后的子野数约30个。切线野计划中的两切线野及SIB-IMRT计划均使用Siemens Primus-M直线加速器的6MV-X线,SIB-IMRT采用MLC静态调强技术。
1.5 评估指标与统计学方法
分别在2种计划的剂量体积直方图上获得以下数据:(1)PTV1:95%处方剂量覆盖的靶区体积(V95%-PTV1),最大剂量(Dmax),最小剂量(Dmin)。(2)PTV2:95%处方剂量覆盖的靶区体积(V95%-PTV2)。(3)心脏(左乳癌患者):平均剂量(Dmean),最大剂量(Dmax),10%体积所受到照射的剂量D10。(4)同侧肺:平均剂量(Dmean),受到大于等于20Gy剂量的体积百分比V20。5)对侧乳腺:平均剂量(Dmean)。利用SPSS14.0统计软件对2种照射方法得出的数据进行配对t检验。
2 结果
2.1 PTV1、PTV2的剂量分布
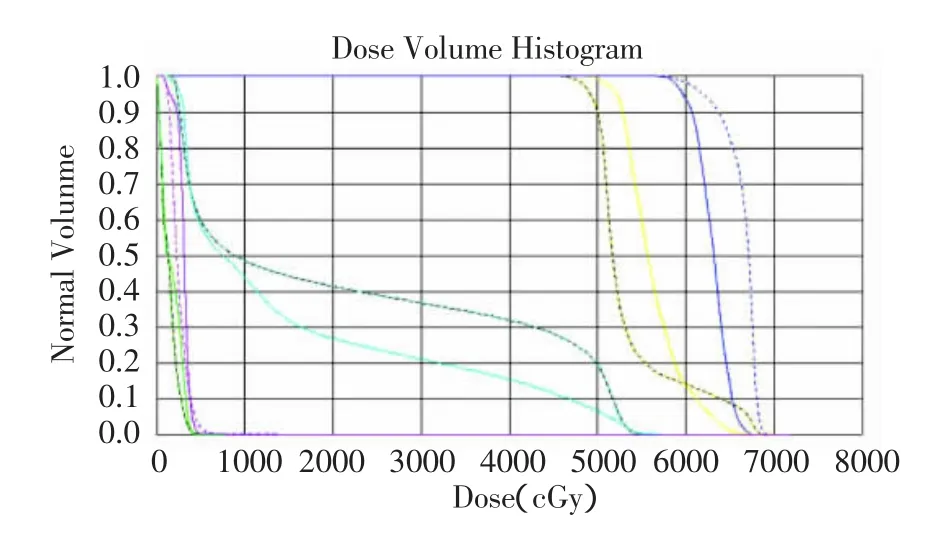
图1 切线野照射与SIB-IMRT计划DVH图比较Fig.1 Comparison of conventional wedged tangential plan and IMRTplan of DVH
在 2种计划中,PTV1、PTV2的靶区覆盖率V95%相似,无统计学差异(P>0.05),均达到了至少95%的处方剂量包绕95%靶体积的要求。SIB-IMRT计划中Dmax-PTV1平均剂量为7046.240 cGy,未明显高于切线野计划,且45例患者的最大剂量点均位于瘤床区内。Dmin-PTV1在2种计划中相似,无明显差异。见图1及表1。

表1 切线野照射与SIB-IMRT计划的PTV剂量学比较Tab.1 Comparison of conventional wedged tangential plan and IMRT plan of Dosimetry
2.2 OARs的剂量分布
与切线野计划相比,SIB-IMRT技术中左侧乳腺癌患者心脏Dmean减少了344cGy,10%体积所受到照射的剂量D10减少了1006cGy;同侧肺Dmean减少了461cGy,V20降低了21.5%;对侧乳腺Dmean减少了52.3 cGy。差异有统计学意义(P<0.05),见表2。

表2 切线野照射与IMRT的OARs剂量学比较Tab.2 Comparison of conventional wedged tangential plan and IMRT plan of OARs in Dosimetry
3 讨论
经过许多前瞻性和回顾性的研究结论证实,保乳治疗已经成为早期乳腺癌的一种标准治疗方式[2,3]。目前保乳术后放射治疗研究的热点在于如何降低放射治疗相关并发症,特别是如何改善全乳靶区剂量分布的不均匀性,和降低心脏、肺、软组织及对侧乳腺等重要器官和组织的受照射剂量。剂量学研究结果显示,在靶区覆盖率(V95%)相似的前提下,IMRT技术无论是在提高靶区剂量分布均匀性方面,还是降低靶区内热点剂量及体积方面,都明显优于传统切线野照射技术[4~7]。保乳术后的IMRT技术可采用2种模式:常规剂量分割的IMRT技术和瘤床同步整合补量的IMRT技术(SIB-IMRT)。前者是在全乳调强放疗之后,再进行瘤床的补量,后者则是在全乳放疗的同时实现瘤床加量减少了总的治疗时间。SIB-IMRT技术已在治疗其他部位肿瘤(如头颈部肿瘤,前列腺癌等)中广泛的应用,但在保乳术后放射治疗中的应用报道较少见。
本研究中SIB-IMRT治疗计划的制定采用了三野照射的简易调强技术,其理论优势在于子野数少,单次放射治疗时间短,提高了生物剂量,及可进一步减少因摆位误差和呼吸运动引起的正常组织受量。有研究证明[8],乳腺靶区内的剂量分布均匀性差与乳腺组织纤维化有关,可直接影响到保乳治疗后长期的美容效果。本研究通过对SIB-IMRT与切线野照射后程电子束补量技术进行剂量学上的比较,发现在保证了全乳靶区和瘤床区的覆盖率同时,采取三野照射的SIB-IMRT计划中全乳靶区的Dmax和Dmin,与切线野计划比较没有明显差别,且最大剂量点均位于瘤床区内,与常规切线野照射技术相比,SIB-IMRT技术保持了与其相同的剂量均匀性。调强放射治疗技术的另一主要目的是减少靶区周围正常组织及重要器官的受照射剂量与容积,从而减少其放射损伤。保乳术后放射治疗的一个并发症是心血管系统疾病的损伤,有文献报道采用呼吸门控结合IMRT技术,可进一步减少左侧乳腺癌保乳术后放射治疗患者心脏的受照射剂量与容积[9]。而本研究结果显示,SIB-IMRT技术不需要使用呼吸门控技术,就可以有效地降低左侧乳腺癌患者心脏Dmean、Dmax及D10,显示出SIB-IMRT技术保护心脏方面的优越性。放射性肺损伤是乳腺癌保乳术后放射治疗中另一主要的非致死性放射并发症。本研究结果显示,SIB-IMRT技术能减少同侧肺的Dmean,及接受≥20 Gy照射的体积百分数V20。理论上可降低放射性肺炎,放射性肺纤维化的发生。目前研究对放射诱发对侧乳腺第二肿瘤的发生率尚无定论。本研究显示SIB-IMRT技术与切线野照射技术相比,SIB-IMRT技术的对侧乳腺Dmean明显减小,可能对减少放射诱发对侧乳腺第二肿瘤的发生率有潜在意义。
临床剂量学研究表明,乳腺癌保乳术后使用三野照射SIB-IMRT技术,在保证了靶区覆盖率的同时,可降低心脏、肺、对侧乳腺受照射剂量和容积,并减少了总的治疗时间,在理论上可以期望减少OARs放射损伤发生率,从而进一步提高乳腺癌保乳治疗患者的生活质量。但因受内脏运动、单次剂量和剂量率等因素的影响,SIB-IMRT技术的剂量学优势有待体模及动物实验研究证实。在剂量率相同的情况下,与切线野照射相比,SIB-IMRT增加了单次放疗时间,其对于胸廓运动的影响导致的误差,有待检验。SIB-IMRT技术的应用对于保乳术后患侧乳房远期美容效果的影响,尚需长期随访证实。
[1]Poortmans PM,Collette L,Bartelink H,et al.The addition of a boost dose on the primary tumour bed after lumpectomy in breast conserving treatment for breast cancer.A summary of the results of EORTC 22881-10882"boost versus no boost"trial[J].Cancer Radiother,2008,12(6-7):565-570.
[2]Fisher B,Anderson S,Bryant J,et al.Twenty-year follow-up of a randomized trial comparing total mastectomy,lumpectomy,and lumpectomy plusirradiation for the treatment of invasivebreast cancer[J].N Engl JMed,2002,347(16):1233-1241.
[3]Veronesi U,Cascinelli N,Mariani L,et al.Twenty-year follow-up of a randomized study comparing breast-conserving surgery with radical mastectomy for early breast cancer[J].N Engl J Med,2002,347(16):1227-1232.
[4]Vicini FA,Sharpe M,Kestin L,et al.Optimizing breast cancer treatment efficacy with intensity-modulated radiotherapy[J].Int JRadiat Oncol Biol Phys,2002,54(5):1336-1344.
[5]Donovan E,Bleakley N,Denholm E,et al.Randomised trial of standard 2Dradiotherapy(RT)versusintensity modulated radiotherapy(IMRT) in patients prescribed breast radiotherapy[J].Radiother Oncol,2007,82(3):254-264.
[6]Kestin LL,Sharpe MB,Frazier RC,et a1.Intensity modulation to improve dose uniformity with tangential breast radiotherapy:initial clinical experience [J].Int JRadiat Oncol Biol Phys,2000,48(5):1559-1568.
[7]Formenti SC,Gidea-Addeo D,Goldberg JD,et a1.Phase I-II trial of prone accelerated intensity modulated radiation therapy to the breast to optimally spare normal tissue [J].J Clin Oncol,2007,25(16):2236-2242.
[8]Freedman GM,Anderson PR,Li J,et al.Intensity modulated radiation therapy(IMRT)decreases acute skin toxicity for women receiving radiation for breast cancer[J].Am JClin Oncol,2006,29(1):66-70.
[9]Vingent MR,Vicini FA,Michael BS,et a1.Significant reduction in heart and lung doses using deep inspiration breath hold with active breathing control an d intensity modulated radiation therapy for patients treated with locoregional breast irradiation [J].Int JRadiat Oncol Biol Phys,2003,55(2):392-406.
