注射用丹参无菌粉末冷冻干燥工艺研究Δ
2011-05-22张晓茹王宝华冉晓萌北京中医药大学中药学院北京市100102
张晓茹,王宝华,倪 健,宋 歌,冉晓萌,杨 璇(北京中医药大学中药学院,北京市 100102)
注射用丹参无菌粉末用于治疗心血管疾病,主要功效为活血通脉,临床用于胸痹血瘀证,冠心病、心绞痛等症的治疗[1]。注射用丹参无菌粉末在生产过程中存在冷冻干燥(后简称冻干)周期过长、冻干工艺过程不稳定等问题,易出现不合格产品,导致生产能力不足,资源浪费,严重制约工厂的发展。因此,缩短冻干周期,稳定产品质量已刻不容缓。本课题组通过研究注射用丹参无菌粉末工艺过程中预冻最低温度、降温方式、解析干燥最高温度等影响因素,确定了丹参最优冻干工艺,使其周期大大缩短,产品质量得到显著改善。
1 仪器与试药
LYO-0.4真空冷冻干燥机(上海东富龙科技有限公司);MA45红外水分测定仪(德国赛多利斯公司);高效液相色谱(HPLC)仪,包括LC Solution工作站、SL-20A/SIL-20AC自动进样器、CTO-10AS柱温箱(日本岛津公司)。
丹参浓缩液,由哈药集团中药二厂自制,经笔者稀释为相应浓度后进行冻干试验;乙腈(美国Fisher公司);丹参素钠(批号:110855-200809)、原儿茶醛(批号:110810-200506)、丹酚酸B(批号:111562-200807)对照品均为供含量测定用,购自中国药品生物制品检定所;所用水为注射级用水。
2 方法与结果
2.1 注射用丹参无菌粉末含量测定方法的建立
2.1.1 色谱条件色谱柱:大连依利特Hypersil BDS C18(250 mm×4.6 mm,5 μm);流动相:乙腈-0.1%磷酸,梯度洗脱(0~5 min,10 ∶90;5~7 min,20∶80;7~30 min维持20∶80);检测波长:281 nm;流速:1.0 mL·min-1;柱温:30 ℃。
2.1.2 各对照品溶液的制备 将丹参素钠、原儿茶醛、丹酚酸B对照品置于蒸发皿中,真空干燥箱中减压干燥12 h。减重法精密称定丹参素钠2.1 mg,加蒸馏水定容于10 mL棕色容量瓶中,摇匀,得浓度为0.21 mg·mL-1的丹参素钠对照品溶液,密封贮藏;减重法精密称定原儿茶醛4.3 mg,加蒸馏水定容于10 mL容量瓶中,摇匀,精密吸取1 mL,置于10 mL容量瓶中,加蒸馏水定容,摇匀,得浓度为0.43 mg·mL-1的原儿茶醛对照品溶液,密封贮藏;减重法精密称定丹酚酸B对照品3.9 mg,加蒸馏水定容于10 mL棕色容量瓶中,摇匀,得浓度为0.39 mg·mL-1的丹酚酸B对照品溶液,密封贮藏。
2.1.3 供试品溶液的制备 精密称定注射用丹参无菌粉末3.5 mg,置于10 mL容量瓶中,加蒸馏水定容,摇匀,0.45 μm微孔滤膜滤过,即得。
2.1.4 方法学考察 按2010年版《中国药典》要求进行方法学考察。结果,注射用丹参无菌粉末中丹参素、原儿茶醛、丹酚酸B的线性关系、精密度、重现性、稳定性、回收率的RSD均<5%,符合要求。
2.2 降温方式、药液浓度及装量的考察
配置不同浓度、装量的丹参药液(见表1),置于西林瓶中,装入冻干箱,半压塞。通过改变预冻阶段的降温程序,模拟控制压缩机开停来控制丹参预冻速度[2]。采取阶段性降温和直接降温到最低温度2种方法,得到的产品性状见表2。

表1 丹参药液浓度、装量Tab 1 Concentration and amount of Salvia miltiorrhiza

表2 不同药液浓度和装量、降温方式下的产品性状Tab 2 The property of difference concentrations and amount of herbal liquid under different cooling ways
结果表明,相同浓度装量,阶段性降温较直接降温下的产品性状好;降温方式、浓度相同,产品装量越大,产品冻干的性状越差;相同降温方式相同装量的药液,浓度越大产品的冻干性状越差,故应选择阶段性降温,低浓度低装量的药液。最终选择浓度100、150 mg·mL-1的药液进行试验。
2.3 预冻时间的确定
精密吸取5份丹参药液,按照阶段性降温的方式进行预冻,改变预冻时间,升华干燥与解析干燥阶段程序相同,若高于规格装量的冻干产品未出现顶部鼓泡、喷瓶等现象,则继续缩短预冻时间,直至高于规格装量的冻干产品出现上述现象的时间为最短预冻时间。不同预冻时间的产品性状见表3。

表3 不同预冻时间的产品性状Tab 3 The property of product under different pre-freezing time
结果表明,浓度为100 mg·mL-1、装量为3.48 mL的药液预冻时间为120 min时产品性状良好,装量为4 mL药液有鼓泡,则100 mg·mL-1规格装量药液最短预冻时间为120 min;浓度为150 mg·mL-1、装量为2.10 mL的药液预冻150 min时,产品性状良好,装量为2.5 mL的药液有鼓泡,则150 mg·mL-1规格装量药液最短预冻时间为150 min。
2.4 压力和升华干燥温度对冻干的影响
2.4.1 压力的优选 精密吸取丹参药液,预抽真空至绝对压力为20 Pa,在-30~-25℃升华干燥初期和解析干燥期的5~35℃阶段,为了使温度较快上升,采用不掺气设置,使绝对压力维持在20 Pa左右,其他温度段为本试验所考察的3种绝对压力,即5、12、18 Pa,采取阶段性降温,100 mg·mL-1的药液预冻时间为120 min,150 mg·mL-1的为150 min。以冻干产品外观性状、骨架结构为指标考察不同压力下的产品情况,详见表4。

表4 不同压力下冻干产品的性状及骨架结构Tab 4 The property and skeleton structure of lyophilized product under different pressures
结果,100、150 mg·mL-1药液随着绝对压力的升高,产品性状变差,到达18 Pa时产品均出现内部焦黑,因此选择5 Pa绝对压力。
2.4.2 压力和升华干燥温度间的关系 以150 mg·mL-1、2.10 mL的丹参药液冻干工艺曲线和工艺报表分析压力和升华干燥温度间的关系及压力对产品冻干的影响,对150 mg·mL-1药液升华干燥阶段的数据进行处理,以冻干箱达到预抽绝对压力作为升华的开始,结果见表5。

表5 150 mg·mL-1、2.10 mL药液压力-温变速率Tab 5 Pressure-temperature variation velocity of 2.10 mL herbal liquid with 150 mg·mL-1
结果表明,压力越高,越有利于传热,产品升温越快;压力过高导致产品升温过快,过早超过共熔点会引起产品回溶(即产品外表看似合格,底部存在孔状大小的回溶区域或变色区域,如内部焦黑),质量不合格。压力越低,越有利于传质,水蒸气越易从冻干产品中除去,缩短干燥时间;压力过低,升温过慢,升华过多停留在低温状态,反倒会延长干燥时间。因此,压力应控制为即利于传热也利于传质,即最佳真空度。
2.5 升华干燥时间的优化
分别精密吸取100、150 mg·mL-1的丹参药液5份,通过不断调节高温段(-12~-5℃)的时间,取得最短干燥时间。升华干燥阶段优化时间及参数设置见表6;不同升华干燥时间下产品性状见表7。

表6 升华干燥阶段优化时间及参数设置Tab 6 Optimization time and parameter set of sublimation drying stage
结果表明,100 mg·mL-1、3.48 mL 的药液与 150 mg·mL-1、2.10 mL的药液的最短冻干总时间分别为36、37 h,升华干燥阶段最短时间(即减去预冻时间后的剩余时间)分别为34、34.5 h。
2.6 解析干燥温度的确定
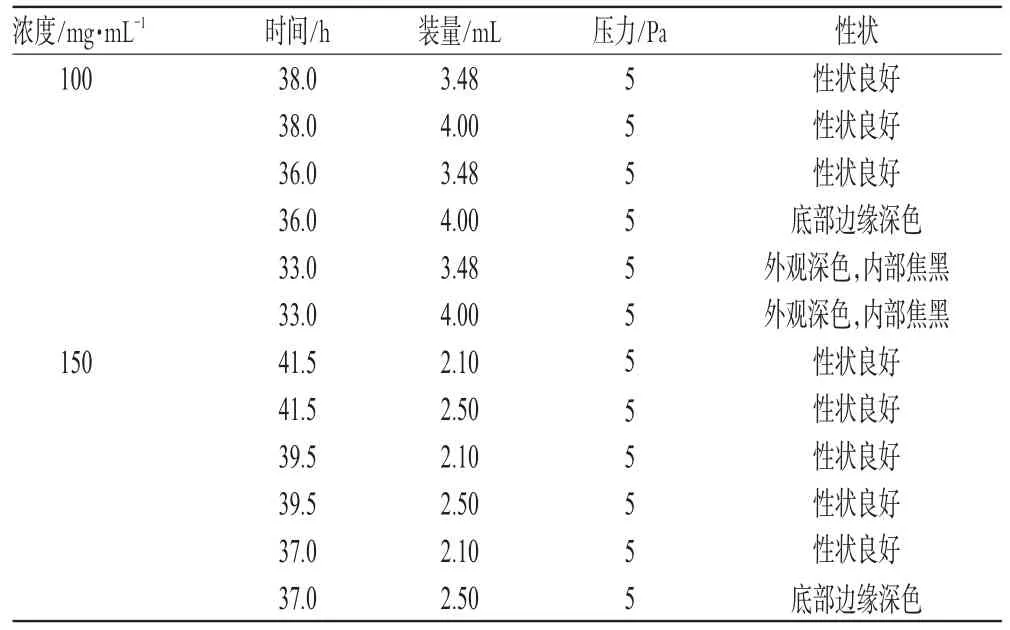
表7 不同升华干燥时间下产品性状Tab 7 Property of products at different sublimation drying time
精密吸取已配置的100 mg·mL-1、3.48 mL,150 mg·mL-1、2.10 mL的丹参药液,选择的最短预冻时间分别为120、150 min,最佳绝对压力为5 Pa,最短解析干燥时间分别为34、35.5 h,解析干燥阶段最高温度设定分别为30、35、45℃。
以冻干产品的含水率作为考察指标,确定解析干燥阶段温度的最高值。取冻干粉1 g,依法[3]测定含水率。结果表明,100 mg·mL-1、3.48 mL,150 mg·mL-1、2.10 mL的丹参药液的注射用无菌粉末样品在解析干燥温度为35℃时含水率均符合药典对注射用无菌粉末含水率的要求,即低于6%[3]。因此,选定解析干燥阶段温度最高值为35℃。
2.7 最优工艺参数的确定
通过以上试验,优选出注射用丹参无菌粉末冷冻干燥的最优工艺参数和过程参数:浓度为100 mg·mL-1,装量为3.48 mL,预冻时间120 min,采用阶段性降温,冷阱温度为-45℃,预抽真空至绝对压力为20 Pa,绝对压力(搁板):-40~-25℃,20 Pa;-25~5 ℃,5 Pa;5~35 ℃,10 Pa;35 ℃,5 Pa;解析干燥温度为35℃;冷冻干燥总时间为36 h。
2.8 验证试验
按上述最优工艺参数,精密吸取浓度100 mg·mL-1、装量3.48 mL的丹参药液,制备30份,平行冷冻干燥3批,每批10支。工艺曲线见图1。
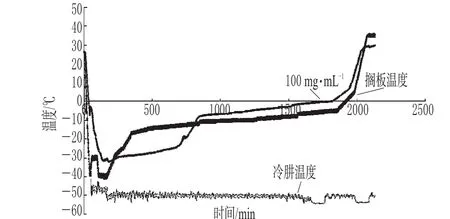
图1 工艺曲线Fig 1 Technology curves
取制备的30瓶样品,考察其物理性质。结果表明,样品骨架完好,韧性好;表面呈棕黄树状晶型且透明;复溶性;含水率为4.95%(药典要求注射剂含水率低于6%)。按“2.1”项下方法测定丹参素、原儿茶醛、丹酚酸B的含量,结果见表8。
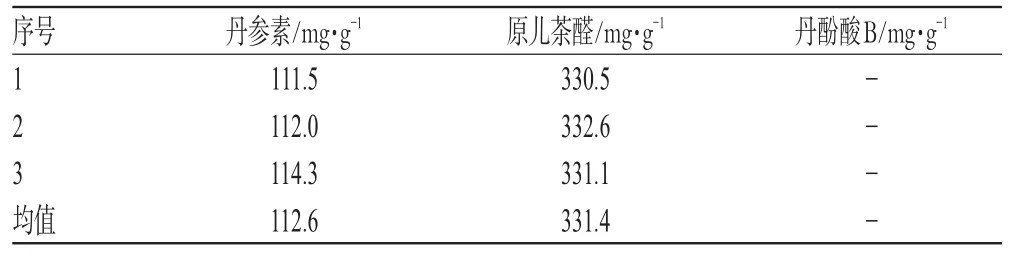
表8 注射用丹参无菌粉末含量测定结果Tab 8 Results of content determination of Salvia miltiorrhiza sterile powder for injection
由表8可知,最优工艺参数下的注射用丹参无菌粉末外观均良好,复溶性快,骨架结构完整,质地坚硬,澄明度良好,且含水率均在6%以下。注射用丹参无菌粉末中丹参素、原儿茶醛的含量分别为112.6、331.4 mg·g-1,丹酚酸B未检出。注射用丹参无菌粉末每支的规格装量为400 mg,本品每支含丹参素钠(C9H9O5Na)不得少于32 mg,每支含总酚以原儿茶醛(C7H6O3)计,应为119~161 mg。表明最优工艺对注射用丹参无菌粉末中主要成分的含量无影响。
3 讨论
阶段性降温较直接降温冻干产品的性状良好;产品装量越大,冻干产品的性状越差;浓度越大,冻干产品的性状越差。在相同的预冻程序下,100 mg·mL-1浓度、3.48 mL装量比150 mg·mL-1浓度的药液预冻速率快;浓度装量相同的药液,直接降温下的预冻速率较阶段性降温快;装量越大,预冻速率越慢,且预冻结束的制品温度越高。
通过试验最终确定丹参冷冻干燥的最优工艺参数和过程参数为100 mg·mL-1,装量3.48 mL,预冻时间120 min,冷凝器的温度为-45℃,预抽真空至绝对压力为20 Pa,升华干燥前期,即搁板温度为-40℃~-25℃时,绝对压力为20 Pa,-25℃~5℃时绝对压力为5 Pa,5℃~35℃解析干燥时期绝对压力为20 Pa,达到最高温度后为使传质速率加快,绝对压力为5 Pa,升华解析干燥阶段时间为34.5 h,冷冻干燥总时间为36 h,解析干燥阶段最高温度为35℃。
本课题组确定了丹参最优冻干工艺,使冻干周期缩短,改善了冻干产品质量,可为注射液丹参无菌粉末的生产及研究提供参考。
[1]赵淑娟,章国瑛,刘 涤,等.丹参水溶性酚酸类化合物药理及生物合成途径研究进展[J].中草药,2004,35(3):341.
[2]姚 静,张自强编著.药物冻干制剂技术的设计及应用[M].北京:中国医药科技出版社,2007:92-93.
[3]国家药典委员会编.中华人民共和国药典(一部)[S].2010年版.北京:中国医药科技出版社,2010:附录52.
