胰岛素抵抗与多囊卵巢综合征
2011-04-10武汉市第五医院妇科湖北武汉430050
(武汉市第五医院妇科,湖北 武汉430050)
多囊卵巢综合征(polycystic ovarian syndrome,PCOS)是指青春期前后发病,卵泡膜细胞良性增生引起的雄激素生成过多造成月经紊乱、持续性排卵障碍、高雄激素血症及卵巢多囊样变等一系列表现[1]。胰岛素促进器官、组织和细胞吸收、利用葡萄糖的效能下降时,称胰岛素抵抗(insulin resistance,IR)。葡萄糖耐量试验(OGTT或IGTT)后,血胰岛素反应高亢,但血糖反应正常,即提示存在胰岛素抵抗(IR)。高胰岛素血症是胰岛素抵抗状态下胰岛素调节糖代谢尚处于代偿阶段的标志。约有50%的多囊卵巢综合症(PCOS)患者不同程度上存在胰岛素抵抗及代偿性高胰岛素血症,目前越来越多的研究认为胰岛素抵抗及高胰岛素血症在多囊卵巢综合征的发病中起着早期和中心作用,胰岛素抵抗、高胰岛素血症是慢性高雄激素性不排卵妇女的重要特征。
1 胰岛素抵抗和高胰岛素血症在PCOS中的病理生理作用
过量胰岛素可引起高雄激素血症,主要通过以下途径:①过量胰岛素通过直接或者间接作用于垂体的胰岛素受体,增加黄体生成素(LH)释放并促进卵巢和肾上腺分泌雄激素,使雄激素合成增加。②过量胰岛素抑制肝脏性激素结合球蛋白(SHBG)的合成,使游离雄激素增加,增多的双氢睾酮和雄烯二酮在外周分别向双氢睾酮和雌酮的转化增多,增多的双氢睾酮导致女性男性化表现,如痤疮和/或多毛,而雌酮的增多,使雌酮/雌二醇比值增大。由于在外周转化的雌酮不受垂体促性腺激素的调节,导致无周期性高雌环境,可进一步反馈性地增强下丘脑/垂体的促性腺激素释放激素/黄体生成素(GnRH/LH)分泌,LH持续高水平、无周期性分泌,不形成月经中期的LH峰,故无排卵发生。同时高LH又促进卵巢分泌雄激素,形成雄激素过多、持续无排卵的恶性循环。
胰岛素水平的异常升高,刺激卵巢分泌过多的雄激素,卵巢局部过高浓度的雄激素不仅不能提高颗粒细胞芳香化酶活性及促进雌激素的产生,反而转化为不能芳香化的双氢睾酮,并抑制卵泡刺激素(FSH)诱导的芳香化酶活性及颗粒细胞LH受体生成,引起FSH-颗粒细胞轴的功能低下,卵泡缺乏FSH的刺激,生长速度缓慢,导致窦前卵泡和小窦状卵泡堆积,卵泡不能发育成熟,导致大量窦卵泡积聚,形成特有的多囊卵巢的形态。
高雄激素血症还可以引起多囊卵巢综合症(PCOS)患者体内的脂质代谢紊乱,但可以平衡由于长期闭经对骨质的退化性影响。
2 对PCOS中胰岛素抵抗的评估
2.1 胰岛素抵抗在COS中的临床征象
研究者发现近来大约有半数PCOS患者的发病与胰岛素爱体丝氨酸磷酸化缺陷有关。因而认为胰岛素在其发病中占有重要地位。胰岛素与IGF-1通过IGF-1受体作用于卵泡膜细胞,促使雄烯二酮和睾酮合成。这几年的探索研究发现,垂体邻近部位有胰岛素受体,或同时存在的高IGF-1血症可促进LH刺激的卵泡膜细胞增生,导致雄性激素过多和卵泡过早闭锁[2](如图1)。Hasegawa用胰岛素增敏剂Troglitazone治疗PCOS,可以大大降低胰岛素水平。LH与雄性激素水平相应降低也支持这一说法。胰岛素升高对调节SHBG的代谢有重要作用,能让肝脏SHBG生成相对减少,游离睾酮升高。此外,胰岛素受丝氨酸磷酸化可抑制胰岛素受体活性,促进P450C17A的17,20-链裂酶活性。这几年在对位于染色体11pl5.5的胰岛素基因的5’-端可变数串联重复顺序(VNTR)的研究发现,胰岛素基因的VNTR是PCOS的一个主要易咸位点(特别是排卵性PCOS),说明胰岛素VNTR多态性是PCOS的遗传学因素。
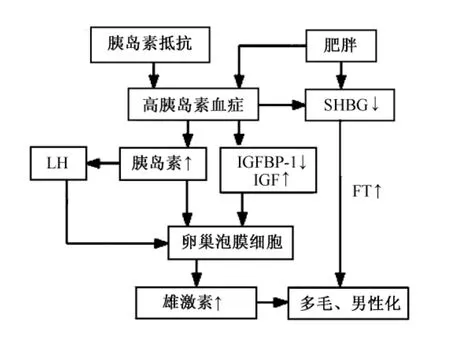
图1 胰岛素抵抗与高雄激素血症的关系
2.2 临床评分法
在业内,有研究根据PCOS中对于胰岛素抵抗临床征象采用评分来判断患者是否存在胰岛素抵抗:有2型糖尿病、高血压、心肌梗死家族史评2分,男性型脂肪分布(WHR>0.85)、高血压(>140/90mmHg)、高三酰甘油(>1.9mmol/L)、高尿酸血症(>386.8mmol/L)、脂肪肝(谷氨酸转氨酶>25IU/L或超声密度)各判1分,总分值3分以内则基本不疑有胰岛素抵抗;而≥3分则疑有胰岛素抵抗,可做75g葡萄糖耐量试验(OGTF)。
如果不测胰岛素或能直接判定为糖耐量受损即可基本确定为胰岛素抵抗,假如有患者血糖值正常,就可以通过测定血胰岛素水平,若≥15mIU/L则也可认为存在胰岛素抵抗,这个办法简单可行。只是这方法对年轻患者的准确率很大,因为大多数年轻患者胰岛素抵抗处于代偿期,尚未出现上述严重的代谢紊乱及等征象,因此临床征象评分法存在一定的局限性。
3 针对性治疗
早期发现和早期治疗胰岛素抵抗能有效治疗多囊卵巢综合症(PCOS)患者的代谢综合征、改善生殖功能,并能起到防治其远期并发症的作用,降低2型糖尿病、高血压、缺血性心脏病、心肌梗死、高脂血症、子宫内膜癌等疾病的发生率和严重程度。研究表明,约有50%PCOS患者存在着不同程度的胰岛素抵抗及代偿性高胰岛素血症。基于胰岛素抵抗/高胰岛素血症在PCOS发病中起到的重要作用,可采取以下针对性治疗。
3.1 调整生活方式
同糖尿病的基础治疗措施一样,肥胖型多囊卵巢综合征患者也应注重调整生活方式,即限制热量、控制饮食并进行耗能锻炼以减轻体质量和腹围,控制饮食的热量可降低血清17α-羟孕酮、总睾酮、游离睾酮以及空腹胰岛素水平,降低卵巢内细胞色素P450的活性,提高性激素结合球蛋白水平,改善胰岛素敏感性;科学而合理的耗能锻炼可以通过提高肝内糖原合成,上调骨骼肌葡萄糖转运蛋白的表达,增加胰岛素受体的磷酸化等一系列作用,改善胰岛素抵抗性。胰岛素抵抗得以改善可使雄激素水平下降,LH/FSH比值正常,进而可改变或减轻月经紊乱、多毛、痤疮等症状,部分患者还可恢复排卵,有利于不孕的治疗。肥胖型PCOS患者刻意地减轻体质量还能显著改善代谢异常,降低糖尿病、高血压及高脂血症等的发病率,提高生活质量。
3.2 使用胰岛素增敏剂
胰岛素增敏剂可改善外周组织对胰岛素的敏感性,增加对葡萄糖的摄取和利用,抑制肝糖的产生,降低胰岛素的浓度,改善多囊卵巢综合症(PCOS)中其他相关的内分泌紊乱,促进排卵,对降低多囊卵巢综合症(PCOS)的近期和远期合并症的发生也有帮助。是胰岛素抵抗的重要治疗措施。目前常用的胰岛素增敏剂有:
3.2.1 双胍类 常用的双胍类降糖药有美迪康(盐酸二甲双胍)。其主要作用机制为抑制肝葡萄糖输出,促进糖的无氧酵解,增加外周组织对糖的摄取和利用,从而改善糖代谢紊乱;提高胰岛素受体的敏感性,从而改善胰岛素抵抗,降低血胰岛素水平。还可以增加对克罗米芬(CC,一种促排卵药物)的敏感性,提高其促排卵效果。应用之前应先给患者做OGTT及胰岛素释放试验,检测血脂、血压、激素及肝功能等,了解病人全面情况。一般剂量为1500mg/d,其副反应小,因而耐受性好,主要副作用是呕吐、腹泻等胃肠道反应,为减轻胃肠道反应,可以采用低剂量逐渐增量法。开始剂量为500mg,1次/d,3~4d,用餐时服,然后500mg,2次/d,3~4d;500mg,3次/d,3~4d;最后加到1000mg,2次/d,连续服用3~6个月,可明显改善患者的内分泌紊乱[3-4]。
3.2.2 噻唑烷二酮类 噻唑烷二酮类是一类新的胰岛素增敏剂,目前临床常用的是曲格利酮、罗格列酮,它一方面可通过与高选择激动脂质过氧化物酶体增殖激活体γ(PPARγ)结合,调节胰岛素应答,逆转胰岛素抵抗(IR),降低血清胰岛素水平,从而间接降低雄激素水平;另一方面作为胰岛素增敏剂直接作用于卵巢,调节卵巢本身糖代谢异常所致的胰岛素抵抗,使其恢复对促性腺激素的敏感性。服用方法:400mg,每日与早餐同服。Mitwally对克罗米芬拮抗的PCOS患者进行了研究,发现单独用曲格利酮治疗或与克罗米芬合用时,能显著提高妊娠率,但要注意其对肝脏的毒性作用。另外它还有可能增加体重,并导致贫血、水潴留,甚至充血性心力衰竭,故应用时应该严格掌握指征,并注意观察用药后反应。但因为其对肝毒性大,目前美国FDA已禁止使用该药。
3.3 抑制胰岛素分泌的药物
近年来人工合成的生长抑素类似物奥曲肽,是一种下丘脑内源性14氨基酸肽,不仅能抑制LH对促性腺激素释放激素(GnRH)的反应性,还能减少脑下垂体生长激素的释放,抑制胰岛素的释放,降低血中胰岛素浓度,使SHBG水平升高,并恢复其糖耐量试验中胰岛素的正常反应,进而减少卵巢雄激素的产生。卵巢中存在生长抑素受体,因此奥曲肽可在卵巢直接发挥作用 ,促进排卵。
3.4 血管紧张素转换酶(ACE)抑制剂
赖诺普利与调节卵巢内肾素-血管紧张素系统(RAS)功能相关,可加强餐后胰岛素敏感性,降低血糖。口服10mg/d,连用4周,可明显降低血清游离睾酮浓度,而不影响SHBG水平。
3.5 α-葡萄糖苷酶抑制剂(AGI)
阿卡波糖可通过抑制小肠粘黏膜刷状缘上的α-葡萄糖苷酶活性来抑制食物中淀粉、糊精和双糖(如蔗糖)分解为葡萄糖,有效延缓葡萄糖在小肠内的吸收,降低餐后血糖和平均血糖。PCOS患者使用AGI,150~300mg/d,连用3个月,改善PCOS的高胰岛素血症、胰岛素抵抗和高雄激素血症[5],促进月经恢复。
3.6 β-内啡肽受体抑制剂
β-内啡肽受体抑制剂包括纳洛酮和纳曲酮,能改善胰岛素抵抗,但其具体效果及安全性有待进一步研究。
多囊卵巢综合症中胰岛素抵抗的表现具有多样化,胰岛素抵抗引起多囊卵巢综合症的发病机制更是错综复杂,还有很多尚不明确的问题待解决,希望有更多进一步的相关研究能帮助明了这些问题,以便预防和/或更好地治疗多囊卵巢综合症。
[1]周应芳.妇产科热点问题聚焦 [M].北京:北京大学医学出版社,2007:193-212.
[2]乐杰.妇产科学 [M].7版.北京:人民卫生出版社,2008:315-318.
[3]迟贞旎,洪杰.多囊卵巢综合征的治疗方法 [J].上海交通大学学报:医学版,2008,28(3):331-335.
[4]郁琦(执笔).多囊卵巢综合征诊治标准专家共识 [J].中国实用妇科与产科,2007,23(6):474.
[5]陆再英,钟南山.内科学 [M].7版.北京:人民卫生出版社,2008:780-784.
