以超导炭黑为还原剂制备磷酸钒锂
2011-02-28曹福彪
曹福彪,马 叙,吕 菲,徐 宁
(1.天津理工大学材料科学与工程学院,天津 300384;2.天津巴莫科技股份有限公司,天津 300384)
以磷酸根聚阴离子为基础的正极材料具有环保、安全性能好、成本低廉、结构稳定及电化学性能较好[1]等优点,代表材料之一是磷酸钒锂[Li3V2(PO4)3]。目前,Li3V2(PO4)3的制备方法主要有高温固相法、溶胶-凝胶法、热液法、掺杂法及软化学法(如微波法)等[1-7]。刘素琴等[2]用溶胶-凝胶法制备的 Li3V2(PO4)3以 0.1C在3.0~4.3 V充放电,首次放电比容量为129.8 mAh/g,循环100次后,放电比容量仍有128 mAh/g。该方法所得产物容量较高,但与热液法一样,制备过程很难控制,不适于工业化生产。掺杂法可提高材料的导电性;但掺杂金属离子会增加生产成本,掺杂金属镍[3]会降低容量,镁在锂位掺杂[4]可将容量提高约7%;微波法[5]与其他方法[6-7]对设备要求较高,工业化生产困难。
高温还原法是研究相对成熟,也是最有可能进行工业化生产的方法[8]。遵循操作性强、可工业化实施的原则,本文作者以超导炭黑为还原剂,采用湿法球磨、碳热烧结还原,合成Li3V2(PO4)3,并分析了产物的性能。
1 实验
1.1 材料的制备
按n(Li)∶n(V)∶n(P)=3.1∶2.0∶3.0将 Li2CO3(四川产,≥99.5%)、V2O5(安徽产,≥99.5%)和 NH4H2PO4(四川产,99.7%)依次加入球磨罐中,加水后,待无大量气泡放出时,加入过量 115%的超导炭黑(日本产,科琴黑 ECP 600JD),在 KQM-X4行星式球磨机(陕西产)上球磨(频率为40 Hz,球料比为8∶1)4 h,之后在80℃下完全烘干,再在FW135高速破碎机(天津产)中以24 000 r/min的速度将前驱体破碎2 min,然后在马弗炉中、300℃下烧结4 h,除去多余的H2O、NH3及 CO2。 材料冷却后,仔细研磨 30 min、过100目筛,在通入N2保护的管式炉中、800℃下烧结12 h,最后自然冷却,研磨、过100目筛,制得 Li3V2(PO4)3材料。
1.2 电池的组装及性能测试
以N-甲基吡咯烷酮(NMP,濮阳产,电池级)为溶剂,将Li3V2(PO4)3、乙炔黑(上海产,电池级)和聚偏氟乙烯(PVDF,无锡产,电池级)按质量比8∶1∶1混合,制成正极浆料,涂覆在20μ m厚的铝箔(浙江产,电池级)上,在烘箱中、80℃下干燥12 h,制成正极片(Φ=12 mm,压制的压力为6 MPa,活性物质含量约为20 mg)。
以金属锂片(北京产,电池级)为负极,1 mol/L LiPF6/EC+DMC(体积比1∶1,哈尔滨产,电池级)为电解液,Celgard 2400膜(美国产)为隔膜,在充满氩气的手套箱中组装CR2025型电池。
以NMP为溶剂,将制得的Li3V2(PO4)3、导电炭黑(哈尔滨产,电池级)、乙炔黑和PVDF按质量比 92∶3∶2∶3混合制浆,均匀涂覆在铝箔上,在100℃下烘干12 h,碾压成 40 μ m厚,裁剪为360 mm×41 mm的电极。以石墨碳(青岛产,电池级)为负极,经卷绕、真空自吸式注液、化成等工序,制得053048型电池。化成步骤为:以1.0C恒流充电至4.3 V,恒压充电到电流为15 mA,再以1.0C恒流放电至3.0 V;将充放电电流调整为0.5C,重复上述步骤一次。
用电感耦合等离子体发射光谱(ICP)仪(北京产)定量分析Li、V、P元素;用 D/Max-2500X全自动 X射线衍射仪XRD(日本产)进行物相分析,测角精度为0.02°,Cu靶,扫描速度为8(°)/min,管流150 mA、管压40 kV。
用SSA-4200比表面积孔径测定仪(北京产)测定比表面积;用JSM-6700F场发射电镜(日本产)进行形貌观察;用Mastersizer 2000全自动激光粒度仪(英国产)测量粒径。
用CT2001A电池测试系统(武汉产)测试电化学性能,电压为3.0~4.3 V。CR2025型电池的充放电电流为0.1C。
将1.0C、3.0C、5.0C、10.0C和15.0C恒流放电与1.0C、4.3 V恒流-恒压充电作比较,即放电容量与充电容量之比为容量保持率,测试电池在不同倍率下的容量保持率。
2 结果与讨论
2.1 元素含量分析
样品中Li、V及P的含量如表1所示。
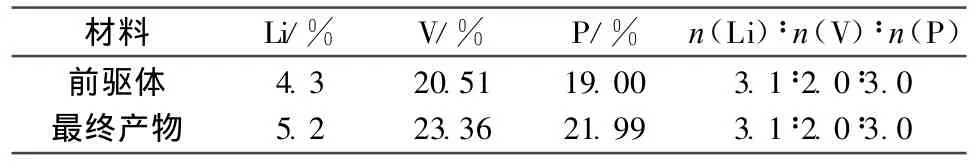
表1 样品中Li、V及P的含量Table 1 The content of Li,V and P in the samples
从表1可知,反应前后各元素的含量变化较小,前驱体与最终产物基本上符合n(Li)∶n(V)∶n(P)=3.1∶2.0∶3.0。在充放电过程中,会有部分Li+用于形成固体电解质相界面(SEI)膜,导致材料不符合Li3V2(PO4)3的化学计量比,因此锂元素过量。最终产物中Li、V及P的含量均比前驱体高,原因是高温反应时排出了部分在预处理中未完全排出的NH3、H2O、CO2,也有导电炭被氧化生成CO及CO2。
2.2 结构分析
对制备的Li3V2(PO4)3进行XRD分析,结果见图1。
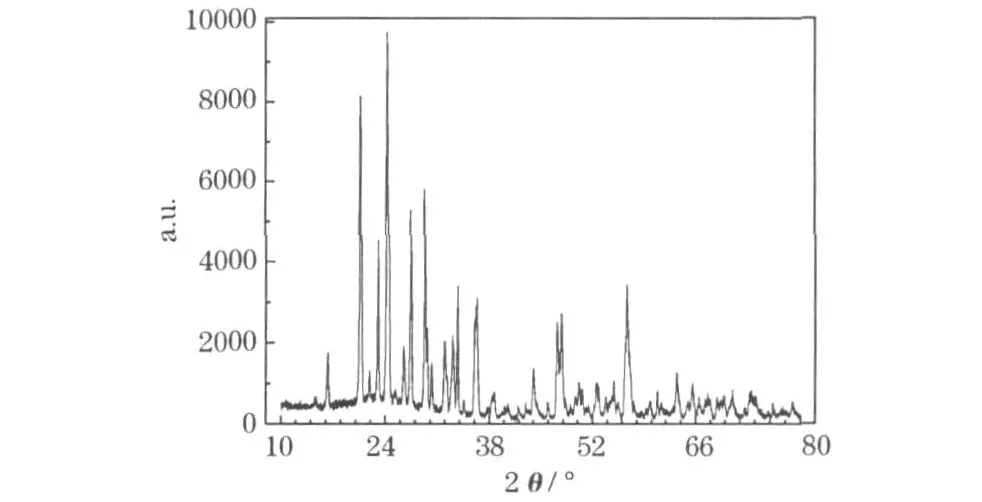
图1 制备的 Li3V2(PO4)3的XRD图Fig.1 XRD pattern of prepared Li3V2(PO4)3
图1中的各衍射峰与文献[7]中的一致,且强度较强,说明样品为单斜结构的Li3V2(PO4)3,晶粒内部排列较规则。
2.3 电池的首次充放电效率分析
组装的CR2025型电池的首次充放电曲线见图2。
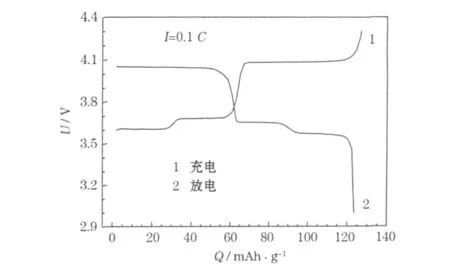
图2 组装的CR2025型电池的首次充放电曲线Fig.2 Initial charge-discharge curves of assembled CR2025type cell
从图2可知,充、放电曲线均有3个平台,比较符合Li3V2(PO4)3多放电平台的特点。3个充电平台分别位于3.6 V、3.7 V及4.1 V左右,其中3.6 V和3.7 V处对应第1个Li+的脱出,4.1 V处对应第2个Li+的脱出。制备的Li3V2(PO4)3首次充、放电比容量分别为126.8 mAh/g和123.5 mAh/g,首次充放电效率为97.4%。
实验使用的超导炭黑有较高的比表面积(952 m2/g),粒径约为30 nm。粒度小,能很好地分散在材料中;比表面积高,则可提高反应效率。过量的超导炭黑可提高导电性,因此制备的Li3V2(PO4)3电性能较好。
2.4 形貌分析
制备的Li3V2(PO4)3的SEM图见图3。

图3 制备的Li3V2(PO4)3的SEM图Fig.3 The SEM photographs of prepared Li3V2(PO4)3
从图3可知,Li3V2(PO4)3颗粒有部分团聚,未团聚的颗粒较小,且表面光滑,大部分颗粒的粒径约为10 μ m。附着在Li3V2(PO4)3表面的、大量未反应的超导炭黑,均匀地分散在材料表面,提高了导电性,使得制备的Li3V2(PO4)3具有较好的充放电性能,充放电效率也较高。
2.5 电池的循环性能分析
组装的053048型电池的循环性能见图4。
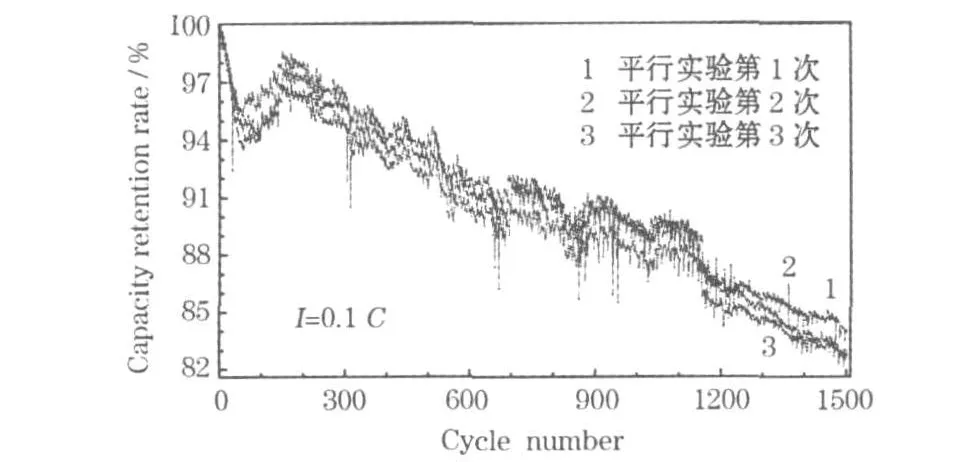
图4 组装的053048型电池的循环性能Fig.4 Cycle performance of assembled 053048 type battery
从图4可知,以0.1C循环 1 500次,Li3V2(PO4)3的容量保持率仍有82%。Li3V2(PO4)3在前几十次循环中的容量保持率降幅很大,随后的循环中,降幅变小,曲线总体变化趋势比较平缓。由此看出,Li3V2(PO4)3的循环性能较好,基本能满足1 500次循环、容量保持率在80%以上的要求。
2.6 倍率分析
快速充放电是锂离子动力电池的一个重要性能指标。组装的053048型电池的快速充放电性能见图5。
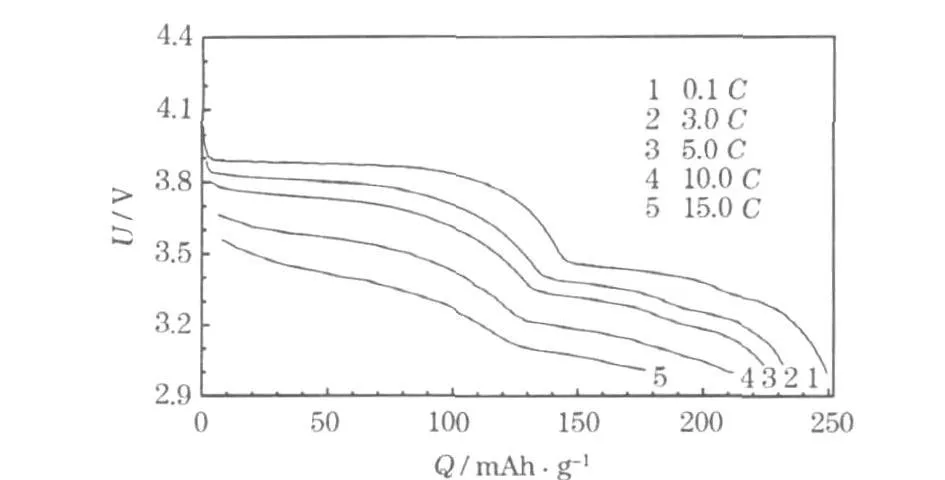
图5 组装的053048型电池的倍率性能Fig.5 The rate capability of assembled 053048 type battery
从图5可知,电池的3.0C、5.0C、10.0C及15.0C放电容量分别为 1.0C充电容量的94.0%、90.9%、85.0%及73.3%。由此可知,制备的Li3V2(PO4)3在快速充电时仍能保持较高的容量。
3 结论
以Li2CO3、NH4H2PO4、V2O5和超导炭黑通过湿法球磨碳热烧结,合成了具有单一晶相组成的锂离子电池正极材料Li3V2(PO4)3。形貌分析结果显示:晶粒生长完全,颗粒比较光滑,表面有过量的导电炭均匀的附着在上面,提高了材料的导电性,材料的粒径在10μ m左右。
组装的CR2025型电池以0.1C在3.0~4.3 V充放电,首次充电比容量为126.8 mAh/g,首次充放电效率为97.4%。组装的053048型电池以1.0C在3.0~4.3 V充放电,第1 500次循环的容量保持率为82%,且倍率性能较好,15.0C放电容量可达1.0C充电容量的73.3%。
用导电炭ECP做还原剂,还原效果好,而过量的导电炭包覆在材料表面,可提高材料的导电性。制得的 Li3V2(PO4)3比容量高、电池循环性能好,倍率放电性能好。
[1] Saidi M Y,Barker J,Huang H,et al.Electrochemical properties of lithium vanadium phosphate as a cathode material for lithium-ion batteries[J].Electrochem Solid-State Lett,2002,5(7):A 149-A 151.
[2] LIU Su-qin(刘素琴),TANG Lian-xing(唐联兴),HUANG Kelong(黄可龙),et al.溶胶-凝胶法制备 Li3V2(PO4)3及其性能研究[J].Chinese Journal of Inorganic Chemistry(无机化学学报),2006,22(6):1 067-1 071.
[3] LIU Yun-xia(刘云霞),ZHANG Fang-qin(章芳琴),GEN Liangmei(耿良梅),et al.Li3V2(PO4)3掺镍的性能研究[J].Journal of Huazhong Normal University(华中师范大学学报),2008,42(4):578-582.
[4] GUO Xiao-dong(郭孝东),ZHONG Ben-he(钟本和),TANG Yan(唐艳),et al.Mg2+掺杂对锂离子正极材料Li3V2(PO4)3的影响[J].Chemical Research and Application(化学研究与应用),2008,20(5):625-627.
[5] REN Man-man(任慢慢),LI Yu-zhan(李宇展),ZHOU Zhen(周震),et al.微波法合成正极材料 Li3V2(PO4)3[J].Battery Bimonthly(电池),2006,36(1):13-14.
[6] HOU Chun-ping(侯春平),YUE Ming(岳敏).液相球化法合成新型正极材料磷酸钒锂[J].Acta Physico-Chimica Sinica(物理化学学报),2007,23(12):1 954-1 957.
[7] Christopher M B,Roger F.Vibrational spectroscopic studies of monoclinic and rhombohedral Li3V2(PO4)3[J].Solid State Ionics,2007,177(39-40):3 445-3 454.
[8] LI Kai-fan(李岂凡),HU Shu-fen(胡淑芬),YE Zhi-qiang(叶志强).锂离子电池正极材料Li3V2(PO4)3研究进展[J].Jiangxi Chemical Industry(江西化工),2008,4(4):1-4.
