A l掺杂对甲醇醇解法合成纳米粉体的影响
2011-02-06陈义川胡跃辉张效华杨丰陈新华陈俊
陈义川 胡跃辉 张效华 杨丰 陈新华 陈俊
(景德镇陶瓷学院机械电子工程学院,江西景德镇333001)
0 引言
氧化锌(ZnO)是重要的工业原料,在塑料和橡胶添加剂、传感器、发光显示器件等领域有着广泛的应用。ZnO作为一种新型的光电材料,在声表面波、透明电极、发光器件等领域也有着巨大的发展潜力。由于其激子束缚能(60meV)远大于室温热能,因此在室温下可获得高效的与激子相关的受激发射。该发射波长比GaN的发射波长更短,可以进一步提高光信息的记录密度和存取速度,ZnO材料成为继GaN宽带隙半导体材料之后在光电领域中又一研究热点[1-3]。
目前,制备ZnO纳米粉体的方法有很多,如:液相法、水热法、氧化法等[4,5]。而且采用化学法合成纳米ZnO粉体已有大量的相关报道。不同方法制备ZnO纳米材料的机理和最终产品的性能各有差异,其中水热法和溶剂热法具有简单易控的优点而倍受关注。本实验采用无水甲醇醇解法在较低温度(130℃)下合成棒状的ZnO晶体,具有操作简单,低温易控制,生成的晶体杂质少等优点。由于Al3+半径小于Zn2+半径,在ZnO晶体形成过程中,Al3+很容易取代Zn2+进入晶格,在ZnO晶体中形成更多的氧空位,所以在ZnO的能带间隙之间形成一定的杂质缺陷。
1 实验
本实验采用原料:醋酸锌(Zn(CH3COO)2-2H2O,分析纯,上海青析化工),无水甲醇(CH3OH,分析纯,上海试剂一厂),九水硝酸铝(Al(NO3)3·9H2O,分析纯,天津市风船化学),无水乙醇(CH3CH2OH,分析纯,上海久亿)。因此配制两种溶液分别为:(1)醋酸锌和无水甲醇,按摩尔比为1∶40混合。(2)醋酸锌和无水甲醇,摩尔比是1∶40,再掺杂Al(Al/Zn比例为3%,掺杂物为Al(NO3)3·9H2O)。将两种溶液在常温下搅拌30min,使溶质充分溶解,放入内衬为聚四氟乙烯的45ml的不锈钢反应釜。在130℃的条件下,反应24hrs后,取出,自然冷却,得到白色沉淀。用无水乙醇冲洗后,在130℃的温度下干燥4hrs,最后得到白色粉末。分别为样品I∶ZnO晶体,样品II∶Al掺杂ZnO晶体。

图1 不同条件下合成的Z n O晶体的X R D图谱Fig.1 XRD patterns for the powders synthesized under various conditions
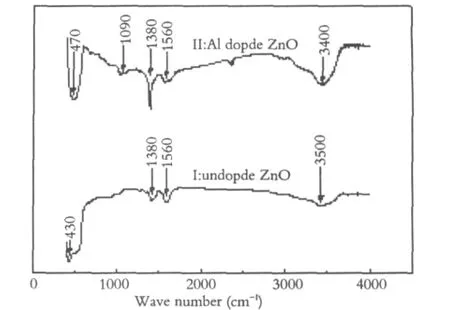
图2 Z n O纳米粉体的F T I R光谱Fig.2 FTIR spectra of sample I:undoped ZnO and sample II:Al doped ZnO

图3 不同合成条件下所制备Z n O纳米粉体的T E M图片(a)和(b):Z n O、(c)和(d):A l掺杂Z n OFig.3 Transmission electron microscope(TEM)images of ZnO nanopowder prepared under different conditions (a)and(b):undoped ZnO,(c)and(d):Al doped ZnO
采用X射线衍射仪(Dmax-rB,X-ray diffraction, XRD)表征ZnO晶体的物相结构,Cu Kα辐射λ= 0.15418nm。采用透射电子显微镜(TEM,JEM-2010)研究ZnO晶体的形貌结构。采用Fourier变换红外光谱仪(FTIR,SHIMADZUIRprestige-21)对ZnO晶体进行结构分析。采用偏振稳态荧光光谱仪(NicoletF-7000)分析ZnO晶体的光致发光性能。
2 结果与讨论
图1为在不同条件下合成的ZnO晶体的XRD图谱。从图1中可知,样品I和II均为ZnO晶体的六方晶系,其衍射峰与标准卡片(JCPDS75-0576)中六方相ZnO的(100),(002),(101),(102)和(110)晶面衍射峰一致。与文献中的醇解法合成ZnO纳米粉体相比[10],本实验采用的甲醇醇解法的反应温度下降了120℃。
图2为ZnO纳米粉体的红外吸收光谱。在波数为4000~400cm-1,分辨率为5cm-1,高纯KBr压片的测试条件下,得到FTIR图谱。图2所示,样品I和样品II分别在430cm-1和470cm-1出现的吸收峰,都是Zn-O-Zn的振动吸收峰。样品I和样品II的吸收曲线中都出现了:1380cm-1,1560cm-1和3400cm-1吸收峰,分别为醇中的甲基(-CH3)的弯曲振动特征峰,乙酸锌中COO-的振动吸收峰和O-H键的伸缩振动吸收峰。这说明了ZnO晶体表面吸附了有机成分,如羟基。样品II的吸收曲线出现的1090cm-1的吸收峰为C-O键的伸缩振动吸收峰。对比样品I和II的吸收曲线,可发现:样品I的吸收曲线中没有出现1090cm-1的吸收峰。这说明溶液中加入一定的酸根离子(NO3-)会游离有机物中的OH-上的H+离子(如-CH2OH变为-CH2O-),从而形成C-O单键。ZnO纳米晶体形成过程是:(1)在一定温度条件下,甲醇与乙酸锌之间发生醇解反应,形成前驱体Zn(OH)2;(2)前驱体Zn(OH)2发生脱水反应,形成ZnO晶核,这些晶核迅速发育成为极为细小的ZnO纳米晶粒(如图3(a)中,所观察到的10nm左右的细小晶粒)。(3)伴随着ZnO晶粒的生长,出现了比较规则的六棱形单晶(如图3(c)所示)。
图3中的(a)和(b)是样品I的TEM图片。图3中(c)和(d)是样品II的TEM图片。从图2的TEM图片中清楚看到通过甲醇醇解合成的ZnO晶体呈明显的六棱柱棒状结构。由于晶粒细小,虽然可以明显的看到晶粒间的界限(图3(b)所示),但是出现了晶粒团聚。晶粒直径平均大小在30nm以下,与Scherrer公式计算结果一致。从图3(c)中可以清楚的看到,样品II呈现明显的六方晶相生长。在晶粒中,均匀的分散着标准的六棱形晶粒(如图3(d)中所示)。六棱晶粒的平均尺寸较大,最大的晶粒直径尺寸达到70nm。从TEM图中也可以看出,样品II晶粒有较好的均匀性和分散性。
2.4 荧光光谱分析
图4为样品I和II在室温下的荧光光谱(标准化图谱),激发波长都是380nm。由图4可知,样品I和II在400nm到650nm之间形成一个可见光的发光带。由于样品I和样品II中ZnO的晶粒都比较大,所以激子浓度降低,从而由自由激子复合产生的紫外发光强度降低,所以没有出现紫外发光峰。可知ZnO发光峰的能量如下式:

其中,h是普朗克常数,其值为4.13566743×10-15eV·s, ν是辐射频率。
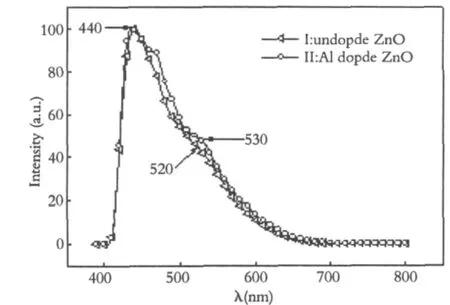
图4 室温下样品I,I I的荧光光谱Fig.4 Room-temperature photoluminescence(PL)emission spectra of samples I:ZnO,II:Al doped ZnO
从图4中可知,样品I和II都有可见光的蓝光发光带,在440nm(2.81ev)处出现发光峰。一般蓝光发射与氧空位或锌填隙有关。氧空位的浅施主能级(位于导带以下0.3~0.5eV)与价带顶之间的能隙约为2.8eV,这与所观测到的2.81eV的光子能量一致。所以2.81eV的蓝光发射可认为源于氧空位的浅施主能级和价带之间的电子跃迁。ZnO蓝光发射的另一种可能来源于锌填隙的浅施主能级和价带之间的电子跃迁。因为对禁带宽度为3.36eV的ZnO来说,锌填隙的能级为2.9eV,位于价带以上,这也接近2.81eV蓝光发射的光子能量。
样品I和II分别在520nm(2.39 eV)和530nm (2.35eV)处出现发光肩峰。而根据全势线性多重轨道理论计算结果[6],导带到OZn缺陷的能级差为2.38eV,与观察到的绿色发光峰能量一致。因此可以认为此绿光发光中心与OZn有密切的关系。由于样品II掺杂了Al3+,在晶体形成过程中,Al3+取代了Zn2+,形成了更多的OZn空位,致使其在绿光的发光峰位置红移了10nm。
3 结论
采用醇解法,在甲醇溶液中和较低温度下合成ZnO晶体。通过XRD,透射电镜和电子衍射分析表明:该ZnO晶粒为六棱形棒状或六棱单晶。高分辨透射电镜分析表明:ZnO纳米晶粒有很好的取向性,Fourier红外吸收光谱表明:用甲醇醇解法合成的ZnO纳米晶体只含有很少的有机物杂质。室温PL光谱表明:ZnO纳米晶体在可见光范围内(400nm~650nm)有良好的发光性,掺入Al3+有助于改善ZnO纳米晶体的发光特性。
1 MURRAY C B,NORRIS D J,BAWENDI M G:Synthesis and characterization of nearly monodisperse CdE (E=sulfur, selenium,tellurium)semiconductor nanocrystallites.J.Am. Chem.Soc.,1993,115:8706~8715
2 OZIN G A.Nanochemistry:synthesisin diminishing dimensions.Adv.Mater.,1992,4:612-649.
3 Markovich G,Collier C P,Henrichs S E.Architectonic quantum dot solids.Acc.Chem.Res.,1999,32:415~423
4 WU C L,QIAO X L,CHEN J G.Controllable ZnO morphology via simple template-free solution route.Mater. Chem.Phys.,2007,102:7~12
5 GUO M,DIAO P,CAI S.Hydrothermal growth of well-aligned ZnO nanorod arrays:dependence of morphology and alignment ordering upon preparing conditions.J.Solid State Chem.,2005, 178:1864~1873
6 PETERSONRB,FIELDSCL,GREGGBA.Epitaxialchemical deposition ofZnO nanocolumnsfrom NaOH solutions. Langmuir,2004,20:5114~5118
