2,5-二羟基对苯二甲酸结构与性能表征
2011-01-22
(中国兵器工业集团第五三研究所,济南 250031)
聚[2,5-二羟基-1,4-苯撑吡啶并二咪唑]{Poly[2,6-diimidazo(4,5-b:4’,5’-e)pyridinylene-1,4(2,5-dihydroxy)phenylene],PIPD}(纤维商品名为M5),是由荷兰阿克苏诺贝尔研究所发明的一种新型液晶刚棒性聚合物[1-6],其独特的双向氢键网络结构使聚合物的压缩性能得到显著提高,弥补了一度被誉为“纤维之王”的聚苯撑苯并双恶唑(PBO)的不足,而2,5-二羟基对苯二甲酸(2,5-Dihydroxyterephthalicacid,DHTA)正是为此氢键网络结构提供大量—OH的重要聚合单体之一;2,5-二羟基对苯二甲酸还是重要的有机合成中间体,可用于生产着色剂和溶解度高的有机发光聚合物。Kolbe-Schmitt反应[7]是目前合成一定类型的芳香族羟基酸最经典的方法,是用高压CO2处理对苯二酚的盐发生羧基取代,还可以通过二羟基对苯二甲酸二甲酯水解得到。目前,国内对2,5-二羟基对苯二甲酸的研究报道为数不多[8-11],没有工业化产品,甚至没有市售商品,鲜见有关结构与性能的表征技术报道。
笔者对于本实验室采用新方法合成的DHTA,分别采用紫外光谱(UV)、傅立叶变换红外光谱(FT-IR)、质谱(MS)、核磁共振(NMR)和热分析红外光谱联用(STA-FTIR)等结构确证方法对DHTA进行结构和热性能的表征研究。
1 实验部分
1.1 主要仪器与试剂
紫外光谱仪:Lambda 900UV/VIS/NIR型,美国Perkin Elmer公司;
傅立叶变换红外光谱仪:Magna 750型,美国Nicolet公司;
核磁共振波谱仪:INOVA-300型,美国Varian公司;
质谱仪:Finnigan LCQ型,美国热电公司;
热分析红外光谱联用仪:STA 6000 (DTA/TG)-FTIR型,美国Perkin Elmer公司;
2,5-二羟基对苯二甲酸(DHTA):自制。
1.2 分析条件
(1)紫外光谱分析 采用甲醇作为溶剂,样品浓度为24 μg/mL,1 cm石英吸收池,狭缝宽度为2.0 nm,波长范围为200~400 nm。
(2)红外光谱分析 采用KBr压片制样方法,波数范围为400~4 000 cm-1,增益为1,样品扫描次数为8次,分辨率为4 cm-1。
(3)核磁共振谱分析 以二甲基亚砜(DMSO)为溶剂,四甲基硅烷(TMS)为内标。1H谱工作频率为300 MHz,采样时间为2 s,延迟时间为8 s;13C谱工作频率为75.42 MHz,采样时间为0.5 s,延迟时间为1 s。
(4)质谱分析 采用电喷雾负离子电离模式,即ESI(-),电压为3 000 V,流速为5 μg/L。
(5)热分析红外光谱联用分析 温度范围为30~500℃,升温速率为10℃/min,采用N2作为保护气,气体流速为20 mL/min,FTIR分辨率为4 cm-1。
2 结果与讨论
2.1 紫外光谱
图1为2,5-二羟基对苯二甲酸在甲醇溶剂中测定的紫外吸收光谱图。图1中依次得到各吸收带:λmax218.22 nm(εmax12 000)、249.43 nm(εmax5 100)及364.62 nm(εmax2 400)等(各波长数字后面的括号内为该峰的强度)。
芳香族有机化合物通常有3个吸收带,依次为E1、E2和B带。E1带是由苯环内乙烯键上的л电子被激发所致,在本结构中对应是218 nm峰位。E2带是由苯环的共轭二烯所引起,该化合物结构中助色团—OH的引入,与苯环形成p-л共轭,使吸收带红移;发色团—COOH的л电子与苯环上的л电子形成л-л共轭,相连产生更大的共轭体系,吸收峰更加显著地红移,吸收强度也显著增加;按Scott规则[12]计算此吸收带λmax为244 nm,与实测值249.43 nm基本一致。B带是苯环的特征吸收,此带为一宽峰,并具有精细结构,在甲醇等极性溶剂中这些精细结构变得不明显或消失,B带呈宽的峰包状。

图1 DHTA紫外吸收谱图
2.2 红外光谱

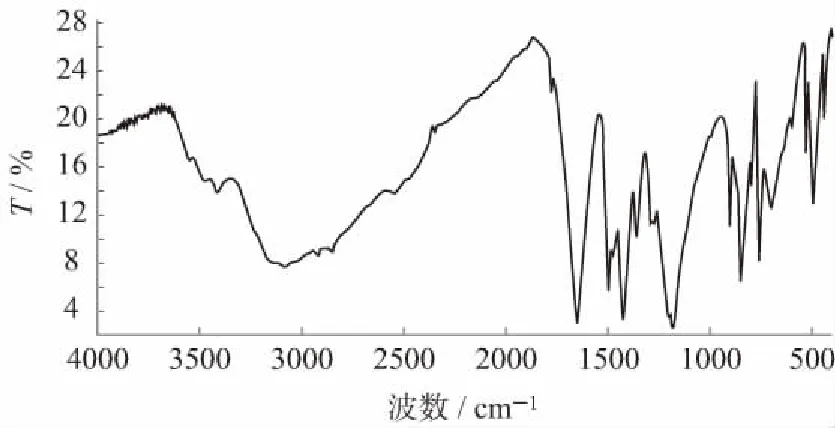
图2 DHTA红外吸收谱图

吸收峰/cm-1归属3300~2500宽峰缔合OH伸缩振动1649CO伸缩振动1497苯环骨架振动1427OH面内弯曲振动1290、1180CO伸缩振动899、849四取代苯环CH弯曲振动699OH面外弯曲振动
2.3 核磁共振谱
DHTA的结构式见图3。图4、图5为DHTA的1H谱和13C谱。文献[3]中给出的NMR(DMSO-d6):δ1H 7.33,δ13C 117.7、119.4、152.5、170.7,与本实验数据:δ1H 7.29,δ13C 117.25、119.23、151.92、170.26非常吻合。结合其结构式可以确定DHTA有4种不同类型的碳,羰基碳的化学位移值在δ160~220范围,很明显δ170.26对应结构式1位碳。取代苯以苯的δC 128.5为基值,δC值在δ100~160范围,即结构式中2,3,4位碳,如果苯环上的氢被其他基团取代,被取代的碳原子δC值有明显变化,一般对于多取代苯的δC值,可以根据经验公式(1)进行计算[12]。
δC(K)=128.5+ΣAi
(1)
式中:δC(K)——苯环碳的δC值;
K——碳原子编号;
Ai——取代基对苯环碳的取代参数。
由(1)式计算得,δC(2)为124.4,实测值为119.23;δC(3)为149.6,实测值为151.92;δC(4)为118.7,实测值117.25。由于取代基—OH与—COOH之间的综合影响,导致计算结果与实测值之间会有一些误差。

图3 DHTA的结构式

图4 DHTA的1H谱

图5 DHTA的13C谱
2.4 质谱
图6是DHTA的串联质谱图。采用ESI(-)模式形成准分子离子[M-H]-,即图6中m/z197.1(M-1),另外芳香酸的谱图有明显的M-18(失去水)和M-44(失去CO2)的特征碎片离子峰,总结主要裂解过程如图7。


图6 DHTA的串联质谱图

图7 DHTA裂解过程
2.5 热分析红外光谱联用
用STA(DTA/TG)-FTIR在氮气中测试DHTA的热分解过程,图8为DHTA的DTA-TG曲线。从TG曲线看,该物质只有一明显的失重台阶,246℃开始失重,308℃失重加快,随温度升高,失重进一步加快,而对应DTA曲线在258、341℃出现两个吸热峰,并且在此温度区间一直是一个吸热过程。

图8 DHTA的DTA-TG曲线
同步FTIR实验测试分别记录了258℃和341℃的挥发物情况,如图9所示,曲线1为仪器基线,曲线2为341℃挥发物,根据红外数据库谱图确定曲线2是CO2光谱图。结合DTA曲线在此位置的吸热峰,可以证明DHTA在341℃发生分解。

图9 258℃(曲线1)和341℃(曲线2)挥发物的红外谱图
从图8可以看出,在DTA曲线出现分解吸热峰之前,TG曲线显示该物质已经明显失重55%以上,为了进一步解释这一失重现象,用STA-FTIR在氮气中测试DHTA在30~330℃范围的热分析状况,DTA-TG如图10所示。在程序升温过程中,设定升温速率为20℃/min,并分别在样品温度为263、291、330℃恒温10 min。同步FTIR实验未检测到CO2,通过红外光谱检测失重过程中坩埚内剩余物质为DHTA,说明在该温度范围内,物质发生了吸热升华现象,进而失重。

图10 DHTA在30~330℃的DTA-TG曲线
3 结论
通过UV、FT-IR、MS、1H-NMR、13C-NMR和STA-FTIR等方法对自制的DHTA进行了结构和热性能表征技术研究。FT-IR、NMR、MS是化合物结构表征的有效手段,三者结合起来对其分子结构进行了较全面的分析,STA-FTIR直观地反映了DHTA的热分解过程,为其热性能研究提供更准确的信息。本研究结果为高纯度、高产率聚合级单体的商品化奠定了理论基础,为工业化推广提供新的支持,并有利于PIPD聚合物及M5纤维的发展与应用。
[1] Wolfe J F,Arnoid F E.Rigid-rod polymers:l synthesis and thermal properties of para-aromatic polymers with 2,6-benzobisthiazole units in the mainchain[J].Macromolecules,1981,14(4):909.
[2] 卢晓东,黄玉东.聚(二羟基苯撑并吡啶双咪唑)的单体合成及表征[D].哈尔滨:哈尔滨工业大学,2004.
[3] Sikkema D J.Design,synethesis and properties of a novel rigid rod polymer PIPD or‘M 5’:high modulus and tenacity fibers with substantial compressive strength[J].Polymer,1998,39:5 981-5 986.
[4] 任鹏刚,梁国正,卢婷利,等.高性能有机纤维-‘M5’的制备研究 [J].化工新型材料,2003,31(8):22-24.
[5] 李霞,曹海林,李国学,等.高性能M5纤维的研究现状[J].高科技纤维与应用,2007,32(2):35-39.
[6] 张清华,李兰,陈大俊.一种新型的刚性高性能纤维M5 [J].高科技纤维与应用,2004,29(6):35-38.
[7] Sikkema D J.Process for Dicarboxylating Dihydric Phenols:美国,6040478[P].2000-03-21.
[8] 漆琳,沈玉堂,殷恒波,等.2,5-二羟基对苯二甲酸的合成及表征 [J].合成纤维,2007(1):23-25.
[9] 沈玉堂,漆琳,殷恒波,等.一种制备2,5-二羟基对苯二甲酸的方法:中国,200910030215[P].2009-08-19.
[10] 孙硕,黄玉东,林宏,等.2,5-二羟基对苯二甲酸的合成研究 [J].化学与黏合,2007,29(6):413-415.
[11] 王艳红,黄玉东,宋元军,等.聚[2,5-二羟基-1,4-苯撑吡啶并二咪唑]单体的合成优化及提纯研究[J].固体火箭技术,2009,32(6):698-705.
[12] 朱淮武.有机分子结构波谱解析[M].北京:化学工业出版社,2005:12-165.
