乙醇胺为碱性催化剂对硅气凝胶性能的影响*
2011-01-22,,
,,
(1.新疆大学化学化工学院,新疆乌鲁木齐 830046;2.新疆乌鲁木齐市气象局)
二氧化硅气凝胶具有高比表面积、高孔隙率、低密度、低热导率、极低介电系数和低折射系数的特殊性能,同时绿色环保,在热学、光学、化工等方面具有广泛的商业应用价值。制备硅气凝胶硅源一般采用正硅酸四乙酯(TEOS),酸催化剂一般采用HF、盐酸、乙酸、草酸[1]等,碱性催化剂通常采用氨水。干燥方法为超临界干燥法和常压干燥法。常压干燥法是今后的发展方向,但表面改性剂的使用条件较为苛刻[2]。S.Yoda等以乙醇胺为催化剂,直接加入到正硅酸四甲酯(TMOS)中,使TMOS凝胶,结果表明乙醇胺的加入对胶凝时间、收缩率、孔隙率等均有影响[3]。F.Carre等认为醇胺直接与硅烷中的硅发生配位反应,硅醇的—OR基团阻止了水解反应[4]。直到目前,硅气凝胶仍不具有商业价值,主要是受到硅源和表面改性剂高昂价格的限制[5]。乙醇胺同时具有胺基和羟基结构,其对气凝胶的合成有影响。笔者以盐酸为酸催化剂,分别以一乙醇胺(MEA)、二乙醇胺(DEA)、三乙醇胺(TEA)为碱性催化剂,并与氨水作比较,采用溶胶-凝胶法合成湿凝胶,不经过表面改性,采用真空干燥得到二氧化硅气凝胶。通过对所得气凝胶的结构特征进行表征,表明乙醇胺为碱性催化剂具有不同于氨水的性质。
1 实验
1.1 SiO2气凝胶的制备
以TEOS、蒸馏水为原料,无水乙醇(EtOH)为溶剂,盐酸为酸催化剂,乙醇胺(MEA、DEA、TEA)、氨水为碱催化剂,采用酸碱两步催化溶胶-凝胶共前驱体法制备二氧化硅湿凝胶。通过对主要合成参数的优化,得到TEOS、EtOH、水物质的量比为1∶4∶4。加入盐酸(5.3×10-3mol)、碱性催化剂[MEA、DEA、TEA、氨水,(7.6~85)×10-3mol]进行凝胶聚合反应。将凝胶置于60 ℃水浴中老化,期间加入无水乙醇置换原溶剂,每隔24 h替换一次无水乙醇,老化总时间为3~4 d。将湿凝胶在真空条件下采用分段升温方式每隔5 ℃从40 ℃升温至70 ℃进行干燥,得到干燥SiO2气凝胶。
1.2 SiO2气凝胶的表征
使用精度为0.000 1 g的电子天平称量已知体积的气凝胶质量,根据下式估算孔隙率:
孔隙率=(1-ρp/ρs)×100%
(1)
式中:ρp为气凝胶表观密度,g/cm3;ρs为SiO2理论密度,2.2 g/cm3。
采用德国BRUKER公司的EQUINOX型傅里叶变换红外光谱仪对样品进行红外光谱测试;采用德国LEO公司的LEO1430VP型环境扫描电子显微镜观察SiO2气凝胶的微观形貌和孔隙结构;采用中国产JW-BK型静态氮吸附仪,采集脱吸附曲线数据并利用BET原理计算气凝胶的比表面积;采用BJH计算方法求得气凝胶的孔径分布和平均孔径,测试前样品先在105 ℃热处理2 h,测试温度为-195.8 ℃。
2 结果与讨论
2.1 SiO2气凝胶吸附性能比较
根据BET方程:
p/[V(po-p)]=1/(VmC)+(C-1)p/(VmCpo)
(2)
C≈exp[(Q1-QL)/(RT)]
(3)
式中:V为单位质量样品表面氮气吸附量;Vm为单位质量样品表面单分子层氮气饱和吸附量;po为在液氮温度下氮气的饱和蒸气压;p为测定吸附量时氮气分压;C为与材料吸附特性相关的常数,由吸附仪直接计算给出;Q1为第一层的吸附热;QL为吸附质的液化热。
根据C的物理意义可知,C值越大表示固体材料内表面吸附能力越强,吸附层数越多。若C>1,表示吸附剂与吸附质分子之间的吸引力大于吸附质为液体时分子之间的引力[6]。
根据多次对比试验,添加不同浓度的MEA、DEA、TEA溶液为碱性催化剂,可得到不同效果的硅气凝胶。试验选择乙醇胺水溶液浓度分别为:MEA,1∶20;DEA,1∶5;TEA,1∶5(均为体积比)。
分别将MEA、DEA、TEA溶液和氨水按照不同的加入量加入到TEOS水解液中,凝胶置换溶剂后不经表面改性,采用真空干燥得到SiO2气凝胶。测试比表面积,得到相应的C值。碱催化剂添加量与C值的关系见表1。由表1可知:当碱催化剂添加量为7.6×10-3mol时,TEA的C值最大,MEA的C值次之,约为TEA的C值的1/2;当碱性催化剂添加量增加到8.5×10-2mol时,TEA的C值降到最低值;对于MEA和DEA,当其添加量由7.6×10-3mol增加到1.7×10-2mol时,二者的C值降到最低,随后随着添加量的增加C值上升;氨水的C值随着氨水添加量的增加呈下降趋势。从表1还可以看出,MEA在添加量为(5.1~8.5)×10-2mol的较宽范围内,其C值比DEA、TEA和氨水的C值高,但在低添加量处TEA的效果最好,MEA和DEA的效果次之。说明MEA作为碱性催化剂的加入,有助于使气凝胶内表面的吸附能力增强,使吸附量增大,吸附更多层的分子,MEA的作用效果要优于DEA和氨水。该特性使气凝胶可能对于某些极性分子的吸附能力增强,有助于提高选择性吸附和吸附量。

表1 碱性催化剂添加量与硅气凝胶吸附参数C、比表面积的关系
由表1看出:在碱性催化剂低加入量处(7.6×10-3mol),以MEA为催化剂所得气凝胶的比表面积最大,为743.3 m2/g,是以氨水为催化剂的2.5倍,并且随着MEA添加量的增加,气凝胶比表面积逐步下降;而DEA和TEA具有相似的规律,在添加量为1.7×10-2mol处,气凝胶比表面积最大,然后随着催化剂添加量的增加,气凝胶比表面积下降;以氨水为催化剂的变化趋势与前面不同,在添加量为7.6×10-3mol处气凝胶比表面积最小,在添加量为1.7×10-2mol时气凝胶比表面积最大,然后随着添加量的增加比表面积逐步下降,但下降幅度不大。究其原因主要是,在相同添加量下乙醇胺水溶液的碱性高于氨水,碱性过强易使局部形成的凝胶颗粒快速缩聚,形成的骨架颗粒粗大,孔径较大,进而使比表面积减小。
2.2 N2吸附-脱附等温曲线的特征
图1为MEA、DEA、TEA和氨水添加量为7.6×10-3mol时所得SiO2气凝胶典型N2吸附-脱附等温线。从图1看出,DEA为催化剂的吸附等温线为I型等温线,其余的吸附等温线为II型等温线。I型等温线是单分子吸附层曲线,随着相对压力的不断提高,发生毛细管凝聚,使吸附量增加,一旦将所有的微孔填满后,吸附量便不会随着相对压力的提高而增加,呈现出吸附饱和。对于以MEA、TEA和氨水溶液为催化剂的II型吸附等温线,吸附分支变化缓慢,而脱附分支在中等大小相对压力处有一陡的变化,具有细颈和墨水瓶形状的孔可以有此类吸附回线。在吸附分支上,当相对压力增至与瓶颈半径相对应的值时,凝聚液便开始充满瓶颈,随着相对压力继续增加,连续地充满整个墨水瓶体。所以,吸附分支是逐渐变化的。在脱附分支上,由于瓶颈上的液体将广体中的液体封住了,一直到相对压力降至与瓶颈对应的值时便发生骤然的脱附至空[6]。比较乙醇胺硅气凝胶的吸附-脱附曲线,在相对压力大于0.53时TEA的吸附线要高出MEA、DEA和氨水较多,说明其吸附能力要高于MEA和DEA,这与TEA的C值较MEA和DEA的C值高有相同的规律。而在相对压力低于0.53时,氨水的吸附-脱附曲线稍高于其他吸附-脱附曲线。从图1还可以看出,TEA、MEA和氨水为催化剂硅气凝胶孔径分布有一定的范围,而DEA为催化剂的硅气凝胶孔径分布较为均匀。
图2为MEA、DEA、TEA、氨水添加量为7.6×10-3mol所得SiO2气凝胶吸附孔径分布图。由图2可知,以氨水和TEA为碱性催化剂时所得二氧化硅气凝胶孔径最小,最高峰位于1.7 nm;DEA为1.93 nm;MEA最大,为2.18 nm,是氨水的1.28倍。这说明,MEA能够形成较大的孔径,孔径的适当增大有利于降低溶剂挥发时的界面张力,减少了孔的收缩和坍塌。从孔径分布的幅度来看,TEA波峰的宽度最大,而氨水的最小,说明以TEA为碱性催化剂所得的气凝胶孔径分布范围较广,这主要与TEA多羟基和SiO2表面羟基形成氢键影响了孔结构有关,而氨水的则比较单一。DEA也可得到孔径分布较窄的硅气凝胶。

图1不同碱性催化剂的吸脱附曲线图2不同碱催化剂的孔径分布图
表2为碱性催化剂添加量与硅气凝胶平均孔径、孔隙率的关系。由表2看出:随着MEA添加量的增加,孔径的变化呈抛物线状,在添加量为5.1×10-2mol时出现最大值,添加量再增大则孔径下降幅度较大;随着TEA添加量的增加,孔径呈逐渐增大趋势,当添加量达到5.1×10-2mol之后,孔径增大不明显,其最大值低于MEA;氨水和DEA的变化规律相似,随着添加量的增加,平均孔径增加。究其原因主要是MEA溶液碱性过强,添加量超过一定量,易使凝胶颗粒发生粘连,使孔径变小。从表2看出:随着MEA、DEA添加量的增加,孔隙率呈增加的趋势,但添加量超过5.1×10-2mol后孔隙率增加不明显;而氨水则在其添加量为1.7×10-2mol 后,孔隙率有较大的上升幅度;随着TEA添加量的增加,孔隙率在出现峰值后则出现下降趋势。表2数据说明,以乙醇胺作为催化剂,在低添加量时所得硅气凝胶的孔隙率高于氨水作催化剂的孔隙率。
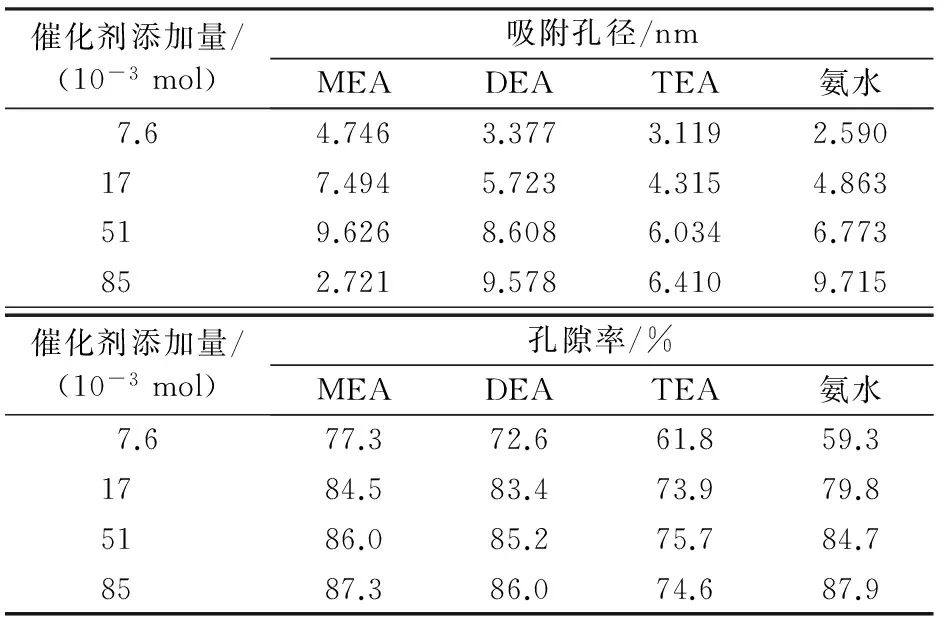
表2 碱催化剂添加量与硅气凝胶吸附孔径、孔隙率的关系
2.3 表面形貌和微观结构
图3为分别加入MEA、DEA和TEA所得SiO2气凝胶的扫描电镜照片,MEA添加量为7.6×10-3mol,DEA、TEA添加量为1.7×10-2mol。从图3看出,所用碱性催化剂不同,SiO2气凝胶的微观结构不同。图3a中SiO2呈颗粒状,几个颗粒互相粘连形成小团,团与团之间鳞次栉比,中间有小孔隙存在。图3b中SiO2部分呈现正四面体颗粒状,其余则是很小的颗粒,形成网状结构。图3c与图3a样品形状相似,但是出现较多的“粘连”,形成团聚现象,使其比表面积、孔隙率下降。分析其原因可能是由于TEA具有3个羟基,氢与硅气凝胶表面羟基中的氧形成氢键,从而使一分子的TEA可“拉住”3个凝胶颗粒,发展开来,则更易形成粘连现象。而MEA和DEA羟基少,形成的凝胶颗粒较分散。

图3 SiO2气凝胶SEM照片
2.4 表面特性
通过N2吸附等温线可检测出不同碱性催化剂对SiO2气凝胶内部表面不规则结构形状的影响。将不同添加量下所得样品的p0/p取对数后,与V/Vm作图得到直线,计算出斜率m,根据文献[7],斜率表示了吸收毛细管冷凝的机制。根据公式Ds=3-|1/m|计算出Ds(表面不规则数),Ds越大表明其内表面越粗糙。将不同碱催化剂添加量下的Ds作图,见图4。由图4看出,TEA的Ds除了在第一个点低于氨水,其余的点始终在其他线的上方,说明以TEA为碱性催化剂得到的硅气凝胶相对于其他碱催化剂其内部较粗糙。
图5为添加不同碱性催化剂制备的SiO2气凝胶的红外吸收光谱。其中460、800[8]、1 080、1 650 cm-1[9]附近的吸收峰是Si—O—Si的振动吸收峰;3 466 cm-1附近的吸收峰代表O—H的吸收带,是物理吸附水产生的,这些峰是SiO2气凝胶的典型峰。960 cm-1是Si—OH 的伸缩振动,二乙醇胺的峰值较弱,可认为该样品中具有较少的羟基基团。2 970 cm-1和930 cm-1[10]附近的吸收峰为—CH3的不对称振动和摇摆振动,说明在表面出现了硅甲基,图5中MEA在该处的振动强度明显增强,而DEA的则相对弱很多。对于氨水,在2 970 cm-1处无峰出现。该峰常出现于使用三甲基氯硅烷(TMCS)表面改性剂进行表面处理的硅气凝胶,即TMCS中的—C2H5基团挂在了湿凝胶的表面[11]。但本研究中并未使用TMCS等表面改性剂,那么这个峰可能是Si—O—C2H5的对称伸缩振动,这也导致了谱图在2 970 cm-1处出现了C—H键的对称和不对称伸缩振动特征峰[12],该峰还显示了SiO2气凝胶具有一定的疏水性能。—O—C2H5基团只能来自于TEOS中,MEA能促使TEOS的水解反应朝逆向进行,增强了硅气凝胶的疏水性。

图4碱催化剂添加量与Ds关系图图5不同碱催化剂制备SiO2气凝胶红外光谱图
3 结论
1)以TEOS为硅源,采用酸/碱催化法,使用不同体积比乙醇胺溶液作为碱性催化剂,在不同添加量下,可得到孔隙率为61.8%~87.3%、平均孔径为2.7~9.6 nm的硅气凝胶。在低添加量时,乙醇胺作催化剂所得硅气凝胶的孔隙率高于氨水,平均孔径大于氨水;2) 使用TEA作碱性催化剂,在添加量为7.6×10-3mol时,其C值明显高于氨水的C值,可提高N2吸附量;3)加入TEA所得SiO2气凝胶,其内表面较加入氨水的粗糙,使吸附能力增强;4)使用MEA作碱性催化剂,可使SiO2气凝胶具有一定的疏水性。
[1] 张伟娜,李云辉,王庆伟,等.二氧化硅气凝胶的表面改性及热稳定性的研究[J].吉林师范大学学报:自然科学版,2009,37(2):67-69.
[2] Woignier T,Phalippou J,Vacher R.Parameters affecting elastic properties of silica aerogels[J].J.Mater.Res.,1989,4(3):668-692.
[3] Yoda S,Ohshima S,Kamiya K.et al.Effects of ethanolamines catalysts on properties and microstructures of silica aerogels[J].J.Non-Cryst.Solids,1996,208(1/2):191-198.
[4] Carre F,Cerveau G,Chuit C,et al.Hexacoordination at silicon: the case of silatranes[J].Organometallics,1990,9(7):1989-1991.
[5] Nakanishi K,Minakuchi H,Soga N,et al.Structure design of double-pore silica and its application to HPLC[J].J.Sol-Gel Sci.Technol.,1998,13(1/2/3):163-169.
[6] 沈钟,王果庭.胶体与表面化学[M].北京:化学工业出版社,2004:147-308.
[7] Pfeifer P,Cole M W.Fractals in surface science:scattering and thermodynamics of adsorbed films II[J].New J.Chem.,1990,14(3):221-232.
[8] 何方,赵红雨,徐三魁.硅石气凝胶老化的新方法[J].河南化工,2008,25(8):19-20.
[9] 史非,王立久,刘敬肖,等.介孔SiO2气凝胶的常压干燥制备研究[J].无机化学学报,2005,21(11):1632-1636.
[10] 张志华,倪星元,沈军,等.SiO2气凝胶表面特性对其吸附性能的影响[J].材料导报,2005,19(7):115-117.
[11] 王娟,张长瑞,冯坚.三甲基氯硅烷对纳米多孔二氧化硅薄膜的修饰[J].物理化学学报,2004,20(12):1399-1403.
[12] 吴国友,余煜玺,程璇,等.甲基三甲氧基硅烷对块状SiO2气凝胶性能和结构的影响[J].硅酸盐学报,2009,37(7):1206-1211.
