两亲无规聚合物的聚集行为及其与非离子表面活性剂的相互作用
2010-11-30乔英杰胡长朝王金本
吴 旭 乔英杰 胡长朝 杨 惠 王金本,*
(1哈尔滨工程大学材料科学与化学工程学院,哈尔滨 150001;
2中国科学院化学研究所,胶体、界面与化学热力学院重点实验室,北京 100190)
两亲无规聚合物的聚集行为及其与非离子表面活性剂的相互作用
吴 旭1,2乔英杰1胡长朝2杨 惠1,2王金本2,*
(1哈尔滨工程大学材料科学与化学工程学院,哈尔滨 150001;
2中国科学院化学研究所,胶体、界面与化学热力学院重点实验室,北京 100190)
以2-丙烯酰胺基-十二烷基磺酸(AMC12S)与2-丙烯酰胺基-2-甲基丙磺酸(AMPS)进行无规共聚,合成了含AMC12S摩尔分数(X)较高(X=0.1,0.3,0.5)的一系列两亲聚合物.采用稳态荧光及动态光散射技术对聚合物在水溶液中的聚集行为及其与三种非离子表面活性剂(HO(CH2CH2O)10C12H25(C12E10)、HO(CH2CH2O)20C12H25(C12E20)和HO(CH2CH2O)40C12H25(C12E40))的相互作用进行了研究,并考察了X对聚集行为的影响以及表面活性剂亲水基团长度对相互作用的影响.随着X的增大,聚合物的临界聚集浓度(CAC)明显减小,X=0.5时聚合物的CAC低达0.0039 g·L-1.聚集体的流体力学半径(Rh)都大于26 nm,并随着聚合物浓度的升高而增大,说明聚合物分子主要以分子间的聚集方式聚集,形成多分子聚集体.随X的增大,聚集体Rh减小,同时Rh随聚合物浓度升高而增大的幅度减小,说明聚集体结构变得更加紧实.表面活性剂与聚合物之间存在很强的相互作用,在混合溶液中表面活性剂浓度达到临界胶束浓度(CMC)左右时聚合物聚集体开始解离,形成混合聚集体.亲水基团长度增长,表面活性剂对聚合物聚集体的解离能力随之增强.C12E40与X=0.5的聚合物形成的混合聚集体Rh为6.8 nm,与C12E40自身形成的聚集体尺寸相当.
非离子表面活性剂;两亲聚合物;聚集行为;聚集体;相互作用
两亲聚合物以其独特的溶液性质,在矿物分离、三次采油、水处理、清洁用品、化妆品及食品业有着良好的应用前景[1-3].由于合成方法不同,两亲聚合物可分为嵌段和无规聚合物,其中无规聚合物的分子结构比较复杂,对其研究相对困难[4].然而,已经用于工业生产的两亲聚合物多是由不同物理、化学性质的单体通过无规共聚得到的,这就使对两亲无规聚合物溶液性质的研究更具实际意义.目前的研究表明,所用单体的种类[5-9]、聚合物的组成[8-13]、聚合度[13]、疏水基团与分子主链之间的连接基团[14-18]都是影响两亲无规聚合物性质的重要因素.聚合物分子可能形成分子内的聚集、分子间的聚集或者同时存在两种聚集.分子内聚集得到的聚集体为单聚体,溶液的粘度随浓度的增加没有明显增加;而分子间聚集得到多聚物或空间网状结构,溶液的粘度随浓度的增加而明显增加.我们实验室以较低含量的两亲单体,合成了一系列结构新颖、具有优良实用性能的无规聚合物[19-20].
虽然对两亲聚合物聚集行为的研究已成为相关领域的热点,但是关于含有高含量两亲单体聚合物的研究却未见报道.本文以2-丙烯酰胺基-十二烷基磺酸(AMC12S)(其摩尔分数X=0.1,0.3,0.5)为疏水基团,与2-丙烯酰胺基-2-甲基丙磺酸(AMPS)进行无规共聚,得到系列两亲聚合物(见图1).并研究了聚合物在水溶液中的聚集行为,探讨X对临界聚集浓度(CAC)、聚集体流体力学半径(Rh)及Rh随浓度的变化等性质的影响.合成三种非离子表面活性剂HO(CH2CH2O)10C12H25(C12E10)、HO(CH2CH2O)20C12H25(C12E20)和HO(CH2CH2O)40C12H25(C12E40),考察聚合物与表面活性剂之间的相互作用,并探讨表面活性剂亲水基团长度对相互作用的影响.
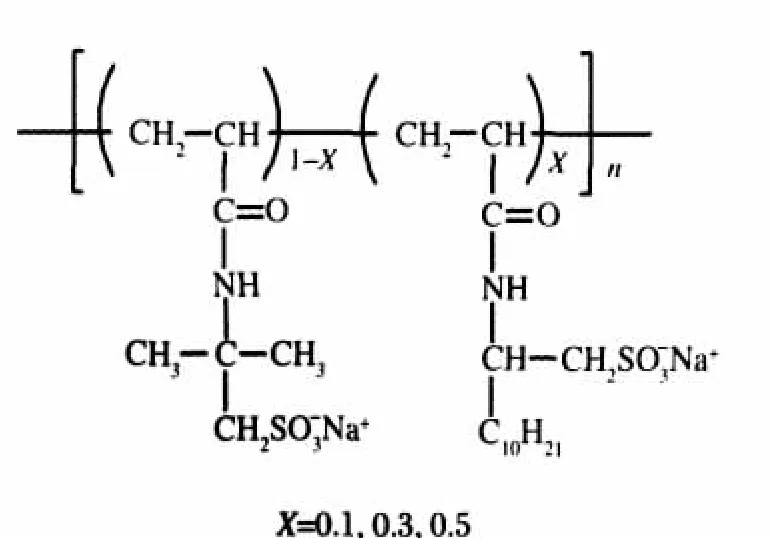
图1 聚合物的结构式Fig.1 Chemical structure of the polymers
1 实验部分
1.1 试剂、合成与表征
1.1.1 实验试剂
氯化钠、过硫酸铵、硫酸亚铁铵、丙烯腈、发烟硫酸、月桂醇、氢氧化钾、环氧乙烷、磷酸均为分析纯,购于北京试剂公司.十二碳烯纯度高于99%,购于美国Fluka公司.芘购于美国Aldrich公司,使用前在乙醇中重结晶.AMPS纯度高于99.4%,购于山东寿光市煜源化学有限公司.
1.1.2 AMC12S的合成与表征
AMC12S合成过程见文献[21].1H核磁共振(1H NMR)(400 MHz,D2O),δ:0.83-0.87(t,3H),1.25-1.30 (m,16H),1.53-1.58(m,1H),1.72-1.77(m,1H),3.09 (d,2H),4.31-4.34(m,1H),5.73-5.76(d,1H),6.15-6.28(m,2H).
1.1.3 聚合物的合成与表征
在50 mL广口瓶中加入0.025 mol的AMC12S (X=0.1、0.3、0.5)和AMPS.加水溶解单体,控制固体含量为25%(w,质量分数).通入氮气10 min,加入引发剂(7.02%(w)硫酸亚铁铵2.25 mL,5.88%(w)过硫酸铵2.25 mL),体系温度升至大约50℃.待体系温度降至室温后,将产物溶于NaOH的稀溶液中,并调节溶液pH值为7左右.用透析袋(北京欣惠泽奥科技有限公司,截流相对分子量为3500)将溶液在水中透析一周,冷冻干燥后得到白色固体样品.元素分析结果表明产物的碳氮比与投料单体碳氮比相符.
1.1.4 溶液的配制
将产物溶解于水中,并在剧烈搅拌下加热到90℃.定量加入NaCl调节溶液离子强度至0.05 mol· L-1后,在90℃下继续搅拌15 min.在高温剧烈搅拌下,聚合物分子在冷冻干燥过程中形成的相互缠绕可以完全打开,并以单分子的形式存在于溶液中.待溶液冷却至室温后,分子重新聚集形成原始的聚集形态[22].样品溶液在进行荧光和动态光散射测试之前均通过0.45 μm薄膜过滤器,并搅拌12 h使溶液达到平衡状态.
1.1.5 非离子表面活性剂的合成与表征
向反应釜中加入月桂醇18.6 g,KOH 0.213 g,并密封.用干燥N2驱替高压釜、进料釜以及进料管中的空气.加热升温,同时用真空泵抽真空,直到温度升为120℃.充N2至釜内压力为正压,加热至150℃时加入环氧乙烷44 g.反应在(165±5)℃,0.3-0.4 MPa下进行,直至釜内压力不再降低.在(155±5)℃下继续反应60 min后,用真空泵持续抽真空30 min.冷却,用磷酸中和后得到产物C12E10.C12E20和C12E40的合成路径与C12E10相同,反应时分别加入88和176 g的环氧乙烷.
C12E101H NMR(400 MHz,CDCl3),δ:0.83-0.86 (t,3H),1.23(s,18H),1.51-1.56(m,2H),3.40-3.46(m, 2H),3.52-3.70(m,41H).
C12E201H NMR(400 MHz,CDCl3),δ:0.85-0.88 (t,3H),1.24(s,18H),1.53-1.58(m,2H),3.41-3.47(m, 2H),3.55-3.72(m,81H).
C12E401H NMR(400 MHz,CDCl3),δ:0.85-0.87 (t,3H),1.24(s,18H),1.52-1.58(m,2H),3.41-3.47(m, 2H),3.55-3.72(m,161H).
1.2 测试方法
1.2.1 稳态荧光
使用配备温度调节装置的Hitachi F-4500荧光仪(日本Hitachi公司)对样品溶液的荧光强度进行测定,测试温度为(25.0±0.5)℃.激发波长设定为335 nm,狭缝宽度为2.5 nm.将1×10-3mol·L-1芘的乙醇溶液注入样品瓶中,自然挥发掉乙醇溶剂.将指定浓度的聚合物溶液注入样品瓶,荧光测试溶液芘的浓度保持在1×10-6mol·L-1.测试前溶液搅拌过夜,使溶液达到平衡.
1.2.2 动态光散射
使用配备有ALV-5000数字式时间相关器的ALV/SP-125激光光散射仪(德国ALV公司,氦-氖光源,波长632.8 nm)对样品溶液进行变角度(30°-90°)的测试,测试温度为(25.0±0.1)℃.散射向量(q)由公式q=(4πn/λ)·sin(θ/2)[23-24]得到,其中θ为散射角,n为溶液的折射率.扩散系数(D)通过逆拉普拉斯变换D=(Γ/q2)q→0[23-24]计算,其中Γ为弛豫率.流体力学半径(Rh)由Stokes-Einstein公式Rh=kBT/(6πηD)[23-24]计算,其中kB为Boltzmann常数,T为绝对温度,η为溶液粘度.
2 结果与讨论
荧光光谱可以反映芘探针所处微环境的极性,从而反映溶液中聚合物形成聚集体的情况[25].图2为不同浓度聚合物溶液的稳态荧光发射光谱,随着聚合物浓度的增加,谱图中峰3的强度(I3)相对于峰1的强度(I1)明显增加.图3为不同X的聚合物荧光发射谱图中I1/I3对浓度的曲线.聚合物浓度极稀时I1/I3值都在1.8左右,数值与分子芘在水中的I1/I3值(1.8)相符,说明该阶段聚合物以单分子形式存在于溶液中.随着聚合物浓度增大,I1/I3值都在临界聚集浓度(CAC)时迅速减小,说明分子芘所处微环境的极性在迅速减小,即芘开始溶解在聚合物形成的聚集体中.X值越大,I1/I3值减小所对应的浓度越小,即聚合物CAC越小(见表1).

图2 X=0.5的聚合物在不同浓度(CP)下芘的稳态荧光发射谱图Fig.2 Steady-state fluorescence emission spectra for pyrene in the presence of varying polymer concentrations(CP)with X=0.5

图3 I1/I3与聚合物浓度(CP)之间的关系Fig.3 Plots of I1/I3ratios as a function of polymer concentration(CP)

表1 聚合物的临界聚集浓度(CAC)以及在不同聚合物浓度(CP)下聚集体的流体力学半径(Rh)Table 1 Critical aggregation concentration(CAC)of the polymers and the hydrodynamic sizes of the aggregates(Rh)at various polymer concentrations(CP)
动态光散射测试中驰豫率(驰豫时间的倒数)是关于散射角的函数,随着散射角度的增加,分子内的运动会影响驰豫率.文中聚合物驰豫率与散射向量平方随着散射角的变化都呈线性关系,说明该体系符合分散模型[23-24],允许我们计算出D,进而利用Stokes-Einstein公式计算出Rh(见表1).
图4为不同X的聚合物在不同浓度下弛豫时间的分布情况,相应Rh见表1.X=0.5的聚合物在浓度为0.2 g·L-1时Rh=26.6 nm,在聚合物浓度为1.0 g·L-1时Rh=34.3 nm,聚集体的尺寸增加较小.X=0.3的聚合物浓度从0.2 g·L-1增大到1.0 g·L-1,Rh从26.9 nm增大到43.1 nm.X=0.1的聚集体尺寸增大最为明显,Rh从聚合物浓度为0.2 g·L-1的34.3 nm增大到浓度为1.0 g·L-1的69.1 nm.聚集体尺寸的大小以及尺寸随浓度增大而增大的性质说明聚合物分子以分子间聚集为主要形式,形成多分子的聚集体.X增大,聚集体尺寸减小,同时尺寸随聚合物浓度升高的增大幅度减小.由此可以推断出聚集体的紧实性随着X的增大得以增强,原因可能是聚合物中疏水基团含量增加,亲水基团含量减小,使疏水缔合作用增强而电荷之间的排斥作用相对减弱,导致聚集体的内部结构更为紧实.


图5 I1/I3与表面活性剂浓度(CS)之间的关系Fig.5 Plots of I1/I3ratios as a function of surfactant concentration(CS)

图6 I1/I3与聚合物溶液中表面活性剂浓度之间的关系Fig.6 Plots of I1/I3ratios as a function of theconcentration of surfactants in the polymer solution X=0.5,CP=0.2 g·L-1
图5为三种非离子表面活性剂荧光发射光谱中I1/I3对表面活性剂浓度的曲线,随着非离子表面活性剂中亲水基团长度的增长,临界胶束浓度(CMC)明显增大.三种表面活性剂C12E10、C12E20、C12E40的CMC分别为0.0550、0.1279、0.1695 g·L-1.
两亲聚合物与非离子表面活性剂相互作用,可使溶液中聚合物聚集体解离,形成聚合物与表面活性剂的混合聚集体[25-28].图6为X=0.5,浓度为0.2 g·L-1的聚合物溶液中,I1/I3值对三种表面活性剂浓度的曲线,I1/I3值都呈先增大,持续某一值后再减小的变化趋势.表面活性剂浓度增加到CMC左右时, I1/I3值明显增大,说明溶液中聚集体极性开始明显增大.聚合物与表面活性剂分子相互作用的增强导致聚合物分子间作用的减弱,使部分多分子聚集体开始解离.随着表面活性剂的加入,I1/I3值不变,此阶段可能由于溶液中已不存在可解离的多分子聚集体,使新增表面活性剂主要以游离状态存在于溶液中,浓度的增大对微观极性影响不大.表面活性剂浓度继续增大,新增表面活性剂自身开始聚集形成聚集体,使溶液中聚集体数目增多,整体微观极性减小,I1/I3值继续减小.

图7 不同表面活性剂及其与聚合物的混合溶液在散射角θ=90°时的弛豫时间分布Fig.7 Distributions of relaxation time measured at dispersion angle θ=90°for the different surfactant solutions and the mixed solutions of surfactants and polymerCS=5.0 g·L-1,X=0.5,CP=0.2 g·L-1
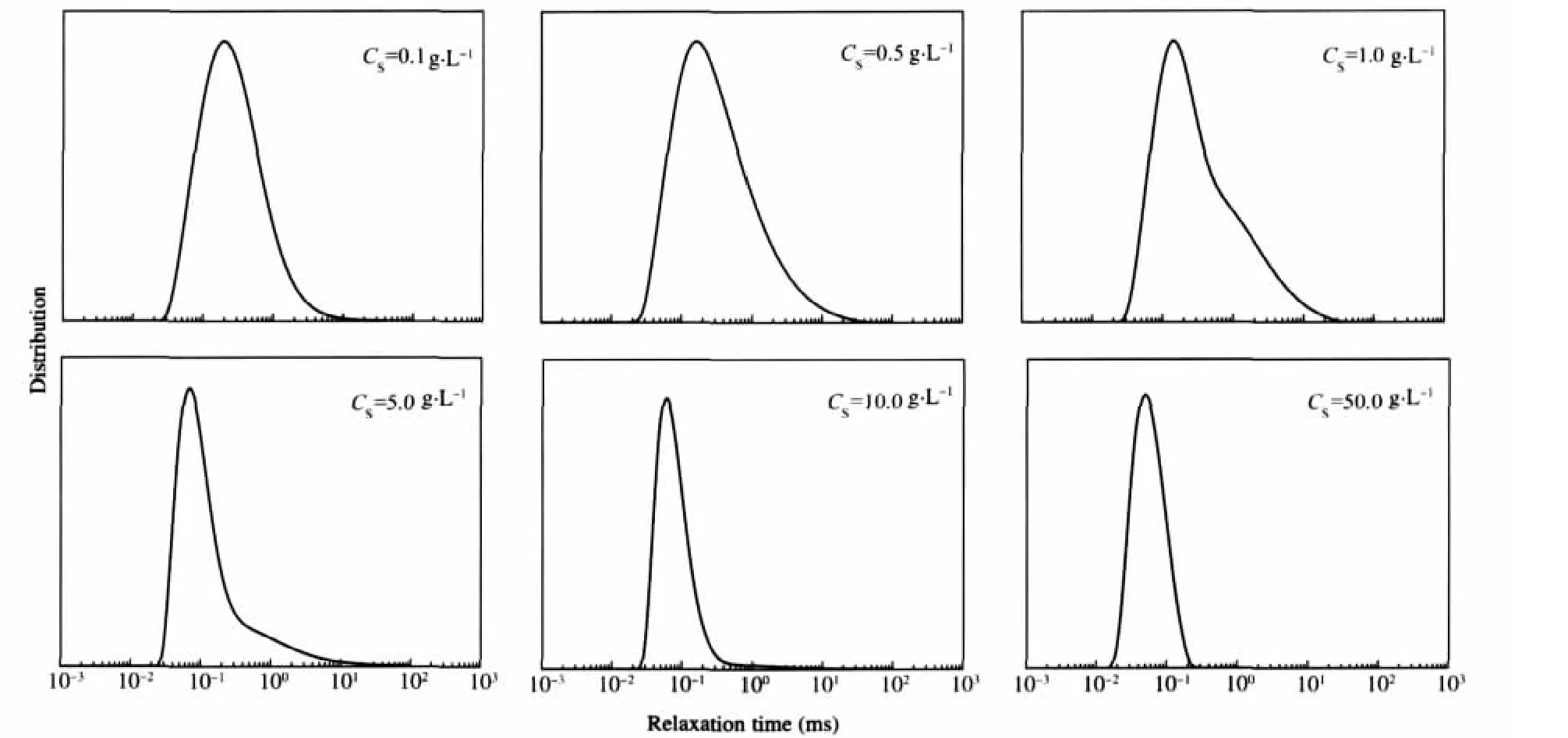
图8 含有不同C12E40浓度的聚合物溶液在θ=90°时的弛豫时间分布Fig.8 Distributions of relaxation time measured at θ=90°for the polymer solutions in the presence of C12E40at different concentrationsX=0.5,CP=0.2 g·L-1
根据图6中I1/I3值平稳阶段取表面活性剂浓度5.0 g·L-1,考察表面活性剂溶液及其与聚合物混合溶液弛豫时间分布情况如图7所示.从图7中混合溶液弛豫时间的峰型可以看出,表面活性剂亲水基团越长,混合溶液中大尺寸的聚集体含量越少,说明表面活性剂对聚合物聚集体的解离能力随着亲水基团长度的增长而增大.原因可能是参与到聚集体中表面活性剂分子亲水基团越长,空间位阻越大,使疏水缔合的聚合物碳链之间更容易分离.溶液中仍存在大尺寸的聚集体,而此时荧光谱图中I1/I3值随表面活性剂浓度增大变化不大可能是因为少量聚合物聚集体的解离对体系微观极性影响不大.
图8为随C12E40浓度增加,混合溶液弛豫时间分布情况.C12E40浓度为1.0 g·L-1时,弛豫时间的分布明显变窄,大尺寸的聚集体开始减少,说明此时部分聚合物聚集体开始解离.当C12E40浓度增加到10.0 g·L-1,体系中不存在大尺寸的聚合物聚集体,此时Rh大体反映了聚合物与C12E40形成混合聚集体的尺寸,经计算Rh为6.8 nm.当C12E40浓度增大到50.0 g·L-1时,相比10.0 g·L-1时弛豫时间并无明显变化,Rh为4.7 nm,说明混合聚集体与C12E40自身形成的聚集体尺寸相当.
3 结论
以AMC12S与AMPS通过无规共聚合成了系列两亲聚合物,其中AMC12S摩尔分数X=0.1、0.3、0.5.随着X的增加,聚合物CAC明显减小.X=0.5的聚合物CAC低达0.0039 g·L-1.聚合物浓度0.2 g·L-1时,聚集体的流体力学半径都大于26 nm,并随浓度的升高而增大,说明聚合物分子主要以分子间的聚集方式聚集,形成多分子聚集体.增大X,使聚合物分子疏水缔合作用增强而电荷之间的排斥作用相对减弱,导致聚集体的内部结构更为紧实.表现为聚集体尺寸减小,同时尺寸随浓度升高的增大幅度减小.非离子表面活性剂与聚合物存在很强的相互作用,在混合溶液中浓度达到CMC左右时聚合物聚集体开始解离,形成混合聚集体.表面活性剂的亲水基团长度越长,空间位阻越大,使疏水缔合的聚合物碳链之间更容易分离,对聚合物聚集体的解离能力越强. C12E40在混合溶液中浓度为10.0 g·L-1时将0.2 g·L-1、X=0.5的聚合物聚集体全部解离,形成的混合聚集体的流体力学半径Rh为6.8 nm,与C12E40自身形成的聚集体尺寸相当.
1 Hurter,P.N.;Scheutjens,J.M.H.M.;Hatton,T.A. Macromolecules,1993,26:5592
2 Glatter,O.;Scherf,G.;Schillen,K.;Brown,W.Macromolecules, 1994,27:6046
3 Webber,S.E.J.Phys.Chem.B,1998,102:2618
4 Kawata,T.;Hashidzume,A.;Sato,T.Macromolecules,2007,40: 1174
5 Kathmann,E.E.;White,L.A.;McCormick,C.L. Macromolecules,1996,29:5273
6 Kramer,M.C.;Welch,C.G.;Steger,J.R.;McCormick,C.L. Macromolecules,1995,28:5248
7 Morishima,Y.;Nomura,S.;Ikeda,T.;Seki,M.;Kamachi,M. Macromolecules,1995,28:2874
8 Hu,Y.;Smith,G.L.;Richardson,M.F.;McCormick,C.L. Macromolecules,1997,30:3526
9 Hu,Y.;Armentrout,R.S.;McCormick,C.L.Macromolecules, 1997,30:3538
10 Suwa,M.;Hashidzume,A.;Morishima,Y.;Nakato,T.;Tomida, M.Macromolecules,2000,33:7884
11 Branham,K.D.;Snowden,H.S.;McCormick,C.L. Macromolecules,1996,29:254
12 Yamamoto,H.;Mizusaki,M.;Yoda,K.;Morishima,Y. Macromolecules,1998,31:3588
13 Hashidzume,A.;Kawaguchi,A.;Tagawa,A.;Hyoda,K.;Sato,T. Macromolecules,2006,39:1135
14 Yusa,S.;Kamachi,M.;Morishima,Y.Langmuir,1998,14:6059
15 Noda,T.;Morishima,Y.Macromolecules,1999,32:4631
16 Noda,T.;Hashidzume,A.;Morishima,Y.Macromolecules,2000, 33:3694
17 Noda,T.;Hashidzume,A.;Morishima,Y.Langmuir,2000,16: 5324
18 Noda,T.;Hashidzume,A.;Morishima,Y.Macromolecules,2001, 34:1308
19 Xu,X.H.;Yang,F.;Wang,N.;Shen,M.H.;Zhou,T.T.;Wang,X. Y.;Wang,Y.L.;Chen,X.J.;Wang,J.B.Journal of Dispersion Science and Technology,2008,29:101
20 Zhao,Y.Z.;Zhou,J.Z.;Xu,X.H.;Liu,W.B.;Zhang,J.Y.;Fan, M.H.;Wang,J.B.Colloid Polym.Sci.,2009,287:237
21 Yu,Y.M.;Gao,B.J.;Wang,R.X.Chin.J.Colloid Polym.,2005, 23:26 [于亚明,高保娇,王蕊欣.胶体与聚合物,2005,23:26]
22 Yamamoto,H.;Tomatsu,I.;Hashidzume,A.;Morishima,Y. Macromolecules,2000,33:7852
23 Wilhelm,M.;Zhao,C.L.;Wang,Y.;Xu,R.;Winnik,M.A.;Mura, J.L.;Riess,G.;Croucher,M.D.Macromolecules,1991,24:1033
24 Hashidzume,A.;Mizusaki,M.;Yoda,K.;Morishima,Y. Langmuir,1999,15:4276
25 Yusa,S.;Hashidzume,A.;Morishima,Y.Langmuir,1999,15: 8826
26 Yamamoto,H.;Morishima,Y.Macromolecules,1999,32:7469
27 Hashidzume,A.;Ohara,T.;Morishima,Y.Langmuir,2002,18: 9211
28 Jacquin,M.;Muller,P.;Cottet,H.;Crooks,R.;Thoédoly,O. Langmuir,2007,23:9939
October 12,2009;Revised:November 17,2009;Published on Web:December 14,2009.
Aggregation Behavior of Amphiphilic Statistical Polymers and Their Interactions with Nonionic Surfactants
WU Xu1,2QIAO Ying-Jie1HU Chang-Chao2YANG Hui1,2WANG Jin-Ben2,*
(1College of Materials Science and Chemical Engineering,Harbin Engineering University,Harbin 150001,P.R.China;
2Key Laboratory of Colloid,Interface and Chemical Thermodynamics,Institute of Chemistry, Chinese Academy of Sciences,Beijing 100190,P.R.China)
A series of amphiphilic polymers were synthesized by the statistical polymerization of 2-(acrylamido)-dodecanesulfonic acid(AMC12S)with 2-(acrylamido)-2-methylpropanesulfonic acid(AMPS)and they contained a high mole fraction of AMC12S(X=0.1,0.3,0.5).The aggregation behaviors of the polymers and their interactions with three nonionic surfactants HO(CH2CH2O)10C12H25(C12E10),HO(CH2CH2O)20C12H25(C12E20),and HO(CH2CH2O)40C12H25(C12E40) in aqueous solutions were investigated by steady-state fluorescence and quasi-elastic light scattering measurements. The effect of X on the association performance and the influence of the surfactant′s hydrophilic group length on these interactionswerealsoinvestigated.Thecriticalaggregationconcentration(CAC)ofthepolymerwasfoundtosignificantly decrease with increasing X.The CAC of the polymer with X=0.5 is as low as 0.0039 g·L-1.The hydrodynamic sizes of the aggregates(Rh)are larger than 26 nm and increase with an increase in polymer concentration,indicating that the polymeric molecules exhibit a strong tendency for interpolymer association,leading to the formation of multimolecular aggregates.When X increases,both Rhand its tendency to increase decrease,suggesting that the aggregates become more compact.The interaction between surfactant and polymer is very strong and the polymer aggregates begin to collapse when the surfactant concentration reaches the critical micelle concentration(CMC)in the mixed solutions and mixed aggregates form.The destructive ability of the surfactant increases as the length of the hydrophilic group increases.The Rhvalue of the mixed aggregates formed by C12E40and the polymer with X=0.5 is 6.8 nm,which is consistent with the Rhvalue of the C12E40aggregates.
Nonionic surfactant;Amphiphilic polymer; Aggregation behavior;Aggregate;Interaction
O648
*Corresponding author.Email:jbwang@iccas.ac.cn;Tel/Fax:+86-10-62523395.
The project was supported by the Important National Science and Technology Specific Project of China(2008ZX05024-02)and National High-Tech Research and Development Program of China(863)(2006AA09Z305).
国家科技重大专项(2008ZX05024-02)和国家高技术研究发展计划(863)项目(2006AA09Z305)资助
