水杨酸、水杨酸甲酯对亚硝胺合成阻断作用研究
2010-11-26黄娟马建华
黄娟,马建华
(集美大学 生物工程学院,福建 厦门 361021)
亚硝胺是目前所知的最强的化学致癌物质之一,亚硝胺能引起人和动物肝脏等多种器官的恶性慢性肿瘤.在人体胃的酸性环境中,过量的亚硝酸盐也可以转化为亚硝胺,清除体内亚硝酸盐是防止癌症的有效途径[1].水杨酸(SA)和水杨酸甲酯(MS)天然存在于一些植物体内,具有镇静止痛、清热解毒等功能,是医药、食品、香料、染料和农药等工业的重要中间体[2-4].近年来,SA、MS的生物功能不断被发现,如有关SA、MS是植物对外界伤害(机械伤害,食草动物、昆虫、病原菌浸染)做出反应而表达抗性基因的信号分子的相关研究报道[5].但目前SA、MS诸多生物功能的分子机制尚不完全明了,SA、MS是否具有对亚硝胺合成的阻断效果呢?本研究工作以254 nm紫外光为辐照源,利用稳态分析方法分别测定SA、MS对亚硝胺合成的阻断率,同时探讨浓度、pH值、反应时间等影响因子对SA、MS阻断效果的影响,并与抗坏血酸作用效果进行对照.所获研究结果将不仅有助于进一步开拓SA、MS的生物功能,而且可为进一步阐释它们光生物活性作用的分子机制提供重要依据.
1 实验部分
1.1仪器和试剂ZF-20C 暗箱式紫外分析仪(上海宝山顾村电光仪器厂),CARY50紫外-可见分光光度仪(东南化学仪器有限公司),UV-2000紫外-可见分光光度计(尤尼柯(上海)仪器有限公司),HH-6数显恒温水浴锅(国华电器有限公司),FA51001电子天平(上海精科天平有限公司),pHS-3TC(0.01级)精密数显酸度计(上海天达仪器有限公司).
水杨酸(SA):广东汕头西陇化工厂;水杨酸甲酯(MS):中国国药(集团)上海化学试剂分公司;抗坏血酸(Vc):广东汕头西陇化工厂;其余试剂均为分析纯,实验用水为超纯水.
1.2实验方法控制适宜的酸性条件,用二甲胺或盐酸二甲胺与温热的亚硝酸钠反应,即可合成二甲基亚硝胺.其化学反应方程式为[6]:

其实质为:

当向样品(SA或MS)溶液中加入二甲胺与亚硝酸钠时,样品优先与亚硝酸钠作用,使得二甲胺不能与亚硝酸钠反应,达到阻止亚硝胺生成的目的.据此可以比较相同条件下生成亚硝胺量的多少来反映样品阻断能力的强弱.
在紫外光照射下,二甲基亚硝胺可分解成二甲基仲胺和亚硝酸根,反应式如下:
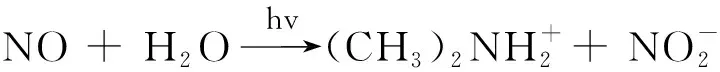
亚硝酸根与对氨基苯磺酸重氮化后,再与α-萘胺偶合生成红色化合物,使用Cary 50紫外分光光度计在400~800 nm波长范围内扫描该化合物的最大吸收波长,测出该化合物的吸光度值,即可计算上述反应液中亚硝胺含量的多少[7].
在空气饱和的状态下,以254 nm为紫外辐照波长,采用紫外光解法,操作及测定方法按照文献[7]进行,同时做浓度、反应时间等影响因子实验,并以Vc做对照.
阻断率/%=[(A0-A)/A0]×100
式中:A0,未加样品时NaNO2的吸光度值(以试剂空白溶液为参比溶液);A, 加入样品后NaNO2的吸光度值(以样品为参比溶液).
2 结果与分析
2.1吸收光谱使用Cary 50紫外分光光度计在400~800 nm波长范围内扫描最大吸收波长,如图1.由图可以看出,加样品(SA、MS和Vc)与不加样品(Blank)时NaNO2经着色反应后的最大吸收峰在525 nm处,这与文献[7]报道的一致,故选择525 nm为检测波长.

图1 吸收光谱图
2.2紫外照射波长对亚硝胺合成阻断率的影响在25 mL比色管中均加入相同体积的样品(SA或MS)溶液,按照1.2的方法,分别测试反应液在365 nm 和254 nm 紫外波长照射下对亚硝胺的阻断率,结果见表1.
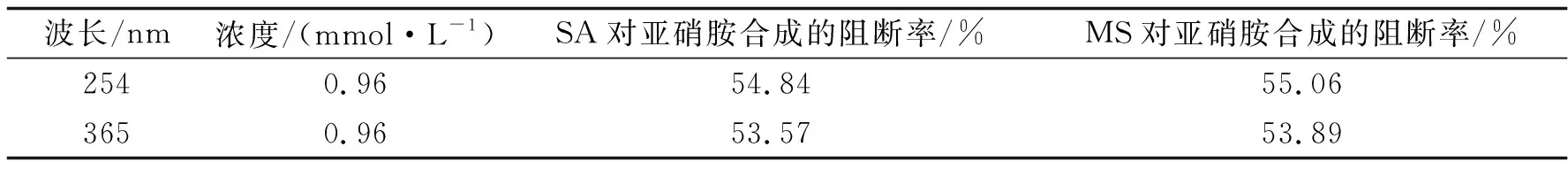
表1 不同紫外波长照射下相同浓度的SA与MS对亚硝胺的阻断率
观察表1可知,254 nm紫外波长照射下,相同浓度的SA、MS对亚硝胺的阻断作用比365 nm 照射下稍微强些,可能是紫外波长不同照射能量不同,导致二甲基亚硝胺的分解率不同.以下选择254 nm作为紫外照射波长进行实验研究.
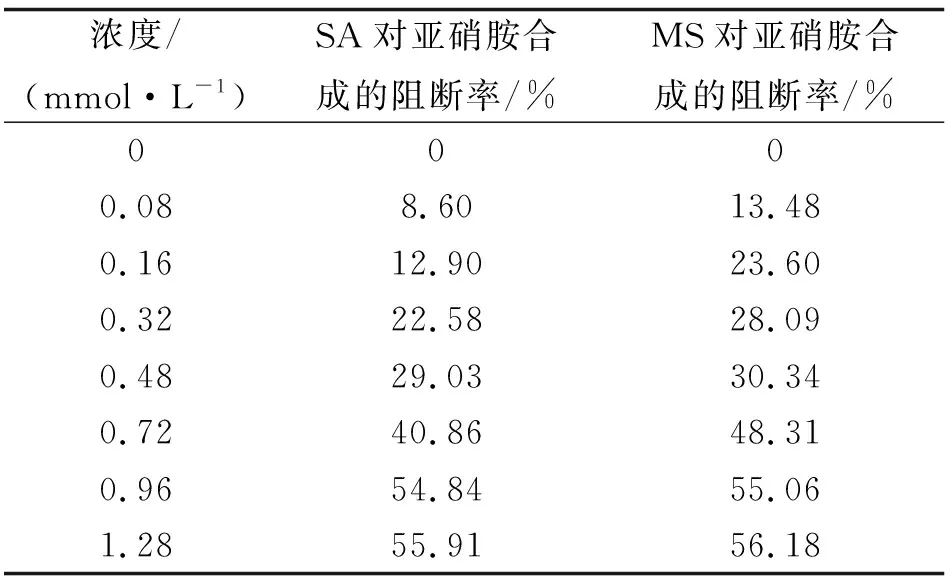
表2 样品浓度与对亚硝胺合成的阻断率的剂量关系
2.3浓度对亚硝胺合成阻断效果的影响在25 mL比色管中均加入不同体积的样品(SA或MS)溶液,按照1.2的方法,测试不同浓度的样品在254 nm 紫外波长照射下对亚硝胺的阻断率,结果见表2.
由表2可以看出,在0.08~1.28 mmol/L范围内,样品浓度与亚硝胺合成的阻断效果呈明显的剂量关系,但当浓度达到1.28 mmol/L时,阻断率增加趋缓.该范围内SA、MS对亚硝胺合成的阻断率最大分别可达55.91%、56.18%.说明SA和MS均可有效地阻断亚硝胺的合成,且相同浓度的SA和MS对亚硝胺阻断作用能力的强弱顺序为MS >SA.
2.4反应时间对亚硝胺合成阻断效果的影响在25 mL比色管中均加入6.0 mL浓度为4 mmol/L的的样品(SA或MS)溶液,按照1.2的方法,分别测试样品液反应不同时间对亚硝胺的阻断率,结果见表3.
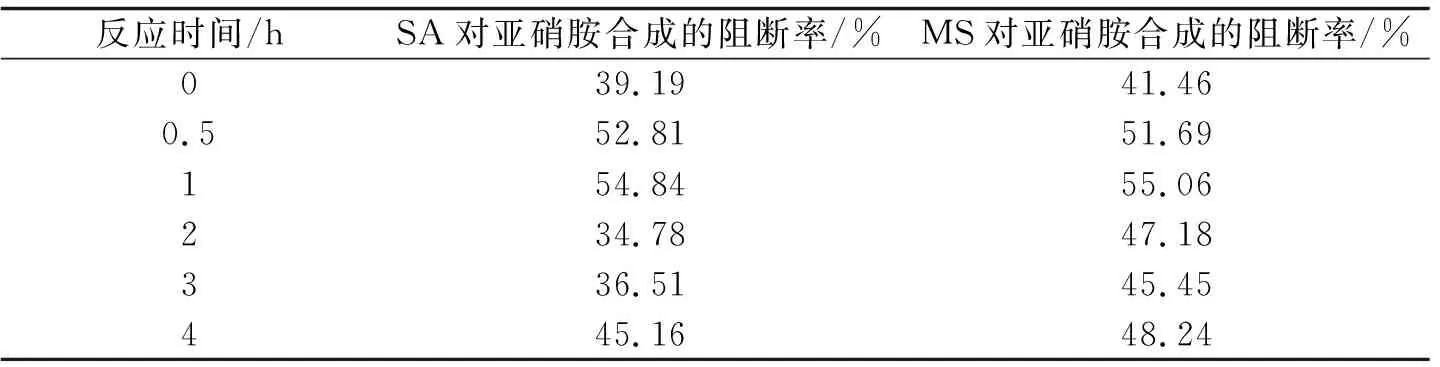
表3 反应时间对SA、MS阻断亚硝胺合成效果的影响
结果表明,SA、MS阻断亚硝胺的反应速度较快,37 ℃水浴下反应1 h时就已达到最大阻断率,此时SA、MS对亚硝胺的阻断率即可分别达到54.84%、55.06%,延长反应时间阻断率反而下降.本实验选择1 h作为反应时间.
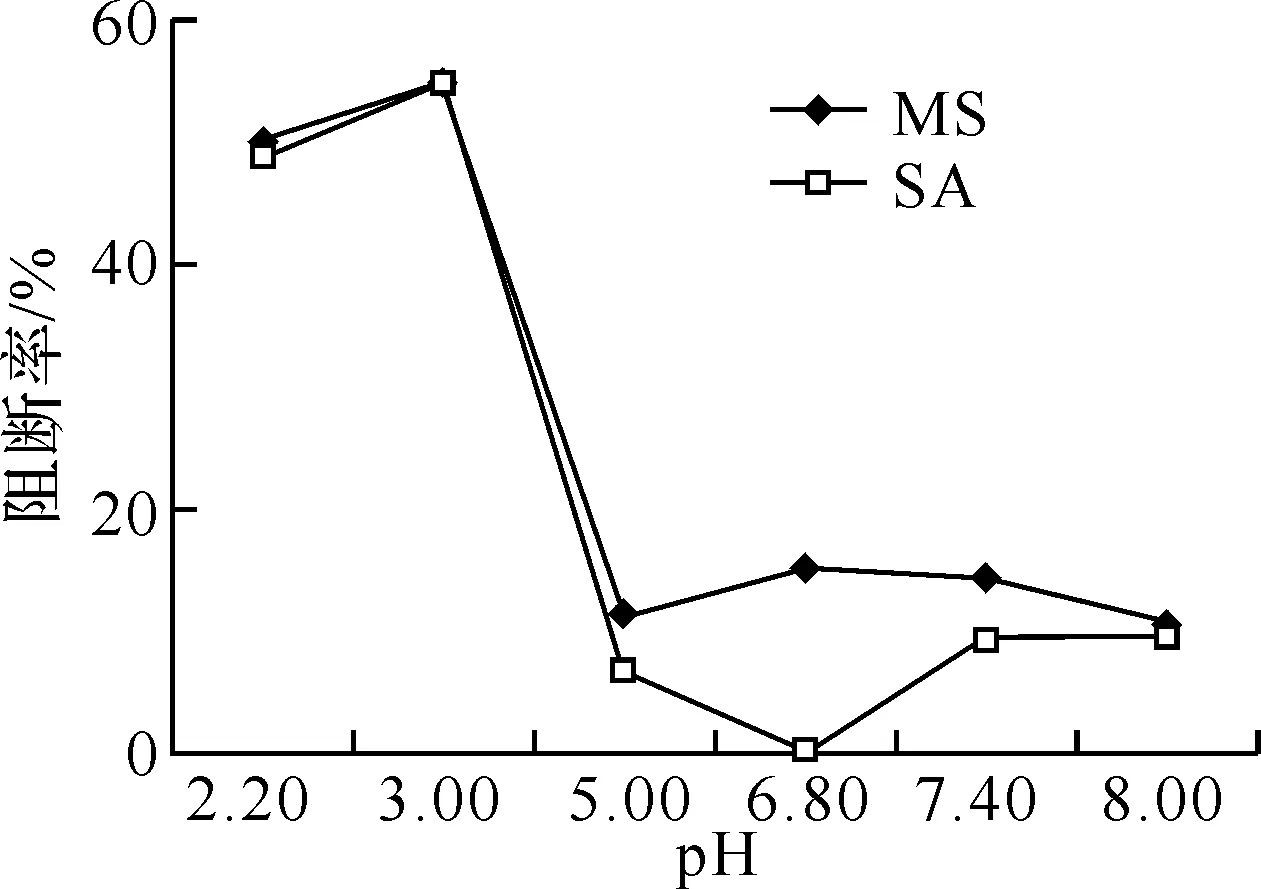
图2 不同pH值对亚硝胺合成阻断效果的影响
2.5不同pH值对亚硝胺合成阻断率的影响根据以上实验结果,改变缓冲液的pH值,在25 mL比色管中均加入6.0 mL浓度为4 mmol/L的的样品(SA、MS)溶液,按照1.2的方法,分别测试反应液在254 nm波长照射下对亚硝胺的阻断率,结果见图2.

图3 不同反应温度对SA、MS对亚硝胺合成阻断作用的影响
结果显示,SA、MS对亚硝胺合成的阻断效果与pH值并不是简单的线性关系,而是一个波动过程.pH ≥ 5.00时,SA、MS对亚硝胺的阻断作用较差,尤其是SA,在pH 6.80时对亚硝胺的阻断率几乎为零.但在pH 3.00时SA、MS对亚硝胺的阻断效果却比较好,可分别达54.84%、55.06%.预示反应体系的pH 值直接影响二甲基亚硝胺的生成,pH 酸性体系有利于SA、MS阻断亚硝胺的合成.
2.6反应温度对亚硝胺合成阻断率的影响根据以上实验结果,改变体系的水浴温度,在25 mL比色管中均加入6.0 mL浓度为4 mmol/L的的样品(SA、MS)溶液,按照1.2的方法,分别测试反应液在254 nm波长照射下对亚硝胺的阻断率,结果见图3.
由图3可以看出,在温度较低或者较高的范围内,SA、MS对亚硝胺的阻断效果不是很明显,而在人体正常温度范围(37 ℃左右),却有良好的阻断效果,说明SA、MS在人体内可以有效地阻断亚硝胺的合成.
2.7 SA、MS与Vc对亚硝胺阻断率的比较已经有很多报道证明了Vc 具有抗氧化作用[8-9],还有文献报道Vc 对亚硝胺合成的阻断率亦很强[10],所以选择Vc 为参照物,比较SA、MS的阻断能力.
根据以上各影响因子的实验结果,以254 nm紫外线为辐射源,用相同量的SA、MS与Vc 进行阻断反应,计算各自的阻断率并进行比较,结果见表3.

表4 SA、MS与Vc对亚硝胺阻断率的比较
由表3可以看出,同等条件下的SA、MS对亚硝胺的阻断能力比Vc弱些,其阻断能力依次为Vc> MS> SA,说明SA、MS均具有较强的阻断亚硝胺的能力.
3 结论与讨论

SA、MS能有效阻断亚硝胺的合成.在反应时间1 h、pH3.00、反应温度37 ℃、反应浓度为1.28 mmol/L、紫外辐射波长254 nm的条件下,SA、MS对亚硝胺合成的阻断效果最好,与同等条件下的Vc相比较,阻断能力依次是:Vc> MS> SA.
SA、MS和Vc的结构如右:
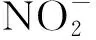
一些植物体内天然存在SA、MS,它们是植物抗逆(抗病、抗虫等)的信号分子.利用植物有效成分阻断亚硝胺合成是防治癌症的有效途径之一;本研究对SA、MS可有效阻断强致癌物—亚硝胺合成的功能研究结果,不仅进一步开拓了SA和MS生物活性功能,也为天然酚类化合物抗癌生物活性分子作用机制的阐释提供了部分科学依据.
参考文献:
[1] 周奇文.实用食品加工新技术[M].北京:中国食品出版社,1998:25-28.
[2] 田霞,赵地顺.水杨酸及其衍生物[J].河北化工,2001(4):4-6.
[3] 安甲驹,王伯英.实用精细化工词典[M].北京:轻工业出版社,1988.
[4] 何坚,孙宝国.香料化学与工艺学——天然、合成、调合香料[M].北京:化学工业出版社,1995:401-402.
[5] 刘新,张玉娜.水杨酸及其衍生物对蚕豆气孔开闭的影响[J].莱阳农学院学报,1999,16(2):104-106.
[6] 胡荣梅,马立珊.N-亚硝基化合物分析方法[M].北京:科学出版社,1980:50.
[7] 赵二劳,王晓妮,张海容,等.山楂清除亚硝酸盐及阻断亚硝胺合成的研究[J].食品与发酵工业,2006,32(10):29-31.
[8] 刘冉,许莹,杨梅,等.一种化学发光体系测定抗坏血酸的抗氧化性[J].鞍山师范学院学报,2004,6(6):58-59.
[9] 伍惠生.维生素C在水产养殖业中的应用[J].河南水产,2000(3):21-24.
[10] 张虹,许钢,袁建耀.刘寄奴提取液对亚硝化反应的抑制作用[J].郑州粮食学院学报,2000,21(1):50-53.
[11] 汪小兰.有机化学[M].北京:高等教育出版社,2000:142-143.
[12] 黄梅丽.食品化学[M].北京:中国人民大学出版社,1986:173.
