临床观察小牛脾提取物注射液联合FOLFOX方案治疗晚期大肠癌的临床观察
2010-09-21张金淑
张金淑
吉林市第二人民医院肿瘤内科(132002)
大肠癌是人类常见恶性肿瘤之一,包括结肠癌和直肠癌,近30年,我国大肠癌也由常见肿瘤的第6位上升到第4位。大肠癌初治诊断分期:Ⅰ期占15%、Ⅱ期占20%~30%、Ⅲ期占30%~40%、Ⅳ期占20%~25%。所以约60%~70%患者需要内科的治疗——辅助化疗和晚期肿瘤治疗。大肠癌晚期治疗以术后常规化疗或全身化疗为主。现常予FOLFOX的双周方案连续化疗[1],疗效较佳。斯普林既能高效抑杀癌细胞,又显著提高机体免疫功能,对化疗有增效减毒的功能,是一种有效安全的抗肿瘤药物,为探讨斯普林与FOLFOX方案联合治疗晚期大肠癌的效果,吉林市第二人民医院自2005年1月至2008年1月共60例并与单纯FOLFOX方案治疗进行了对比,现将结果报道如下。
1 材料与方法
1.1 临床资料
60例晚期大肠癌患者均经病理和细胞学检查证实。男性38例、女性22例;年龄35~73岁,中位年龄47岁;Kamofsky评分60分;按国际TNM分期均为Ⅲ~Ⅴ期,预计生存期3个月以上,心、肝、肾功能及血象正常,随机分为试验组和对照组30例。两组病例的各项指标没有明显差异(P>0.05),见表1。
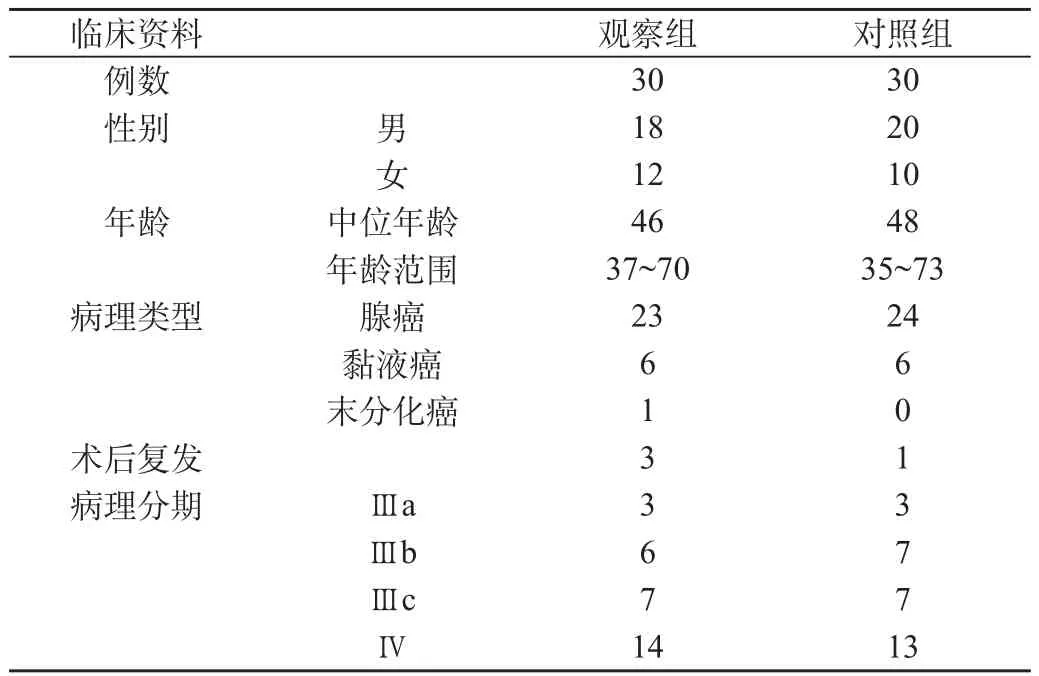
表1 两组病例一般资料比较
1.2 治疗方法
对照组采用FOLFOX方案,奥沙利铂100mg/m2,静脉滴注1d,亚叶酸钙200mg/m2,静脉滴注1~2d,氟尿嘧啶400mg/m2静脉注射1~2d,氟尿嘧啶600mg/m2持续46h静脉泵入,每2周为1个周期,至少2周期。治疗组在对照组的基础上化疗同时给予斯普林10mL/d,静脉滴注连用2个周期。
1.3 评价标准
全部病例在完成2个周期后进行疗效评价,疗效评价按照WHO化疗标准[2]:完全缓解(CR)即临床指标显示肿瘤完全消失,持续至少4周;部分缓解(PR)即肿瘤缩小超过50%,持续至少4周;稳定(SD)即肿瘤缩小不足50%,或增大不超过25%,无新病灶出现持续4周以上;进展(PO)即肿瘤增大超过25%以上或出现新病灶。有效率(PR)为缓解(CR+PR)的病例数点全部可评价疗效病例的百分数,不良反应按WHO抗肿瘤药物不良反应分级标准分为0~Ⅳ。
1.4 统计学方法
有效率和不良反应比较采用χ2检验,P<0.05表示差异有统计学意义。
2 结 果
2.1 血象变化性况
两组治疗前的血象(WBC、RBC、HB、PLT)比较无统计学意义(P>0.05)。治疗后试验组现象(WBC、RBC、HB、PLT)与治疗前相比无统计学意义(P>0.05)而对照治疗后(血象WBC、RBC、HB、PLT)与治疗前相比较有明显的下降(P<0.05)。两组治疗后血象(WBC、RBC、HB、PLT)相比较有明显差异,对照组治疗后血象(WBC、RBC、HB、PLT)试验组明显下降(P<0.05)。由此可见,斯普林具有良好的稳定血象,促进骨髓造血功能恢复的作用。见表2。
2.2 近期疗效
试验组有效率46.6%(14/30);对照组有效率为20%(6/30)两组间疗效有显著性差异P<0.05,见表3。
2.3 不良反应
试验组乏力,食欲减退,恶心呕吐及手脚麻木的发生率明显低于对照组,两组间差异有显著性(P<0.05),见表4。
3 讨 论
大肠癌的发病率和病死率在我国一直处于上升期,FOLFOX方案为大肠癌化疗的推荐方案[3],但如何更有效发挥其对癌细胞的杀伤作用,并减少不良反应的发生是关键,随着对肿瘤研究不断深入,肿瘤辅助药物研究也不断深入,并与手术、放疗、化疗联合使用,起到较好的增效减毒的作用。斯普林注射液是从健康胎牛脾脏中以高科技先进手段提取精制而成的高活性小分子多肽相对分子质量<100000。普斯林独特作用于肿瘤细胞代谢活跃的G1期和静止期G0期向G2和S期转化过程发生障碍而达到抗肿瘤作用。此外癌细胞以高度糖酵解为特征而斯普林则可非毒性抑制糖酵解导致肿瘤细胞变性和凋亡而达到抗癌作用。斯普林还激活免疫系统使T淋巴细胞活性增强,数量增多,并刺激细胞分裂抑制素增加整体提高机体免疫力及诱导抗肿瘤因子释放,最后斯普林刺激骨髓干细胞增殖,使外周血细胞数量增加升高血细胞,提高造血功能。

表2 两组治疗前后血象变化
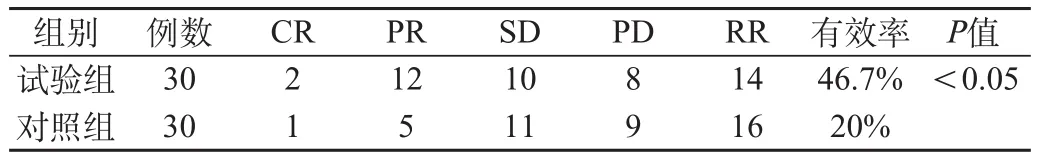
表3 两组近期疗效的比较

表4 两组不良反应发生情况的比较
本实验采用随机分组对照比较的方法,研究了斯普林联合FOLFOX方案治疗晚期大肠癌,结果试验组有效率为46.7%,明显高于对照组,显示了斯普林对奥沙利铂和氟尿嘧啶有明显的增效减毒,稳定血象的作用。
[1]孙燕,石远凯.临床肿瘤内科手册[M].北京:人民卫生出版社,1987.
[2]孙燕.内科肿瘤学[M].北京:人民卫生出版社,2001.
[3]爱德华·楚.国际化疗标准方案检查[M].北京:化学工业出版社,2008.
