溶剂热法制备钴微球及其表征
2010-09-15贺文启成嘉亮魏冠东易观贵刘应亮袁定胜黄浪欢谭绍早
贺文启 肖 勇 成嘉亮 魏冠东 赵 率 易观贵 刘应亮袁定胜 黄浪欢 谭绍早
(暨南大学化学系,纳米化学研究所,广州 510632)
溶剂热法制备钴微球及其表征
贺文启 肖 勇 成嘉亮 魏冠东 赵 率 易观贵 刘应亮*袁定胜 黄浪欢 谭绍早
(暨南大学化学系,纳米化学研究所,广州 510632)
磁性材料;溶剂热法;钴微球
0 引 言
过渡金属钴以及它的一些氧化物,以其特殊的电、磁和光学性能被广泛应用到信息存储[1]、催化剂[2]、磁光材料[3]、铁磁流体[4]以及生物医学[5]等诸多领域。前人曾经用羰酰钴热解法[6-7]、γ射线照射法[8]、光刻气相沉积法[9]、电化学沉积法[10]和金属盐溶液的液相还原法[11-12]等方法合成出诸多新颖形貌的钴纳米材料,如钴纳米棒[6,13-14]、钴纳米线[10,15-17]、钴纳米带[18]、钴纳米片[19]、钴纳米花[12]、钴立方块[20-21]、钴空心球[22]等。而有关溶剂热法合成钴球及其性能的研究却鲜有报道。本工作在不锈钢反应釜中,以Co(CH3COO)2·4H2O为钴源,用无水乙醇做溶剂和还原剂,采用溶剂热法在250℃一步合成出形貌均一、分散性好的钴微球。考查了反应时间和反应温度对钴微球形貌以及晶型结构的影响,验证了高温条件下六方晶型的钴向面心立方晶型转化的实验结果。在250℃的低温条件下用弱还原性的、无毒环保的乙醇便合成出了钴单质,该方法与其它的合成方法相比,具有操作简便,工艺简单等优点。磁性测试表明我们合成的钴微球磁矫顽力(Hc)达230 Oe,与胶状球形钴材料相比要高出许多[23],同一些纳米级的钴材料相比也并不低[10]。
1 实验部分
1.1 实验试剂
Co(CH3COO)2·4H2O(广东光华化学厂有限公司),无水乙醇(天津市大茂化学试剂厂),所用试剂均为分析纯。
1.2 钴微球的制备
称取 3.0 g Co(CH3COO)2·4H2O,于烧杯中加入50 mL无水乙醇搅拌溶解,然后转移至60 mL不锈钢反应釜中,封盖,置于预先设定好反应温度和时间的高温炉中,待反应完毕后,自然冷却至室温,开釜,抽滤,用去离子水和无水乙醇分别洗涤多次,收集固体产物,置于硅胶干燥器中晾干,收集产品进行下一步的表征。
1.3 钴微球的表征
产物结构分析在MSAL-XD2型X射线粉末衍射仪 (Cu靶Kα射线,λ=0.15418 nm,X射线管电压36 kV,电流 20 mA,扫描速度 8°·min-1)上进行,形貌在Philips XL-30扫描电镜(加速电压为30 kV)上进行,磁性测量在MPMS XL-7磁性测量仪进行。
2 结果与讨论
2.1 最佳条件下得到的钴微球
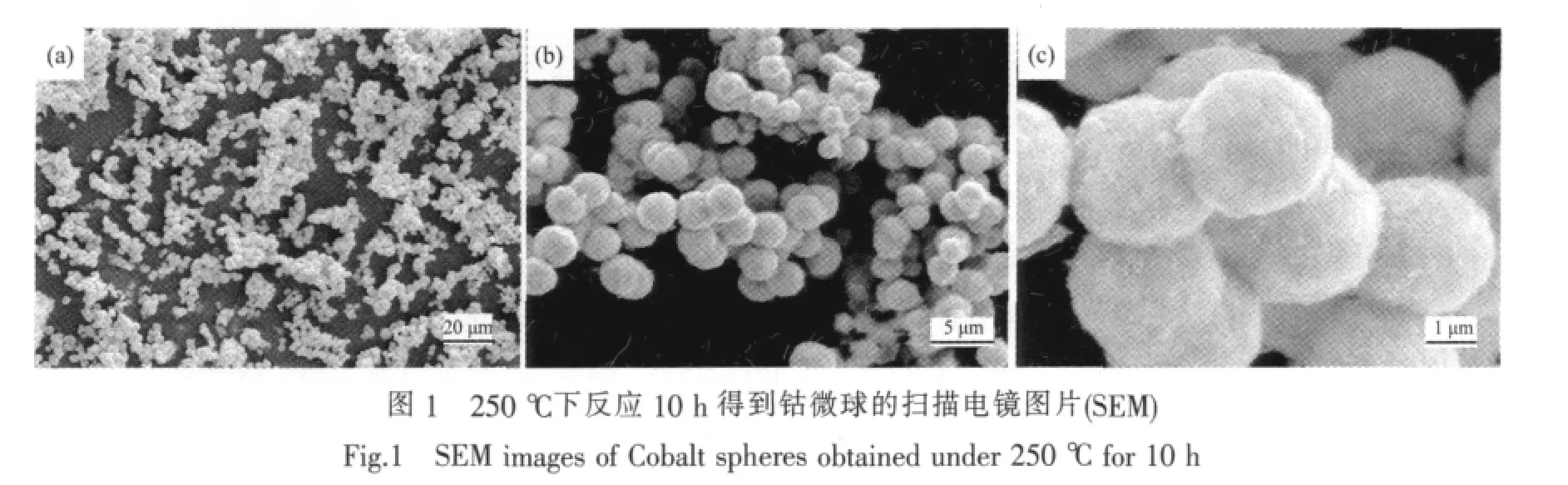
图1是最佳反应条件(250℃下反应10 h)下得到的钴微球的扫描电镜图片(SEM),图1a为低倍下的全景图,由图1a可知所得产物分散性好,形貌单一;图1b为图1a的局部放大图,由图可知所得产物是尺寸比较均一的钴球;图1c为图1b的局部放大图,由图1c可知钴球的尺寸为3~4 μm,钴微球的表面不是很光滑,但其形状都是很规整的球形。由此,可以认为在该实验条件下得到了分散性好、尺寸较均一的钴微球。
2.2 反应时间对钴微球的影响
图2是250℃下反应10、20和40 h所得产物的XRD图。由图可知所得产物大约在2θ角为41.6°、44.3°和 47.4°处有较强的衍射峰,与标准 PDF(89-4308)卡片对比,其对应的晶面分别是100面、002面和101面,标识如图,可知其为六方晶相(hcp)的钴单质。比较图2a、b、c可知随反应时间的延长衍射峰的强度有所增强,衍射峰位置没有发生变化,说明随反应时间的延长钴的结晶度变好,而其晶形仍为六方晶相。

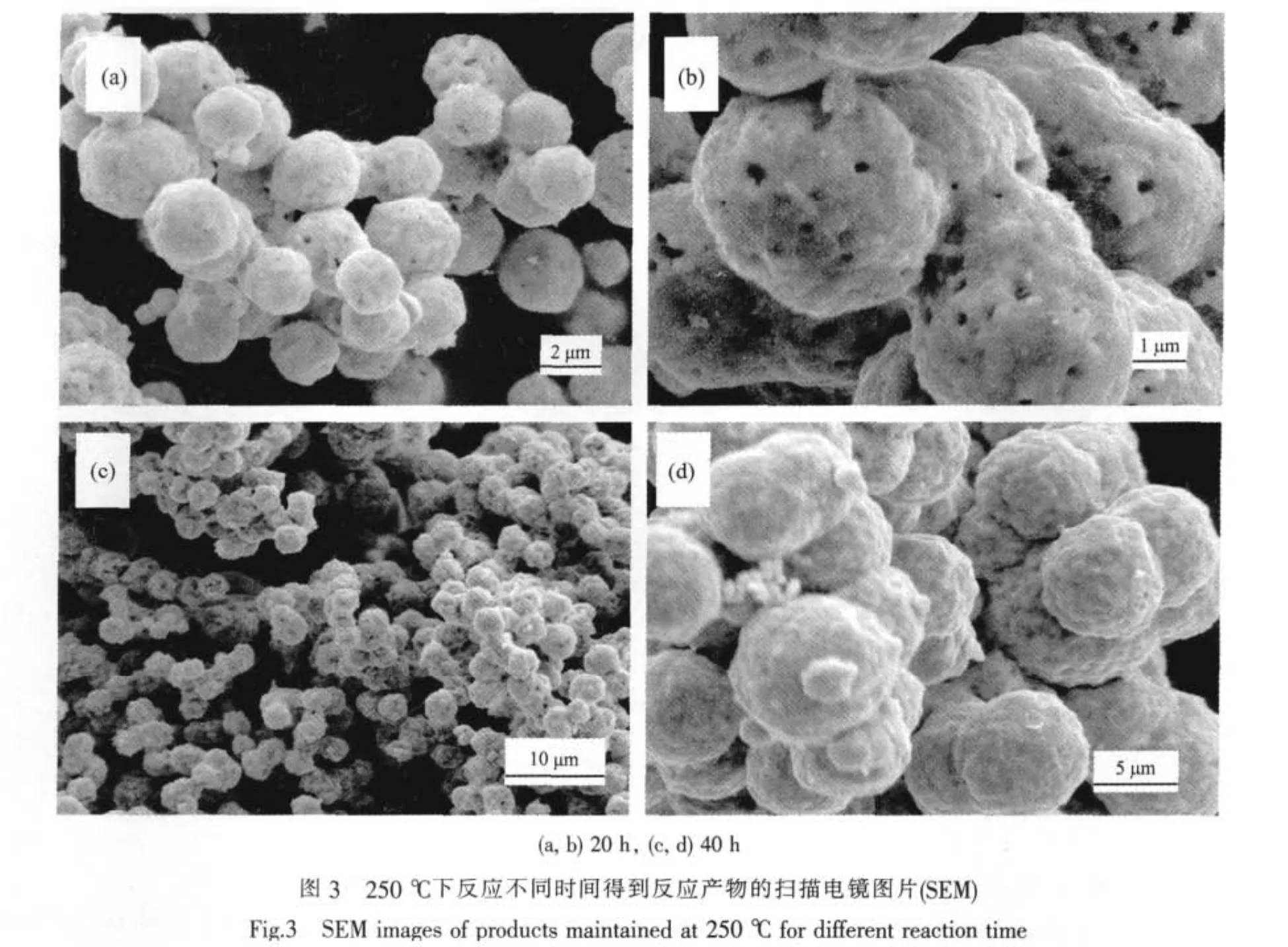
图3是250℃下反应不同时间所得产物的扫描电镜图片(SEM),从图3与图1的比较可以看出,在反应温度不变的情况下,随反应时间的延长,钴微球的形貌得到很好的保持,但钴球表面的絮状绒丝消失了,而且其尺寸随时间的延长略有增大,这是因为随反应时间的延长,会有更多的钴单质被还原出来并吸附在原先的钴球表面,使其直径不断增大。同时我们也注意到这样一些细节,反应20 h得到的产物表面有一些微小的孔道(图3b),而反应40 h得到的产物中这些孔道又消失了但其表面却不再是先前那样的平整(图3d)。我们认为,反应10 h得到钴球的表面是一层蓬松的丝状钴单质,随着反应时间的延长,这一层蓬松物慢慢熔结在一起,使钴球表面出现一些微小孔道,当时间继续延长时,这些孔道又由于钴球表面钴单质的熔结而消失,但钴球表面却留下一些坑道,从而导致钴球表面不平整。
2.3 反应温度对Co晶形的影响
钴单质有两种稳定的晶相,六方晶型(hcp)和面心立方晶型(fcc),多以六方晶相存在,常温常压下两种晶型的钴也能够共存,但当温度高于425℃时,六方晶型的钴全部会转化为面心立方[13]。此外,当钴元素以细小颗粒(微米或者纳米尺寸)存在时,还会有一种亚稳态的ε-钴,这在Dinega等[1]报道中有明确的解释,后来,Hinotsu等[24]也证明了其与β相的锰元素的晶型结构相似。
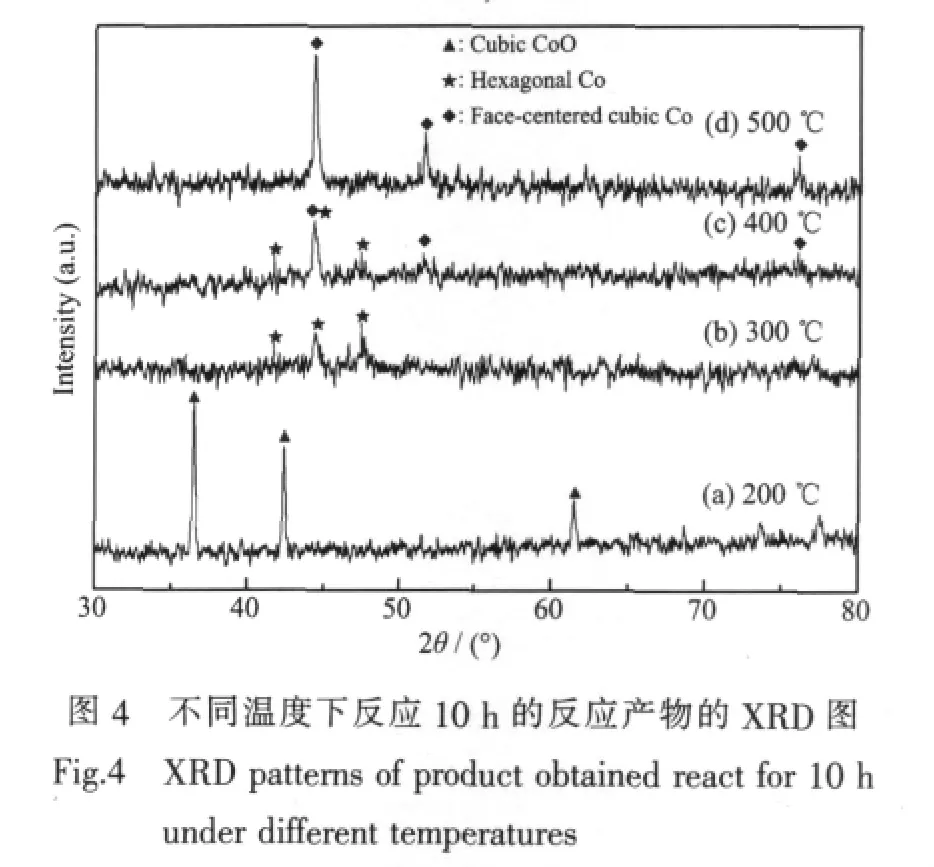
图4为不同温度下反应10 h的反应产物的XRD图。反应温度为200℃时,由图4a可知2θ角在36.5°、42.4°和61.5°处有较强的衍射峰,与标准PDF(75-0393)卡片一致,可知其为立方晶相的氧化钴,由此说明在200℃下还没有钴单质生成。当反应温度为300℃时,由图4b可知2θ角为41.6°、44.3°和47.4°处有明显衍射峰,对比标准PDF(89-4308)卡片,可知其为六方晶相(hcp)的钴单质。当反应温度为500℃时,由图4d可知2θ角为44.3°、51.5°和75.9°处有较强的衍射峰,对比标准PDF(89-4307)卡片,可知其为立方晶相(fcc)的钴单质。反应温度为400℃时,由图4c与图4b、d比较可知,既能看到六方晶系的衍射峰,又能看到立方晶系的衍射峰,其产物恰好是300和500℃条件下两种晶形的混合相。
通过扫描电镜图片我们同样可以看出有关晶相转化的一些迹象,由图5a可知,当反应温度为300℃时,钴微球的形貌还是基本得以保持,但球形不是太规整,而且有部分熔结在一起。当反应温度升高到500℃时(图5c),取而代之的是另外一种形貌,一些小颗粒杂乱地堆积在一起,并没有规则的形状。而当反应温度设定在400℃时,由图5b我们既能看到一些与图5a类似的规则的钴球,又能看到一些像5c一样的不规则的小颗粒。不同晶相的钴单质以不同的形貌存在,在该工作中,得到的六方晶系的钴是球形,而立方晶系的钴却是一些杂乱堆积的小颗粒。

2.4 磁性分析
图6是最佳条件下所得样品在室温 (293 K)时的磁滞回线曲线图,在该温度下测得其磁矫顽力(Hc)、剩余磁感应强度(Br)及饱和磁感应强度(Ms)分别为 230 Oe、5.19 emu·g-1、35.97 emu·g-1。本文合成的钴微球具有较低的饱和磁感应强度却有较高的磁矫顽力,这与钴微球的尺寸比较大(3~4 μm)大小却均一、分散性好是相一致的[25]。所得样品的磁矫顽力(Hc)达230 Oe与块体钴(几十个Oe)相比要高出很多[10],相比Chen等[23]合成的胶状球形钴纳米粒子(约150 Oe)要大很多,比Fan等[26]合成出的树枝状钴(133.1 Oe)也高出许多,与 Cao等[10]合成的钴纳米线相比磁矫顽力(Hc)也差不多。由此可见,我们合成的钴微球在同类钴磁性材料中有一定的优势。

[1]Dinega D P,Bawendi M G.Angew.Chem.Int.Ed.,1999,38(12):1788-1791
[2]Zhang H Z,Qiu J S,Liang C H,et al.Catal.Lett.,2005,101(3/4):211-214
[3]Diwekar M,Kamaev V,Shi J,et al.Appl.Phys.Lett.,2004,84(16):3112-3114
[4]Raj K,Moskowitz B,Casciari B R.J.Magn.Magn.Mater.,1995,149(1/2):174-180
[5]Pankhurst Q A,Connolly J,Jones S K,et al.Appl.Phys.,2003,36(13):R167-R181
[6]Puntes V F,Krishnan K M,Alivisatos A P.Science,2001,291(5511):2115-2117
[7]Tripp S L,Pusztay S V,Ribbe A E,et al.J.Am.Chem.Soc.,2002,124(27):7914-7915
[8]Kapoor S,Salunke H G,Pande B M,et al.Mater.Res.Bull.,1998,33(10):1555-1562
[9]Javey A,Dai D.J.Am.Chem.Soc.,2005,127(34):11942-11943
[10]Cao H Q,Xu Z,Hai S,et al.Adv.Mater.,2001,13(2):121-123
[11]Sun S,Murray C B.J.Appl.Phys.,1999,85(8):4325-4330
[12]Zhu Y C,Yang Q,Zheng H G et al.Mater.Chem.Phys.,2005,91(2/3):293-297
[13]Puntes V F,Krishnan K M,Alivisatos A P.Topic.Catal.,2002,19(2):145-148
[14]Liu Q Y,Guo X H,Li Y,et al.J.Phys.Chem.C,2009,113,(9):3436-3441
[15]Kenz M,Bittner A M,Boes F,et al.Nano.Lett.,2003,3(8):1079-1082
[16]Yang P X,An M Z,Su C N,et al.Electrochim.Acta,2008,54(2):763-767
[17]Viau G,Garcia C,Maurer T,et al.Phys.Status Solidi A,2009,206(4):663-666
[18]Xie Q,Dai Z,Huang W W,et al.Nanotechn.,2005,16(12):2958-2962
[19]Li H,Liao S J.J.Magn.Magn.Mater.,2009,321(17):2566-2570
[20]Graf C P,Birringer R,Michels A.Phys.Rev.B,2006,73(21):212401-1-212401-4
[21]Cheng G J,Shull R D,Walker A R H.J.Magn.Magn.Mater.,2009,321(10):1351-1355
[22]Jiang C L,Wang Y F.Mater.Chem.Phys.,2009,113(2/3):531-533
[23]Chen J P,Sorensen C M,Klabunde K J.Phys.Rev.B,1995,51:11527-11532
[24]Hinotsu T,Jeyadevan B,Chinnasamy C N,et al.J.Appl.Phys.,2004,95:7477-7480
[25]ZHU Yong-Chun(朱永春).Thesis for the Doctorate of University of Science and Technology of China(中国科学技术大学博士学士论文).2006.
[26]Fan N,Yu H X,Ju Z C,et al.Mater.Lett.,2009,63:551-553
Cobalt Microspheres:Preparation by Solvothermal Method and Characterization
HE Wen-QiXIAO Yong CHENG Jia-Liang WEI Guan-Dong ZHAO ShuaiYI Guan-Gui LIU Ying-Liang*YUAN Ding-Sheng HUANG Lang-Huan TAN Shao-Zao
(Department of Chemistry and Institute of Nanochemistry,Jinan University,Guangzhou 510632)
High purity and uniform sized cobalt microspheres were prepared via solvothermal method by using acetate cobalt as and ethanol as raw materials through one step reaction under 250℃.The samples were characterized by XRD,SEM and magnetic measurements.The effects of time and temperature on products were studied.The extension of the reaction time has no effect on the crystal,but only some tiny changes on the morphology of cobalt spheres and with the increasing of temperature,the cobalt crystal transforms from hcp-Co to fcc-Co.The cocercivity of the cobalt material obtained is up to 230 Oe which is higher than that of the available cobalt magnetic materials.In addition,this method has advantages such as relatively lower synthesis temperature,easier operation,shorter reaction time and lower power consumption.
magnetic material;solvothermal;cobalt microsphere
O612.8
A
1001-4861(2010)09-1685-05
2010-04-26。收修改稿日期:2010-06-23。
国家-广东联合基金(No.U0734005)和中央高校基本科研业务费专项资金(No.21610102)资助项目。
*通讯联系人。E-mail:tliuyl@jnu.edu.cn;会员登记号:S060017521P。
贺文启,男,25岁,硕士研究生;研究方向:纳米化学与纳米材料。
