奥硝唑氯己定洗剂微生物限度检查的方法学验证
2010-08-07朱庆玲黄海潮叶娟陈颖广东食品药品职业学院广州市510520
朱庆玲,黄海潮,叶娟,陈颖(广东食品药品职业学院,广州市510520)
奥硝唑氯己定洗剂为广东食品药品职业学院研制的新型复方制剂,用于细菌性阴道炎、滴虫性阴道炎和霉菌性阴道炎的治疗。该制剂中奥硝唑是第3代硝咪唑类衍生物,与甲硝唑相比,是一种疗效更高、疗程更短、耐受性更好的强力抗厌氧菌药物,其对于细菌性阴道炎、滴虫性阴道炎和霉菌性阴道炎的疗效优于甲硝唑及替硝唑[1,2];处方中另一有效成分醋酸氯己定则是广谱抗菌消毒药[3],具有较强的抗菌作用,2药合用疗效更为显著;此外制剂处方中加有山梨酸钾作为防腐剂。在研制过程中,笔者采用常规法进行微生物限度检查时,发现奥硝唑、氯己定和山梨酸钾的抑菌作用较强,不能消除其干扰,所以需要选择合适的方法。经查阅文献[4],发现这3种成分的水溶性较好,故认为采用薄膜过滤法过滤时抑菌成分可通过滤膜[5],而细菌被截留。决定根据0.22 μm滤膜可截留细菌的特性,选用薄膜过滤法来进行本品种的微生物限度检查。
根据《中国药典》2005年版(二部)附录ⅪJ微生物限度检查法[4],笔者对薄膜过滤法用于奥硝唑氯己定洗剂微生物限度检查进行了方法学验证。
1 材料
LX-B75L型高压灭菌锅(合肥华泰医疗设备有限公司);LRH-150型恒温培养箱(上海一恒科技有限公司);SHP-070型生化培养箱(上海实验仪器厂);HWS-24型恒温水浴锅(上海一恒科技有限公司);MSC-Advantage1.2生物安全柜(美国Thermo公司);0.22 μm醋酸纤维素微孔滤膜(直径:50 mm,上海新亚净化器件厂)。
奥硝唑氯己定洗剂(自制,批号:20090501,规格:醋酸氯己定1.2 mg·mL-1、奥硝唑0.2 mg·mL-1);pH 7.0氯化钠-蛋白胨缓冲液(自制,批号:20090501);0.9%无菌氯化钠溶液(自制,批号:20090501)。
营养琼脂培养基、营养肉汤培养基、改良马丁培养基、玫瑰红钠琼脂培养基、胆盐乳糖增菌培养基、改良马丁琼脂培养基、溴化十六烷基三甲铵琼脂培养基、甘露醇氯化钠琼脂培养基(广东环凯微生物科技有限公司)。
大肠埃希菌(ATCC8739)、金黄色葡萄球菌[CMCC(B)26003]、枯草芽孢杆菌[CMCC(B)63501]、铜绿假单胞菌(ATCC9027)、白色念珠菌(ATCC10231)、黑曲霉(ATCC16404),均购自广东微生物菌种保藏中心。
2 方法与结果
2.1 菌悬液制备
2.1.1 大肠埃希菌、金黄色葡萄球菌、枯草芽孢杆菌悬液。取3种菌的新鲜斜面培养物接种环置于10 mL营养肉汤培养基中,35℃培养18~24 h后取新鲜培养物1 mL加入9 mL 0.9%无菌氯化钠溶液中,10倍稀释至10-5~10-7,使成50~100 cfu·mL-1的菌悬液,备用。取白色念珠菌的新鲜斜面培养物接种环至10 mL改良马丁培养基中,经25℃培养18~24 h后取新鲜培养物1 mL加入9 mL 0.9%无菌氯化钠溶液中,10倍稀释至10-4~10-6,使为50~100 cfu·mL-1的菌悬液,备用。
2.1.2 黑曲霉悬液。取经改良马丁琼脂斜面培养基25℃培养1周的黑曲霉斜面培养物,加0.9%无菌氯化钠溶液l0 mL,将孢子洗脱,吸出孢子悬液,用垫有脱脂棉的漏斗(湿热灭菌)过滤,除去菌丝,收集孢子悬液至另一无菌试管内作为菌原液,取此孢子悬液1 mL加入9 mL 0.9%无菌氯化钠溶液中,稀释至10-4~10-5,使成50~100 cfu·mL-1的孢子悬液,备用。
2.2 供试品溶液的制备
称取本品10 mL至无菌锥形瓶中,加入灭菌后恒温至45℃的氯化钠-蛋白胨缓冲液100 mL,采用少量分次加入,并在加入的同时晃动锥形瓶,使供试品充分分散,充分振摇5 min,作为1∶10供试液。
2.3 微生物限度检查方法验证
2.3.1 试验组。取1∶10供试液10 mL,各5份,分别置于45℃的氯化钠-蛋白胨缓冲液100 mL中摇匀,在无菌操作下加入过滤器内,减压抽干后,用45℃氯化钠-蛋白胨缓冲液冲洗3次,每次100 mL。其中3份在最后一次的冲洗液中分别加入1 mL大肠埃希菌、金黄色葡萄球菌、枯草芽孢杆菌的菌悬液(约50~100 cfu·mL-1),过滤,将滤膜菌面朝上贴于营养琼脂培养基,倒置35℃培养48 h后取出进行菌落计数;其余2份加入1 mL白色念珠菌、黑曲霉的菌悬液(约50~100 cfu·mL-1),同法过滤,将滤膜菌面朝上贴于玫瑰红钠琼脂培养基,倒置于25℃培养72 h取出计数。
2.3.2 菌液组。取大肠埃希菌、金黄色葡萄球菌、枯草芽孢杆菌的菌液各1 mL(约50~100 cfu·mL-1),注入平皿中,立即倾注营养琼脂培养基,倒置35℃培养48 h后取出做菌落计数。取白色念珠菌、黑曲霉的菌悬液各1 mL(约50~100 cfu·mL-1),注入平皿中,立即倾注玫瑰红钠琼脂培养基,倒置于25℃培养72 h取出计数。
2.3.3 供试品对照组。取1∶10供试液10 mL 2份,分别置于45℃的氯化钠-蛋白胨缓冲液100 mL中摇匀,在无菌操作下加入过滤器内,减压抽干后,用45℃的氯化钠-蛋白胨缓冲液冲洗3次,每次100 mL。其中1份滤膜菌面朝上贴于营养琼脂培养基,倒置35℃培养48 h后取出做菌落计数;另1份同法过滤,将滤膜菌面朝上贴于玫瑰红钠琼脂培养基,倒置于25℃培养72 h取出计数,测量样品本底菌数。
2.3.4 稀释剂对照组。将供试液换成稀释剂(氯化钠-蛋白胨缓冲液),平行操作2张滤膜,将滤膜菌面朝上贴于培养基上,同“2.3.1”项下方法进行操作,考察稀释剂对试验有无干扰。
“2.3.1~2.3.4”项试验每次平行做2个平皿并重复进行3次独立平行试验。
分别计算各试验菌每次试验回收率,回收率的计算依据《中国药典》2005版附录ⅪJ相关要求[4],按照如下公式计算:
试验组的加菌回收率%=(试验组平均菌落数-供试品对照组平均菌落数)/菌液组平均菌落数×100%
稀释剂对照组的加菌回收率%=稀释剂对照组平均菌落数/菌液组平均菌落数×100%
本制剂的微生物限度检查法回收率结果见表1。
由表1可知,各类试验菌的回收率均大于70%,本试验方法不受制剂中抑菌成分的影响,可用于对制剂中细菌、霉菌、酵母菌数的检查。
2.4 控制菌检查方法的验证
2.4.1 供试液的制备。同“2.2”项下1∶10供试液的制备。
2.4.2 试验组。取1∶10供试液10 mL,置于稀释剂100 mL中摇匀,以无菌操作加入过滤器内,减压抽干后,用稀释剂冲洗3次,每次100 mL,然后取出滤膜,加入至100 mL增菌培养基中,然后加入1 mL控制菌(10~100 cfu·mL-1),其中金黄色葡萄球菌加入至营养肉汤增菌培养液中,铜绿假单胞菌加入至胆盐乳糖增菌培养液中,置于35℃下培养24 h。营养肉汤增菌培养液划线接种于甘露醇氯化钠琼脂培养基平板上,倒置于35℃下培养72 h观察结果;胆盐乳糖增菌培养液划线接种于溴化十六烷基三甲铵琼脂培养基平板上,倒置于35℃温度下培养48 h。均平行操作2个平皿,观察结果。
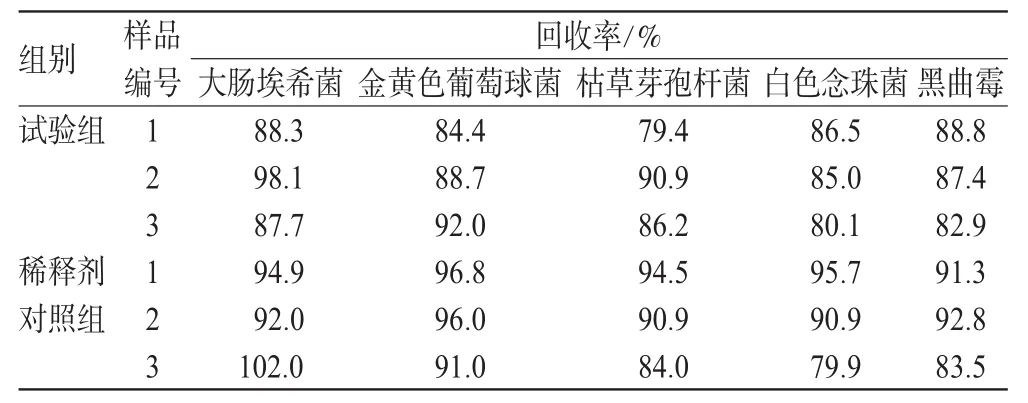
表1 微生物限度检查法回收率结果(n=3)Tab 1Recovery results of microbial limit test(n=3)
2.4.3 阴性菌对照组。取1∶10供试液10 mL,置于稀释剂100 mL中摇匀,以无菌操作加入过滤器内,减压抽干后,用稀释剂冲洗3次,每次100 mL,然后取出滤膜,加入到100 mL增菌培养基中,然后加入1 mL大肠埃希菌(10~100 cfu·mL-1),置于35℃下培养24 h。营养肉汤增菌培养液划线接种于甘露醇氯化钠琼脂培养基平板上,倒置于35℃下培养72 h观察结果;胆盐乳糖增菌培养液划线接种于溴化十六烷基三甲铵琼脂培养基平板,倒置于35℃温度下培养48 h。均平行操作2个平皿,观察结果。
铜绿假单胞菌和金黄色葡萄球菌控制菌方法验证结果见表2。
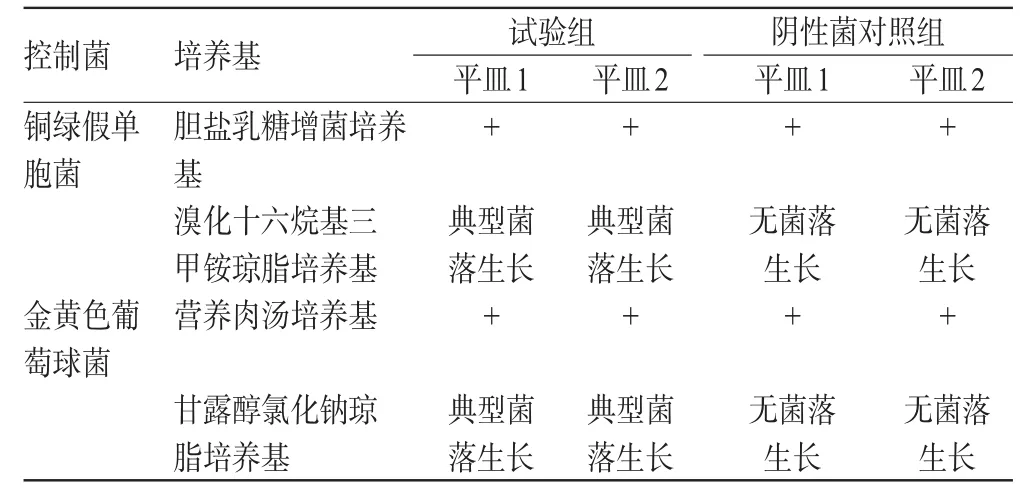
表2 铜绿假单胞菌、金黄色葡萄球菌控制菌方法验证结果Tab 2Validation test result of Pseudomonas aeruginosa and Staphylococcus aureus
由表2可知,试验组检出铜绿假单胞菌与金黄色葡萄球菌,阴性菌对照组无生长,说明本试验方法适用于该制剂中铜绿假单胞菌与金黄色葡萄球菌的检查。
3 讨论
试验中所用的菌株必须为标准菌株,其生物学特性应典型稳定,且所用菌株的传代不得超过5代;试验用的菌液最好存放在4℃下冷藏,在1个月内使用。
奥硝唑氯己定洗剂中的主药奥硝唑和氯己定抑制细菌能力很强,同时对酵母菌和真菌也有很强抑制作用,处方中还加有其它防腐剂导致对细菌也有抑制作用,但由于这3种成分在水中溶解度很好,故采用薄膜过滤法可将抑菌成分除去。
本试验结果表明,采用薄膜过滤法测定时,试验中各类菌的回收率均大于70%;因其为外用制剂,故对铜绿假单胞菌和金黄色葡萄球菌进行控制菌验证试验,结果阴性对照组均未检出阴性对照菌,试验组检出控制菌,可确定薄膜过滤法适用于奥硝唑氯己定洗剂的微生物限度检查。
[1]卢岩,葛卫红,谈恒山,等.复方奥硝唑凝胶的研制与质量控制[J].中国药房,2005,16(21):1630.
[2]王军,王增寿,朱光辉,等.奥硝唑的临床应用及不良反应[J].医药导报,2006,25(7):711.
[3]中华人民共和国卫生部药政局编.中国医院制剂规范[S].第2版.北京:中国医药科技出版社,1995:38.
[4]国家药典委员会编.中华人民共和国药典(二部)[S].2005年版.北京:化学工业出版社,2005:附录ⅪJ.
[5]王沁馨,周剑.双黄连口服液微生物限度检查法的验证[J].中国药房,2008,19(27):2125.
