调强放射治疗计划的剂量学验证
2010-06-08张玉海高杨
张玉海,高杨
解放军第309医院放疗科,北京,100091
调强放射治疗(IMRT)是在各辐射野与靶区外形一致的条件下,将每一个辐射野分割成多个细小的子野,使辐射野内的剂量强度按一定要求进行调节,最大限度地将束流集中到靶区,而使周围的危及器官或组织少受或免受不必要的照射。IMRT是利用MLC的运动来实现的,每一个辐射野内通过MLC的运动会产生一定数量的子野,而每一个子野的形状、跳数各不相同,它们之间存在着复杂的关系,所有这些子野合成以后的剂量分布是无法去想象和预见的,这一点与辐射野均匀的三维适形放疗完全不同[1]。因此,临床上为了保证调强射野输出剂量的准确性,必须对IMRT计划进行精心的设计与准确的剂量学验证。目前,以模体内剂量实测为基础的验证,仍然是当前最为常用的个体化IMRT计划的剂量学验证技术[2],其中点剂量验证和平面剂量验证结合使用可以较为全面地验证IMRT的剂量分布。自2009年8月到2009年12月,共有30多名患者在我科接受了IMRT治疗,按要求IMRT治疗实施之前,均需要对治疗计划进行剂量学验证,现将我科的IMRT计划验证方法总结报告如下。
1 材料与方法
1.1 设备和仪器
德国PTW公司生产的2D-729二维电离室矩阵,在27 cm×27 cm有效测量范围内均匀分布有729个电离室,每个电离室中心间隔10 mm。PTW UNIDOS E型剂量仪与30013型电离室(有效测量体积0.6cc)相匹配。测量使用Varian ClinacIX直线加速器的6MV X射线,剂量率为400MU/min。该加速器内置60对多叶准直器,中间40对叶片在等中心的投影宽度为0.5 mm,形成20 cm×20 cm的射野范围;外围20对叶片在等中心的投影宽度为1 mm,可形成的最大射野范围是40 cm×40 cm。另外,使用Varian公司的Eclipse8.0治疗计划系统和ARIA放疗网络。
1.2 调强计划设计
用热塑膜固定病人,并作好定位标记,进行CT模拟定位。将CT扫描图像传到治疗计划系统进行靶区和危及器官的勾画。设定靶区处方量及危及器官限量,用Eclipse进行逆向IMRT计划设计。计划产生后,放疗医师和放疗物理师通过各层面的剂量分布图及剂量体积直方图(DVH)评估计划。
1.3 模体计划设计
完成病人的IMRT计划后,因为无法直接在病人身体中进行剂量测量,因此必须把该计划移植到验证模体上,在模体上进行绝对剂量和相对剂量的测量,从而起到间接验证治疗剂量的作用。测量选用RW3固体水作为验证模体,其密度为1.045 g/cm3,与水的等效性好。
1.3.1 用于绝对剂量验证的模体计划设计
将2 cm厚带测量孔的固体水置于中间,下面放9块 1 cm厚的固体水,上面加10块1 cm厚的固体水,形成尺寸为40 cm×40 cm×21 cm的模体。然后把30013型指形电离室插入测量孔中,仿照患者在CT模拟机下以2.5 mm层厚扫描,在计划系统上进行影像重建,勾画模体外轮廓和电离室探头轮廓,设定电离室探头中心为坐标原点。此模体即作为所有治疗计划进行绝对剂量验证的模体。
利用Eclipse的创建验证计划功能,调用待验证的IMRT治疗计划,并将该计划的MLC叶片位置文件以及机架角度、准直器角度、射野跳数等相关治疗数据完全拷贝到模体上,其等中心点自动位于坐标原点处(即电离室中心位置),然后重新计算模体的剂量分布。由于电离室有一定体积,因此等中心测量点的绝对剂量取电离室探头体积剂量的平均值。
1.3.2 用于平面剂量验证的模体计划设计
在电离室矩阵上下各加4 cm和5 cm厚的固体水,根据矩阵侧面的“+”线确定其有效测量中心,并做好标记。将夹着矩阵的固体水在CT模拟机下以2.5 mm层厚扫描,同样在计划系统上进行影像重建,勾画模体外轮廓,确定坐标原点。此模体作为所有治疗计划进行平面剂量验证的验证模体。
用Eclipse创建平面剂量验证计划的方法与以上方法基本相同,所不同的是平面剂量验证计划需要将计划的机架角度、准直器角度和床角度都设为0°。如果想验证每个野的剂量分布情况,则需要将每个射野生成一个独立验证计划。这些设置在创建验证计划过程中只需要勾选相应的项目即可完成。重新计算各个射野在模体中的剂量分布,并导出各个射野在矩阵测量中心层面的剂量分布文件,作比较分析时用。
1.4 剂量学验证
在进行剂量学验证之前,先用PTW30013型0.6 cc电离室对Varian加速器6MV X线进行剂量校准,保证其出束偏差在1%以内。接下来进行绝对剂量验证和平面剂量验证。
1.4.1 绝对剂量验证
完全按照CT扫描的方式把模体(40 cm×40 cm×21 cm)摆放于加速器治疗床上,借助激光线将模体测量点调整到等中心位置,注意等中心位置应在第十块板(2 cm厚)测量孔的中心处,因为模体计划的测量点放在此处。将PTW30013型指形电离室插入测量孔中,连接PTW UNIDOS E型剂量仪,输入气压、温度及校准因子修正,依次执行各野照射,记录最终的测量值。
1.4.2 平面剂量验证
机架和准直器角度置于0°,PTW二维电离室矩阵放在5cm厚的固体水上方,参考激光线调整电离室矩阵,使其有效测量点位于等中心层面上,然后在上面加4 cm的固体水,考虑到电离室矩阵固有的5 mm测量深度,则SSD=95.5 cm。连接电缆,调出验证计划准备测量。运行MatrixScan软件,输入气压、温度值进行校准。对每个射野采集1次数据并保存。计划有多少个野就采集多少个数据文件。测量完毕后,用Verisoft软件将每个射野平面剂量分布的测量文件与计划文件对比分析,得出剂量分布的误差。
2 结果
表1给出6例IMRT计划的绝对剂量验证结果。将测量得到的等中心点剂量与计划平均剂量相比较得:百分相对误差=(测量剂量-计划平均剂量)/计划平均剂量,所得百分相对误差在±3%之内,则认为患者的治疗计划可以通过。否则,需要分析误差过大的原因,再次测量验证,直至验证计划通过方能治疗。第3例,第一次误差大于3%,第二次符合要求。

表1 绝对剂量验证结果Tab.1 The results of the absolute points dose verification
平面剂量验证误差分析采用Gamma分析方法[3-4],它是Verisoft软件中自动分析的工具,设置剂量误差标准和距离误差标准为3%/3 mm。验证通过与失败的标准是,测量点Gamma值≤1通过,Gamma值>1失败,通过的测量点数大于90%为照射野剂量分布验证通过。表2列出了6例患者计划验证结果,采用Gamma分析方法比较而获得的通过率情况。图1中(a)(b)(c)所示为一患者计算/测量等剂量线分布情况比较及Gamma分析结果。

表2 平面剂量验证结果Tab.2 The results of the plane dose distribution verification
3 讨论
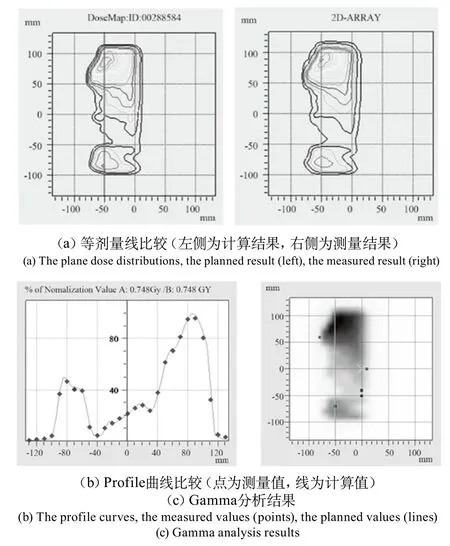
图1 二维电离室矩阵测量与计划计算结果比较分析Fig.1 The comparison of the planned and the measured values with 2DArray ion chamber
从以上绝对剂量的验证结果可以看出,测量值都比计划值偏小,说明有系统误差存在,该结论与戴建荣等[5]报道结果一致。究其原因,我们认为IMRT射野中经常会包含一些面积很小的子野,在实际测量中,只有少数子野的射野区域包含测量点,即测得的是该子野的主射线,而对于大多数子野,只测得其边缘剂量或散射剂量,这部分剂量通常较小,宜采用小灵敏体积的电离室测量[6],以得到更加精确的结果。另外,我们进行绝对剂量验证采用患者治疗的实际照射角度,因此验证过程中还存在治疗床板和横梁对剂量的衰减。表1中第3例计划经过两次验证方才通过,第一次验证结果误差>5%,分析发现可能的原因是射线穿过横梁发生衰减;第二次验证过程中,移动横梁位置避免射野穿过横梁,发现验证结果偏差明显减小(<1%)。可见治疗床的衰减对验证结果的影响还是不容忽视的。综合以上分析,笔者认为虽然各种原因导致测量结果偏小,但是误差仍然是在临床可以接受的范围内(<3%),因此以上的测量方法和测量结果是可信的。
关于绝对剂量验证测量点位置选择的基本原则是选择剂量均匀、梯度较小的点。简单的判定方法是电离室探头的(最大剂量- 最小剂量)/ 平均剂量的值小于10%。通常等中心点是作为绝对剂量验证的首选位置。表1中第1-5例计划测量点均满足上述条件,并且测量点均为计划的等中心点。但是,有些计划的等中心点在靶区边缘或在靶区外,比如鼻咽癌IMRT计划,它的等中心点就不适合作为测量点。为此需要适当调整模体计划中的等中心位置,使模体中测量点位于高剂量低梯度区域,这样可减少因测量点处剂量变化太大而导致测量结果不准确。表1中第6例计划(鼻咽癌)就是因为计划的等中心点位于靶区外的低剂量区,无法准确测量。笔者通过移动计划的等中心位置,使测量点位于高剂量低梯度区域,完成绝对剂量的验证。
二维电离室矩阵是目前较先进的调强验证系统之一,它可以测量照射野的剂量分布和强度分布,利用它可以极大地简化验证工作量,提高验证的效率。大量研究表明,用二维电离室矩阵进行IMRT计划验证是可行的[7-8]。笔者利用PTW729二维电离室矩阵对IMRT计划的验证结果显示,平面剂量分布的计算值和测量值之间具有良好的一致性,Gamma分析的点通过率均在90%以上。值得一提的是,本研究选取最大剂量的10%作为有效测量点的最低剂量限值,其原因有二:一是电离室矩阵在低剂量区域的测量误差明显增大;二是低剂量区主要是动态MLC散射剂量形成。对于TPS来讲,散射剂量的计算不可能与开放野内的剂量计算一样精确。
综上所述,由于IMRT有着肿瘤靶区剂量分布高度适形和高梯度变化的特点,为确保治疗剂量能够精确地定位在肿瘤区域,严格的个体化剂量学验证是治疗执行前的一项重要工作[9]。笔者利用已有的设备条件,建立了患者调强放射治疗计划的剂量学验证方法,并取得了值得信赖的结果。随着设备条件的改善和经验的积累,调强计划的剂量学验证方法还会得到进一步完善。
[1]胡逸民, 主编.肿瘤放射物理学[M].北京:原子能出版社, 1999,538-548.
[2]马金利, 蒋国樑.调强适形放射治疗剂量学验证体系的建立[J].中国肿瘤, 2004, 13(8): 485-489.
[3]Low D, Harms W, Mutic S, et al.A technique for the quantitative evaluation of dose distributions[J].Med Phys, 1998,25:656-661.
[4]Depuydt T, Van Esch A, Huyskens D, et al.A quantitative evaluation of IMRT dose distribution: refinement and clinical assessment of the gamma evaluation[J].Radiother oncol, 2002,62:309-319.
[5]戴建荣, 胡逸民, 张红志, 等.针对患者调强放射治疗计划的剂量学验证[J].中华放射肿瘤学杂志, 2004, 13(3): 229-233.
[6]Low DA, Gerber RL, Mutic S, et al.Phantoms for IMRT does distribution measurement verification[J].Int J Radiat Oncol Biol Phys, 1998, 40:1231-1235.
[7]Jursinic PA, Nelms BE.A 2-D diode array and analysis software for verification of intensity modulated radiation therapy delivery[J].Med Phys, 2003, 30(5):870-879.
[8]Poppe B, Blechschmidt A, Djouguela A, et al.Two-dimensional ionization chamber arrays for IMRT plan verification [J].Med Phys, 2006, 33(4): 1005-1015.
[9]姜瑞瑶.调强放射治疗技术及其质量保证[J].医疗卫生装备,2006, 27(7): 63.
