HPLC法同时测定黄芩中5种黄酮类成分的含量Δ
2010-05-22阚红玉宋殿荣王跃飞潘桂湘戚爱棣教育部方剂学重点实验室天津市中药化学与分析重点实验室天津中医药大学中医药研究院天津市300193
阚红玉,宋殿荣,王跃飞,潘桂湘,戚爱棣(教育部方剂学重点实验室/天津市中药化学与分析重点实验室/天津中医药大学中医药研究院,天津市 300193)
黄芩为唇形科植物黄芩Scutellaria baicalensis Georgi.的干燥根[1],性寒,味苦,具有清热燥湿、除火解毒、止血安胎的作用。目前,市场流通的商品黄芩除来自野生的和栽培的黄芩之外,有些地方还将根断面为黄色的黄芩属(Scutellaria)的多种植物作黄芩药用,如粘毛黄芩(S.viscidula Bge.)、滇黄芩(S.amoena C.H.Wright)、甘肃黄芩(S.rehderiana Diels)等[2]。
黄芩中有效成分主要是黄酮类化合物。近年研究发现,除黄芩苷外,其它黄酮类化合物如黄芩素、汉黄芩苷以及汉黄芩素等同样具有重要的药理活性。其中,黄芩素具有抗氧化、抗菌、抗病毒、抗肿瘤等作用;汉黄芩苷具有抗菌、抗病毒、凝血等作用;汉黄芩素具有抗炎、解热的作用;此外,黄芩素、黄芩苷、汉黄芩素对紫外线照射产生的氧化作用有明显的抑制作用,而黄芩及其有效成分解热、保肝和防辐射、抑制凝血酶引起的血小板凝聚等作用也有很多报道[3~5]。
2005年版《中国药典》在黄芩药材项下,仅对黄芩苷单一成分进行质控。鉴于此,本试验建立同时测定黄芩中黄芩苷、汉黄芩苷、黄芩素、汉黄芩素和千层纸素A 5种黄酮类有效成分含量的方法,并分析天津市15家零售药店的黄芩药材中黄酮类有效成分的差异,为综合评价黄芩药材的质量提供参考。
1 仪器与试药
1100型高效液相色谱(HPLC)仪,包括四元溶剂泵、脱气机、自动进样器、柱温箱、光电二级管阵列检测器及软件(美国Agilent公司);AX205型十万分之一天平(瑞士Mettler Toledo公司);BP121S型万分之一天平(德国Satorius公司);KQ-250E型超声波清洗器(昆山市超声仪器有限公司)。
黄芩苷(批号:110715-200212)、黄芩素(批号:111595-200604)、汉黄芩素(批号:1514-200202)对照品购于中国药品生物制品检定所;汉黄芩苷(批号:061012,纯度≥99%)、千层纸素A(批号:060530,纯度≥99%)标准品购于上海友思生物科技公司;黄芩饮片购自天津市内6区15家零售药店,经天津中医药大学中药学院生药学教研室李天祥副教授鉴定均为唇形科植物黄芩S.baicalensis Georgi.的干燥根;甲醇、乙腈为色谱纯,甲酸为分析纯,水为超纯水。
2 方法与结果
2.1 色谱条件
色谱柱:Agilent Zorbax SB-C18(150 mm×4.6 mm,5 μm);流动相:0.1%甲酸水溶液(A)-0.1%甲酸乙腈(B),梯度洗脱(0~10 min,22%~25%B;10~20 min,25%~40%B;20~22 min,40%~45%B;22~27 min,45%B;27~28 min,45%~60%B);检测波长:278 nm;流速:1.0 mL·min-1;柱温:20 ℃;进样量:10µL。在此色谱条件下,分别取对照品混合溶液及供试品溶液进样。结果,黄芩苷、汉黄芩苷、黄芩素、汉黄芩素、千层纸素A与其它组分均能达到基线分离,保留时间分别为10.03、16.27、20.93、26.54、27.82 min。色谱见图1。
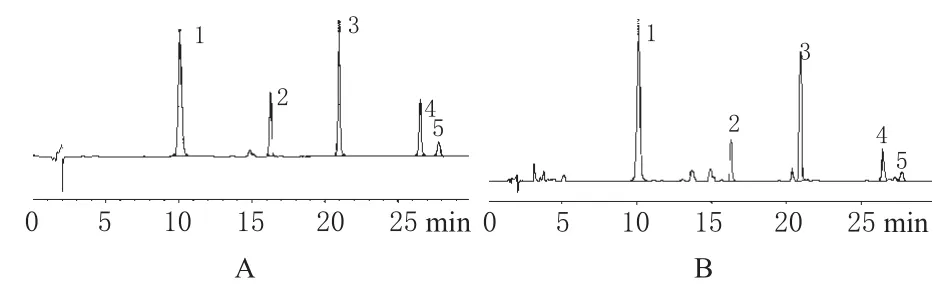
图1 高效液相色谱图A.混合对照品;B.供试品;1.黄芩苷;2.汉黄芩苷;3.黄芩素;4.汉黄芩素;5.千层纸素AFig 1 HPLC ChromatogramsA.mixed reference substance;B.test sample;1.baicalin;2.wogonoside;3.baicalein;4.wogonin;5.oroxylinA
2.2 混合对照品溶液的制备
分别精密称取对照品(或标准品)黄芩苷16.04 mg、汉黄芩苷5.17 mg、黄芩素7.38 mg、汉黄芩素4.58 mg、千层纸素A 1.32 mg,置于10 mL容量瓶中,用70%甲醇溶解并稀释至刻度,得对照品贮备液,4℃冷藏,备用。分别精密移取各成分对照品贮备液适量,置于同一10 mL量瓶中,加70%甲醇定容,摇匀,即得黄芩苷、汉黄芩苷、黄芩素、汉黄芩素、千层纸素A浓度分别为272.7、67.21、118.1、50.38、18.48 μg·mL-1的混合对照品溶液。
2.3 供试品溶液的制备
精密称取黄芩药材粉末(过80目筛)0.2 g,置于25 mL容量瓶中,加入70%甲醇至2/3刻度处,超声提取10 min,冷却至室温后定容,摇匀,静置,取上清液1 mL,置于10 mL容量瓶中,70%甲醇定容,摇匀,用0.45 μm微孔滤膜过滤,取续滤液10 μL注入液相色谱仪。
2.4 线性关系考察
精密移取混合对照品溶液适量,分别制备含黄芩苷浓度为8.52、17.0、34.1、68.2、136.3、272.7 μg·mL-1,汉黄芩苷浓度为2.10、4.20、8.40、16.8、33.6、67.2 μg·mL-1,黄芩素浓度为3.69、7.38、14.8、29.5、59.0、118.1 μg·mL-1,汉黄芩素浓度为 1.57、3.15、6.30、12.6、25.2、50.4 μg·mL-1,千层纸素A浓度为0.58、1.16、2.31、4.62、9.24、18.5 μg·mL-1的混合对照品溶液,摇匀。吸取上述混合对照品溶液各10 μL注入液相色谱仪,按“2.1”项下色谱条件进行分析。以对照品进样量(X)为横坐标,峰面积积分值(Y)为纵坐标,制备标准曲线,得5种成分的回归方程。结果表明各成分在相应进样量范围内与各自峰面积积分值呈良好线性关系。线性关系考察结果见表1。
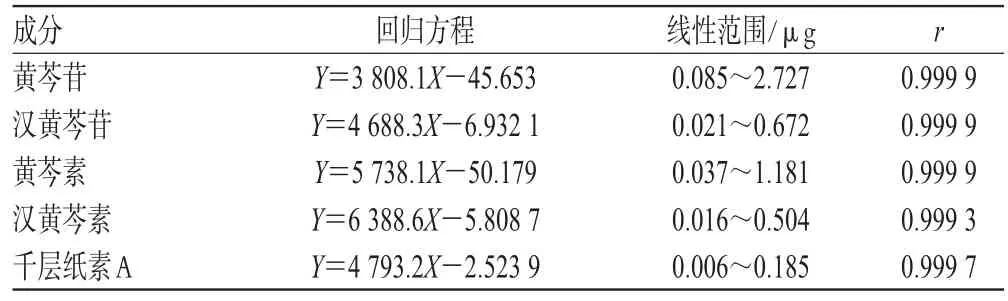
表1 线性关系考察结果(n=6)Tab 1 Linear relation of peak area and concentration(n=6)
2.5 精密度试验
精密吸取同一混合对照品溶液10 μL,按“2.1”项下色谱条件重复进样6次。结果,黄芩苷、汉黄芩苷、黄芩素、汉黄芩素和千层纸素A峰面积的RSD分别为0.25%、0.26%、0.20%、0.24%、0.25%,表明仪器精密度良好。
2.6 稳定性试验
取同一供试品溶液,于室温放置0、2、4、6、8、10、12 h,精密吸取10 μL进样分析,考察溶液稳定性。结果,黄芩苷、汉黄芩苷、黄芩素、汉黄芩素和千层纸素A 12 h内峰面积的RSD分别为0.44%、0.58%、0.43%、0.66%、1.22%,表明供试品溶液在12 h内稳定性较好。
2.7 重复性试验
精密称取同一药材粉末6份,分别按“2.3”项下方法制备供试品溶液,按“2.1”项下色谱条件进行分析。结果,黄芩苷、汉黄芩苷、黄芩素、汉黄芩素和千层纸素A的平均含量分别为67.19、9.584、25.29、6.204、2.696 mg·g-1,RSD 分别为 2.19%、2.26%、2.75%、2.01%、1.69%,表明方法重复性良好。
2.8 加样回收率试验
取已知含量的样品6份,分别精密加入一定量黄芩苷、汉黄芩苷、黄芩素、汉黄芩素和千层纸素A对照品(或标准品),按“2.3”项下方法制备供试品溶液,按“2.1”项下色谱条件测定,计算加样回收率,结果见表2。

表2 加样回收率试验结果(n=6)Tab 2 Results of recovery test(n=6)
2.9 样品含量测定
取天津市15家零售药店黄芩样品粉末各0.2 g,按“2.3”项下方法制备供试品溶液,按“2.1”项下色谱条件测定峰面积,并用外标法计算样品中黄芩苷、汉黄芩苷、黄芩素、汉黄芩素和千层纸素A的含量,结果见表3。
3 讨论
本试验以黄芩药材的多组分分离为目的,尽可能在同一色谱条件下分离黄芩中多个成分,故对流动相溶剂系统及柱温进行了考察。由于甲醇-水系统的分析时间长于乙腈-水系统,且分离效果稍差,故采用乙腈-水系统,并加入少量甲酸改善峰形,即A为0.1%甲酸水溶液,B为0.1%甲酸乙腈。柱温在15、20℃时分离效果无明显差别,30℃时分离效果差,故最终确定柱温为20℃。

表3 天津市内6区15家零售药店黄芩饮片含量测定结果Tab 3 Results of content determination of S.baicalensis decoction from 15 retail drug stores of six districts in Tianjin
2005年版《中国药典》规定,黄芩药材含黄芩苷不得少于9.0%。本试验选择的15家零售药店中,若以黄芩苷来评价黄芩药材优劣(表3以此高低排序),其中仅有9家药店出售的黄芩中黄芩苷含量高于9.0%,不合格率高达40%;且黄芩苷的含量最高11.03%,最低2.63%,相差近5倍,表明天津市内零售黄芩药材质量参差不齐,且相差较大。药材质量的优劣直接关系药效的好坏,故应引起临床用药部门的重视。
若采用单一成分含量进行评价,如河西A药店和河北B药店,以黄芩苷计属不合格药材,但其黄芩素含量则为最高和次高;黄芩苷含量最高的红桥A药店,另4种成分含量却非相应最高。这说明仅以单一成分作为质量控制的指标存在一定的局限性,也说明了本试验建立同时测定黄芩药材中5种黄酮类有效成分含量方法的必要性。
本试验首次采用HPLC-梯度洗脱法同时测定黄芩药材中黄芩苷、黄芩素、汉黄芩苷、汉黄芩素、千层纸素A 5种黄酮类有效成分的含量,并分析了天津市内6区15家零售药店黄芩药材有效成分的差异,方法准确、简便、重复性好,可为黄芩药材的质量控制及安全、合理应用提供试验依据。
[1]国家药典委员会编.中华人民共和国药典(一部)[S].2005年版.北京:化学工业出版社,2005:231.
[2]肖丽和,王红燕,李发美,等.不同来源黄芩药材HPLC指纹图谱比较[J].沈阳药科大学学报,2004,21(1):28.
[3]孙娇月,孙维亮.黄芩黄酮对脑线粒体损伤的保护作用[J].实用中医药杂志,2004,19(3):101.
[4]高中洪,黄开勋,徐辉碧.黄芩黄酮对H2O2导致的神经细胞损伤的保护作用[J].中国药理学通报,2000,16(5):589.
[5]王新华,何红梅,张延霞,等.黄芩苷对异烟肼和利福霉素钠肝损伤小鼠的保护作用研究[J].中国药房,2007,18(28):2175.
