Rh弱 D、Del的检测及临床意义探讨
2010-03-21孔庆芳谭庆芬
杨 珊,孔庆芳,谭庆芬
(广西壮族自治区血液中心,广西 柳州 545005)
Rh血型系统是人类红细胞血型系统中最为复杂且最具多态性的系统,在临床的重要性仅次于ABO血型系统,Rh(D)阴性者接受 Rh(D)阳性的血液,可能产生抗 -D导致免疫性输血反应。因此,正确检定 Rh(D)阴性个体,排除 Rh弱 D、Del的个体,建立真正的 Rh(D)阴性献血者库尤显重要。现将我们的检测结果报道如下:
1 资料与方法
1.1 一般资料 2003年 1月至 2010年 1月我院采用常规血清学方法初筛为 Rh(D)阴性样本 341例,进一步用间接抗人球蛋白试验检测弱 D,应用三氯甲烷/三氯乙烯吸收放散法检测 Del。302例中144例确证为 Rh(D)阴性者及 16例 Del型进行了Rh系统其他抗原的测定。
1.2 试剂 IgM抗 -D,IgG抗 -D试剂(上海血液生物医药有限责任公司,北京金豪制药有限公司,Biotest),IgM抗 -C、抗 -c、抗 -E、抗 -e试剂(上海血液生物医药有限责任公司),三氯甲烷(成都正达化学试剂有限公司),三氯乙烯(广东光华化学试剂有限公司)。
1.3 方法 Rh(D)阴性筛选及确认:用 3批不同生产厂家、不同批号的单克隆 IgM抗 -D试剂作盐水法试验,未出现凝集者用 3批不同生产厂家、不同批号的单克隆 IgG抗 -D试剂作间接抗人球蛋白试验。出现凝集者判为弱 D,未出现凝集者用 3批不同生产厂家,不同批号的单克隆 IgM抗 -D试剂及 3批不同生产厂家、不同批号的单克隆 IgG抗 -D试剂作三氯甲烷/三氯乙烯吸收放散试验:将充分洗涤的两份压积红细胞 0.5 ml,1份加入 0.5 ml混合 3批不同生产厂家、不同批号的单克隆 IgM抗 -D试剂(置 4°C孵育 1 h),另 1份加入 0.5 ml混合 3批不同生产厂家、不同批号的单克隆 IgG抗 -D试剂(置 37°C孵育 1 h),每隔 10 min摇匀一次。洗涤吸收抗 -D后的红细胞 7次,末次洗涤后弃尽上清,加入与之等体积的生理盐水,再加入与之等量的三氯甲烷/三氯乙烯(1∶1)混合液。加盖振摇 30 s,颠倒混匀 30 s,开盖后 37°C水浴 5 min,3 000 r/min离心后取上清液,与 Rh(D)阳性细胞分别在盐水、抗人球蛋白介质中反应,出现凝集者为 Del型。
2 结 果
初筛为 Rh(D)阴性样本 341例中,检出弱 D 23例 ,占 6.7%,Del 16例 ,占 4.7%,确证 Rh(D)阴性302例 ,占 88.6%。
144例确证为 Rh(D)阴性及 16例 Del型个体Rh系统表型分布见表 1。
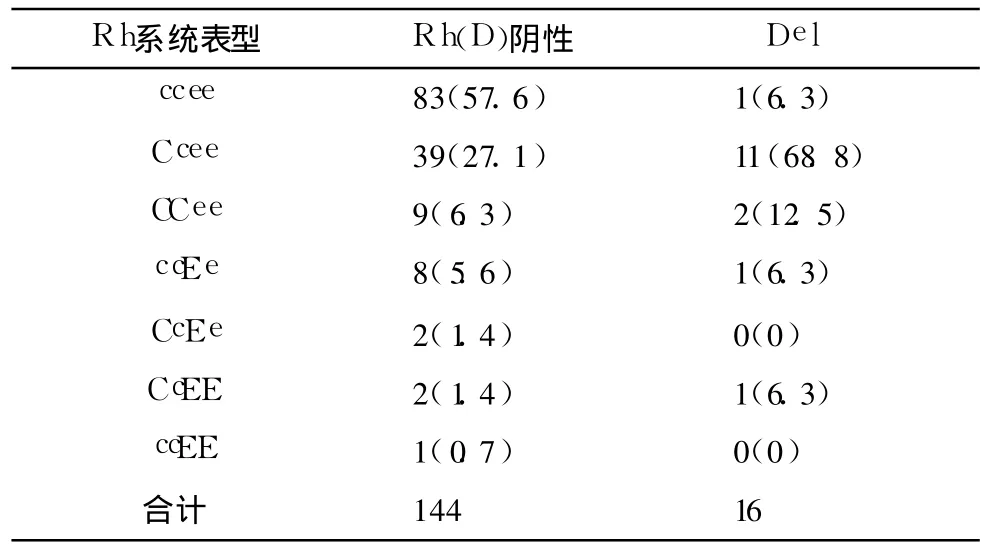
表1 144例确证为 Rh(D)阴性及 16例Del型个体 Rh系统表型分布[例(%)]
Rh(D)阴性者中 ccee最多,占 57.6%,其次是Ccee,占 27.1%。Del型中 Ccee最多,占 68.8%,其次是 CCee,占 12.5%。
3 讨 论
D抗原分阳性和阴性两大类,阳性中包括正常D与变异 D,变异 D中又包括弱 D和部分 D,而 Del属弱 D。弱 D型、部份 D型、Del型在初筛时一般为阴性,如果不进一步用间接抗人球蛋白试验及吸收放散试验会漏检。血液中心或血站在建立 Rh(D)阴性稀有血型库时,采用间接抗人球蛋白试验筛出弱 D型,但一般不采用吸收放散试验筛出 Del型。有报道 Del型血液输给 Rh(D)阴性受血者有可能被免疫产生抗 -D[1-2]。弱 D型、Del型个体作为献血者,其血液应当作 Rh(D)阳性血使用,而作为受血者,则应视为 Rh(D)阴性而输注 Rh(D)阴性血液,以确保安全、有效输血。因此检测弱 D型、Del型有利于建立真正的 Rh(D)阴性献血者库,保障输血安全。同时有必要为弱 D型、Del型人群建立档案,并应告之作为受血者输血时应输注 Rh(D)阴性血液。
Del型是非常弱的 D抗原,可以在约 30%的 Rh(D)初筛阴性个体中检出[3],我们从 341例初筛为Rh(D)阴性样本中检出 Del型 16例,占 4.7%。国内报道湖北地区占 22.67%[4],海南地区占20.65%[5],安徽地区占 15.6%[6]。我们检测的结果偏低于所见的报道,可能是我们检测的数量较少,还有待进一步证实。但从报道中可以看出 Del型分布存在一定的地区差异。
确认部分 D需要一组针对全部 D表位的单抗来检测,因条件所限,我们仅采用 3批 IgM抗 -D、3批 IgG抗 -D单克隆试剂,假如这些试剂是针对不同的 D表位,其结果仅可提示而不能确定是部分 D。检测弱 D型、Del型时宜采用不同生产厂家多种抗 D试剂,避免漏检。
检出 Rh(D)阴性者中 ccee最多,占 57.6%,其次是 Ccee,占 27.1%。Del型中 Ccee最多,占68.8%,其次是 CCee,占 12.5%。有报道[7]Del型与C抗原相关。Okuda等[8]报道,在日本 Rh(D)阴性供血者中,27.7%存在 RhD基因,同时发现具有RhD基因的 Rh(D)阴性个体表型为 CC或 Cc。在我们的检测结果中 Del型检出比例较多者含 CC及Cc抗原,但因检测数量较少,有待进一步证实。
[1] Wagner T,Kormoczi GF,Buchta C,et al.Anti-D immunization by DEL red blood cells[J].Transfusion,2005,45(4)∶520-526.
[2] Yasuda H,Ohto H,Sakuma S,et al.Secondary anti-D immunization by Del red blood cells[J].Transfusion,2005,45(10)∶1 581-1 584.
[3] 王晓珠,兰炯采,吴绪华,等.Rh弱 D及 Del样本的检测研究[J].中国实验血液学杂志,2005,13(3)∶509-511.
[4] 沈 钢,章俊华,张 浩,等.湖北汉族 RhD阴性个体 Rh表型及 RhD基因多态性研究[J].中国输血杂志,2007,20(4)∶304-306.
[5] 叶建忠,杨向萍,蔡于旭,等.海南汉族 RhD阴性个体 RhD基因研究[J].中国输血杂志,2005,18(2)∶97-100.
[6] 蔡玲君,丁 权,陈文仙,等.云南地区 RhD阴性个体 RhD基因研究[J].中国输血杂志,2006,19(6)∶452-453.
[7] 陈善华,丁 琪,杨育红,等.洛阳地区 RhD阴性无偿献血者表型分布调查[J].中国输血杂志,2009,22(11)∶921-922.
[8] Okuda h,Kawano M,Iwamoto S,et al.The RhD gene is higly detectable in Rhd-negative Japanese donors[J].J in Invest,1997,100(2)∶373-379.
