Ⅲc期乳腺癌的诊断与治疗
2010-03-21海南省人民医院肿瘤医学部乳腺癌专业组钟晓捷执笔
海南省人民医院肿瘤医学部乳腺癌专业组钟晓捷,汤 鹏,李 高,陈 茹 执笔
(海南省人民医院肿瘤医学部,海南 海口 570311)
1 病例摘要(一)
患者,女性,73岁,于 2006年 4月 2日体检发现左侧乳房肿块,质硬,不易被推动,大小约 3.0 cm×1.5 cm,无压痛,无乳头溢血,皮肤无“橘皮样”改变,无纳差、体重下降,无畏寒发热。门诊彩超检查示左侧乳腺实性肿物,左侧腋窝及左锁骨上窝淋巴结肿大,考虑乳腺癌并转移癌,行肿物穿刺,病理诊断为“乳腺浸润性癌”。为进一步明确诊断和治疗来我院。发病以来食欲睡眠良好,大小便正常。
既往有高血压病史 10余年,服“洛丁新”。无糖尿病史,无肝炎、结核等传染病病史;无手术、外伤史;否认输血史;无吸烟酗酒史;无药物过敏史。已婚 40余年,月经52岁;无肿瘤家族史。
专科体查:左乳外上象限可触及一肿块,大小3.0 cm×1.5 cm,边界不规则,不易被推动,无压痛,右侧乳房未触及肿块,左腋下可触及数个肿大淋巴结,质地硬,无压痛,可推动,最大直径 2.0 cm。左锁骨上窝可触及数个肿大淋巴结,质地硬,无压痛,不易推动,最大直径 1.0 cm×1.5 cm。
辅助检查:2006年 4月 4日穿刺病理报告见纤维组织中片巢状的异型细胞浸润,形态特征符合乳腺浸润癌。免疫组化检测:雌激素受体(ER)(15%细胞阳性),孕激素受体(PR)(-),癌因子(C-erbB-2)(++)。
2006年 4月 10日骨扫描:全身骨显像未见典型肿瘤转移征象。第五腰椎骨质代谢异常,考虑退行性变。
2006年 4月 11日胸部 CT平扫:左侧乳房边缘模糊,稍高密度结节,符合乳腺癌。双侧腋窝小结节,考虑淋巴结肿大;双侧肺野及纵膈未见异常。
实验室检查:血常规、血生化、多肿瘤标志物检测未见异常。
2006年 4月 14日 PET-CT检查:左乳腺癌并左锁骨上淋巴结转移。
术前 CT检查见图 1。

图1 术前 CT片
术前 PET-CT检查见图 2。
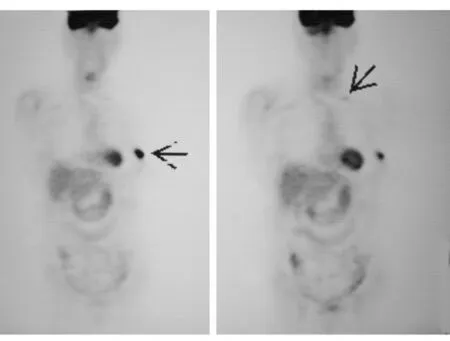
图2 术前 PET-CT片
2 讨 论(一)
问题:治疗前的检查是否完善?
(海南省人民医院)周卫平主任:该病例治疗前的检查存在较大缺陷。应用乳腺钼靶片检查,并且该病者为较晚期病人,如有条件,应该做 MRI检查[1]。若考虑新辅助化疗,应行腋窝 LN(腋窝淋巴结)、锁骨上 LN穿刺[2]。
旁述:中国抗癌协会乳腺癌诊疗指南共识:新辅助化疗前,肿大区域淋巴结须穿刺病理证实[1]。
问题:如果该患者新辅助化疗,PET-CT已证实乳腺癌淋巴结转移,是否肿大淋巴结仍需穿刺病理证实?若不考虑费用,原发灶病理是空心针或组织(Mammatone)获取?
(广东省人民医院)廖宁主任:即使 PET-CT检查证实淋巴结转移,新辅助化疗前肿大淋巴结仍需穿刺病理证实。目前主张空心针获取术前化疗的病理[2]。
问题:分析该病人的临床分期?
(海南省人民医院)谢贤和主任:肿瘤最大直径3.5 cm,为 T2;同侧锁骨上淋巴结转移,为 N3。TNM分期 T2N3M0,为 IIIc期[1]。
旁述:对于同侧锁骨上淋巴结转移,第五版《癌症分期手册》上定义为 M1,但临床治疗证明,这部分病例若无其他全身转移的证据,经联合治疗常获得长期生存,预后与 III期病例相似,因此重新划归为N3,分期为Ⅲ c期(任何 T,N3)[1]。
问题:如何评价细针穿刺获取的细胞学诊断,能否作为新辅助化疗的依据?
(海口市人民医院)刘新梅主任:细胞学诊断准确性为 90%,并且不能获得组织学的诊断,也无法知道 ER、PR、Her-2等情况,不能作为新辅助化疗的依据。
3 病例摘要(二)
2006年 4月 11日海南省人民医院组织院内大会诊。
综合意见:(1)诊断为左乳腺癌,腋窝、锁骨上淋巴结转移可能性大。(2)肿外:晚期患者,目前暂不手术,可先行化疗,选“泰素帝 +赫赛汀”,观察化疗情况后再考虑是否手术。(3)肿内:目前不考虑手术,化疗为首选,如有效,则考虑手术或放疗;如无效,考虑内分泌治疗。化疗方案为“多西他赛 +恩环类 +赫赛汀”。放疗科:建议先化疗,单纯放疗不能解决问题。(4)鉴于病人情况特殊,请外院专家会诊,确定治疗方案。
2006年 4月 12日中山医科大学肿瘤医院内科教授会诊。
综合意见:(1)主张先做 PET-CT检查,了解腋窝、锁骨上是否为癌转移,以及全身其他部位是否有转移灶。(2)若无肺、肝、骨骼等转移,主张先行手术(改良根治术)。(3)目前病人状况应能耐受手术,否则延长手术时间,化疗后病人一般情况更差,以及化疗无效,局部病灶增大后失去手术机会。(4)病灶超过 2 cm,建议术后辅助治疗,方案为 AC或 CAF 4-6周期,化疗后加局部(锁骨上窝)放疗,放化疗后再考虑内分泌治疗。
2006年 4月 14日广东省人民医院肿瘤中心乳腺外科会诊。
综合意见:(1)结合病史及 PET-CT检查,诊断为左乳腺癌伴左腋窝、左锁骨上窝淋巴结转移。(2)建议新辅助化疗,方案“泰素帝 +法玛新”,病人为高龄患者,剂量酌减,泰素帝 60 mg/m2,法玛新 70 mg/m2[4-9]。(3)若条件许可,做荧光原位杂交(FISH)试验,考虑合用赫赛汀。(4)观察化疗疗效后再定手术方案。
4 讨 论(二)
问题:先手术后化疗?先化疗后手术?
(农垦总局医院)吴煌福主任、王琳主任、(海口市保健院)刘安主任:
病人为Ⅲc期患者,属局部晚期。新辅助化疗是局部晚期乳腺癌治疗的标准组成部分,建议先化疗后,再根据病情定治疗方案。
旁述:NCCN指南明确指出,局部晚期是新辅助化疗的主要适应证[1]。
治疗经过:
患者于 2006年 4月 18日起开始执行新辅助化疗,方案为“泰素帝 +法玛新”,结束 4个周期化疗后,检查显示左乳肿块明显缩小(1.0 cm×0.9 cm),左腋窝未扪及肿大淋巴结,左锁骨上窝肿大淋巴结明显缩小(0.8 cm×0.6 cm),易推动。2006年 7月24日在硬外麻下行左乳腺癌改良根治术,术后病理见:成片小细胞浸润,核小,胞浆红染,另有部分管状和散在的畸形核细胞,胞浆肿胀变性,免疫组化符合小叶浸润癌。左腋窝淋巴结 0/17,胸小肌内侧淋巴结 0/3,均未见转移。术后恢复好。2006年 9月 11日起,继续同方案术后辅助化疗两个周期。2006年10月 22日转入放疗科补充锁骨上区放疗。放疗结束后,一直予内分泌治疗(来曲唑 2.5 mg,qd),随访至今,无复发转移征象。
问题:新辅助化疗方案的选择——常用方案?
谢贤和主任:对于新辅助化疗的方案,必须是术后辅助化疗检验安全有效的方案,该病人我还是主张用“紫杉 +蒽环”的方案[2]。
钟晓捷主任:我同意谢主任的观点,中科院肿瘤医院 3年 400多例的临床试验[10],AC方案有效率不足 80%,PCR为 8%;“紫杉类 +蒽环”方案安全性好,有效率接近 90%,PCR达 20%。在保证安全的前提下,尽量选择现代有效、能达到更高 PCR的方
案[3,5]。
问题:新辅助化疗周期数?
刘新梅主任:主要看化疗的有效性而定,若化疗后肿瘤明显缩小,通常给予 4-6周期化疗[2]。
问题:若两个周期后化疗无效,手术还是换化疗方案?
吴煌福主任:病人年纪大,较晚期,可考虑更换化疗方案,观察疗效后再定治疗方案。
王琳主任:亦可考虑精确的放疗以局部控制[6]。
问题:四个周期后化疗,若术后病理 PCR,是否继续化疗?
王琳主任:化疗后原发灶术后病理 PCR,说明化疗药物对该病者敏感有效,但并不代表外周微小病灶已消灭,所以应予原有效方案补充 2-4周期化疗。当然,前提是病人能耐受[11]。
问题:如果该病人强烈要求保乳,能否做保乳?
刘安主任:只要病人强烈要求,化疗后肿块已明显缩小,病人接受保乳术后的复发风险,同样可行保乳术。
问题:该病者如何行内分泌治疗?
王琳主任:病人为绝经后患者,ER阳性,可予口服 5年的芳香化酶抑制剂,如来曲唑。当然,若经济困难,也可口服他莫昔芬[3]。
问题:如何决定靶向治疗?
(广东省人民医院病理科)刘艳辉主任:应送蜡片做 FISH试验,若阳性,可考虑予赫赛汀治疗。
问题:若病人术后 2年,无病状态,FISH(+),是否用赫赛汀(Herceptin)?若病人术后 4年,无病状态,FISH(+),是否用 Herceptin?
廖宁主任:若病人术后两年,无病状态,FISH(+),用 Herceptin病人仍可获益,可予其一年赫赛汀治疗。若病人术后 4年,尚无依据用 Herceptin是否有效。
旁述:2010年 Her-2阳性乳腺癌临床诊疗专家共识指出,HERA研究显示,延迟 2-3年使用曲妥珠单抗辅助治疗也可以使患者获益[2]。
问题:目前仅做补充锁骨上区?若病人体格较强健,能耐受放疗,该腋窝、锁骨上淋巴结肿大,化疗后明显缩小,病理(-),放疗范围?
(海南省医院)李发奋主任:病人仅做补充锁骨上区放疗,主要是考虑病人的年纪大,耐受力差。从个体化治疗角度出发,缩小放疗的范围。若病人体格较强健,耐受好的话,则考虑予以常规范围的放疗,即范围包括胸壁、腋窝及锁骨上区,量为 50-52 GY,25-26次完成[1]。
[1] 中国抗癌协会乳腺癌专业委员会.2009乳腺癌临床实践指南(中国版)[M].北京:人民卫生出版社,2009∶232-248.
[2] St Gallen.International Expert Consensuson the Primary Therapyof Early Breast Cancer 2009.Annals of Oncology 20∶1319-1329,doi:10.1093/annonc/mdp322,published online,7 June 2009.
[3] Chlebowski RT,Kuller LH,Prentice RL,et al.Breast cancer after use ofestrogen plus progestin in postmenopausal women[J].N Engl J Med,2009,360∶573-587.
[4] Brody LC.Current knowledge on genetic predispositions for breast cancer[J].Breast,2009,18(Suppl 1)∶4-9.
[5] Farmer H,Mc Cabe N,Lord CJ,et al.Targeting the DNA repair defect in BRCA mutant cells as a therapeutic strategy[J].Nature,2005,434∶917-921.
[6] Rottenberg S,Jaspers JE,Kersbergen A,et al.High sensitivity of BRCA1-decient mammary tumors to the PARPinhibitor AZD2281 alone and incombination with platinum drugs[J].Proc Natl Acad Sci U S A,2008,105∶17 079-17 084.
[7] Powles T,Neven P,Osborne C,et al.Five year results of a randomised placebo controlled trial of lasofoxifene(PEARL)on the incidence of ER positive breast cancer in postmenopausal women with osteoporosis[J].Breast,2009,18∶5-12.
[8] Powles T,Neven P,Osborne C,et al.Effects of 5 years of treatment with lasofoxifene on incidence of breast cancer in older women by baseline estradiol levels[J].Breast,2009,18∶26-33.
[9] Krum SA,Miranda-Carboni GA,Lupien M,et al.Unique ERalpha cistromes control cell type-specic gene regulation[J].Mol Endocrinol,2008,22∶2 393-2 406.
[10]Lupien M,Eeckhoute J,Meyer CA,et al.FoxA1translates epigenetic signatures into enhancer-driven lineage-specic transcription[J].Cell,2008,132∶958-970.
[11]林本耀.乳腺癌保乳治疗学[M].北京:清华大学出版社,2004∶198-201.
