水热法合成RMn2O5 (R=Eu,Tb,Dy,Ho)微纳米粉体
2010-02-23黄锡金朱刚强
黄锡金, 冯 波, 朱刚强, 刘 运, 陈 苑
(1.陕西师范大学物理学与信息技术学院, 陕西 西安 710062; 2.陕西科技大学电气与信息工程学院, 陕西 西安 710021)
0 引言
多重铁性原指具有两种或两种以上的铁电、铁磁或铁弹性能,但现在也把反铁电、反铁磁及螺旋铁磁性归入其中.目前研究较多的是具有铁电、(反) 铁磁耦合性能的单相或复合材料,这类材料外加电场可以诱发铁磁性、铁电性,存在乘积关系的磁电效应[1].这种特殊的功能材料在信息存储、微波领域、宽波段磁探测以及多功能电子设备如传感器、感应器、转换器等方面都颇具发展潜力,受到了研究者的广泛关注[2].
RMn2O5(R=稀土)是一类具有复杂分子结构和内部相互机理的多重铁性材料.Alonso等利用X-射线衍射分析发现Mn3+和Mn4+离子占据了晶体中的不同位置,分别为氧八面体中心和四棱锥底中心[3],这类材料的铁电相变温度在25~39 K左右,反铁磁相变温度在39~45 K左右,通常制备这类单相多价态锰氧化合物需要高温、高氧压条件.为了简化制备条件,研究者们又发展了溶胶-凝胶和自蔓延燃烧法等合成方法来制备RMn2O5(R=稀土)粉体[4-6],而这些方法需要较高的后期处理温度,并且容易造成粉体的团聚和在粉体中生成其他的杂相.水热法作为一种重要的化学方法常用于低温合成各种形貌和尺寸的纳米粉体,通过控制反应条件可以调控颗粒的粒度、形貌、相组成等,是一种很有应用前景的粉体制备方法[7].
本文采用水热法在250 ℃反应18 h制备了EuMn2O5、TbMn2O5、DyMn2O5和HoMn2O5微纳米粉体,利用X射线衍射、透射电镜、选区电子衍射和高分辨透射电镜等分析手段表征了RMn2O5(R=Ho,Dy,Tb,Eu)的微纳米结构,研究了反应时间对产物尺寸和晶相结构的影响,并且分析了产物的形成机理.
1 实验
1.1 试剂
硝酸(西安化工厂);KMnO4(分析纯,国药集团化学试剂有限公司);Mn(NO3)2(分析纯,国药集团化学试剂有限公司);NaOH (分析纯,国药集团化学试剂有限公司);R2O3(R=Ho,Dy,Tb,Eu,国药集团化学试剂有限公司,纯度为99.99%);去离子水为实验室自制.
1.2 实验过程
首先,称取一定量的R2O3(R=Eu,Tb,Dy,Ho)溶于2 M的硝酸溶液中形成0.2 M的R(NO3)3(R=Eu,Tb,Dy,Ho)标准溶液.量取12.5 mL R(NO3)3(R=Eu,Tb,Dy,Ho)倒入50 mL烧杯中,然后向溶液中加入计量的高锰酸钾和硝酸锰,搅拌20 min后加入一定量的NaOH,NaOH的浓度为0.3 M,继续搅拌5 min,在所制备的前驱物中加入去离子水至25 mL后将所得的前驱物装入40 mL的反应釜中,最后将反应釜放入恒温箱中在250 ℃反应18 h,反应结束后将粉体用去离子水清洗至中性后在80 ℃烘干.
1.3 样品的表征
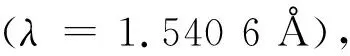
2 结果与讨论
2.1 粉体结构和形貌分析
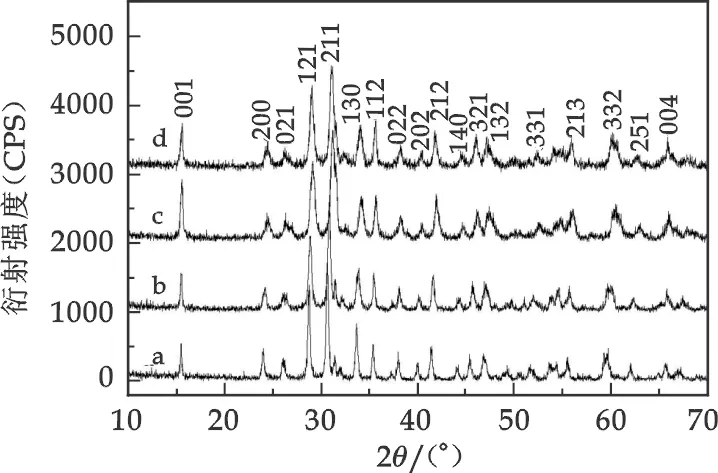
图1 样品的XRD图谱: (a) EuMn2O5; (b) TbMn2O5; (c) DyMn2O5; (c) HoMn2O5

图2 水热法制备粉体的SEM照片:(a)EuMn2O5; (b)TbMn2O5; (c)DyMn2O5; (d)HoMn2O5
将所制得产物进行X 射线衍射分析,结果如图1所示.图1a为在250 ℃反应18 h所制备EuMn2O5粉体的XRD图谱.XRD图谱中所有的衍射峰与正交相EuMn2O5的衍射峰相对应,经计算其晶格常数为a=0.740 5、b=0.856 2和c=0.569 6 nm,与PDF卡号为52-1097正交相EuMn2O5的晶格常数相一致(a=0.739 9、b=0.856 7和c=0.569 3 nm).图1b XRD图谱中所有的衍射峰与正交相TbMn2O5(PDF卡号: 88-0087)的衍射峰相对应,经计算其晶格常数分别为a=0.734 7、b=0.852 5和c=0.568 0 nm.图1c XRD图谱中所有的衍射峰与正交相DyMn2O5(PDF卡号: 72-1696)的衍射峰相对应,经计算其晶格常数为a=0.729 5、b=0.855 6和c=0.568 6 nm.而图1d XRD图谱中所有的衍射峰与正交相HoMn2O5(PDF卡号: 88-0088)的衍射峰相对应,经计算其晶格常数为a=0.731 4、b=0.850 3和c=0.568 1 nm.所有XRD图谱中均没有杂相的衍射峰,这说明碱浓度为0.3 M的水热条件下于250 ℃反应18 h可以分别制备出纯净的正交相RMn2O5(R=Eu,Tb,Dy,Ho)粉体.
2.2 SEM分析
利用SEM观察水热条件下所制备粉体的形貌,结果如图2所示. 图2a为在250 ℃反应18 h所制备EuMn2O5粉体的SEM照片,从图中可以看出所制备的粉体是由尺寸为1~3 μm的颗粒组成.图2b为TbMn2O5粉体的SEM照片,从图中可以看出所制备的粉体是由尺寸不均的颗粒组成,大颗粒直径为20 μm.图2c为DyMn2O5粉体的SEM照片,从图中可以看出所制备的粉体是由尺寸均匀的纳米颗粒组成,颗粒直径为500 nm.而在250 ℃反应18 h所制备HoMn2O5粉体的SEM照片如图2d所示,从图中可以看出粉体是由大量棒状的颗粒组成,其直径为4~10 μm,长为5~30 μm.
2.3 反应时间对HoMn2O5粉体形貌的影响
为了研究不同反应时间对HoMn2O5粉体形貌和尺寸的影响,我们在250 ℃分别反应6 h,10 h和14 h,所制备HoMn2O5粉体的SEM照片如图3所示.从图3a可以看出,反应6 h后所制备的粉体是由大量直径为100~200 nm的纳米颗粒和少量纳米棒组成,图3b是对应的TEM照片,从图中可以清楚地看出粉体是由一些纳米颗粒和纳米棒组成;图3b的插图是纳米颗粒的HRTEM照片,可以测出两个相邻晶面的间距为0.78 nm,对应着正交相HoMn2O5的(001)晶面.当反应时间延长至10 h时所制备的粉体如图3b所示,粉体的颗粒尺寸增大,其直径为500~1 500 nm.当反应间继续延长至14 h时所制备的粉体是由大量尺寸均匀的微米棒组成,长度为5~10 μm.

图3 不同反应时间所制备HoMn2O5粉体的SEM和TEM照片:(a,b)6 h,(c)10 h;(d)14 h
2.4 RMn2O5 (R=Eu,Tb,Dy,Ho)微纳米结构的形成机理
在水热体系中的反应过程是非常复杂的,但是从前面XRD和SEM的测试结果还是可以推断出产物的形成机理.产物中锰的价态是通过KMnO4和Mn(NO3)2的摩尔比来调控的,不同比例的Mn2+/Mn7+可以制备出不同晶体结构的产物.为了制备纯净的RMn2O5(R=Eu,Tb,Dy,Ho)产物,本研究中KMnO4和Mn(NO3)2的摩尔比控制为7∶3,因此可以推断出在此反应体系中形成RMn2O5(R=Ho,Dy,Tb,Eu)的化学反应方程式为:
5R(NO3)3(R=Ho,Dy,Tb,Eu) +3KMnO4+ 7Mn(NO3)2+26NaOH → 5RMn2O5+ 3KNO3+ 26NaNO3+ 7H2O (Mn2+/Mn7+=7∶3)
在水热反应过程中,产物的尺寸和形貌强烈的依赖于晶体成核速率和晶体生长速率二者间的竞争.在反应溶液中,当生长速率大于成核速率时,产物的尺寸较大;成核速率大于生长速率时,产物的尺寸小.而是否能够生长出高各向异性的微、纳米结构还依赖于晶体本身的结构特点和溶液中的化学势能.RMn2O5(R=稀土)是一类具有正交相结构的物质,本身具有高的各向异性,因此当具有合适的外界合成条件时很容易制备出高各向异性的微、纳米结构.从图3可知,反应时间对产物的尺寸有决定性的影响.当反应时间较短时,不定形的前驱物在溶液中溶解后形成过饱和溶液并且通过结晶形成尺寸均匀的纳米颗粒;当延长反应时间时,部分小的纳米颗粒在高温高压下容易溶解,从而大颗粒吸收溶液中的离子长大成更大的晶体,最终大颗粒吸收溶液中的离子由自组装生长而形成高长径比的微纳米结构.
参考文献
[1] Wang J, Neaton J B, Zheng H,etal. Epitaxial BiFeO3multiferroic thin film heterostructures[J]. Science, 2003, 299: 1 719-1 722.
[2] Xia Y N, Yang P D, Sun Y G,etal. One-dimensional nanostructures: synthesis, characterization, and applications[J]. Adv. Mater, 2003, 15: 353-389.
[3] C.R. dela Cruz, B. Lorenz, C.W. Chu. Tuning ferroelectricity in DyMn2O5by pressure and magnetic fields[J]. Physica B: Condensed Matter, 2008, 403: 1 331-1 335.
[4] Yu C C, Huang S Y, Yeh C J,etal. The dynamic magnetic transitions in LaxHo1-xMn2O5(x=0~0.2) compounds[J]. J. Appl. Phys., 2008, 103: 07E311-07E313.
[5] Chen Y, Yuan H M, Tian G,etal. Hydrothermal synthesis and magnetic properties of RMn2O5(R=La,Pr,Nd,Tb,Bi) and LaMn2O5+δ[J]. J. Solid State Chem., 2007, 180(4): 1 340-1 346.
[6] Li N, Xu X, Luo D,etal. Electrocatalytic activities of REMn2O5(RE=Dy,Ho,Er,Tm,Yb,and Lu) and Er0.76Zr0.11Ca0.13Mn2O5for oxygen reduction in alkaline solution[J]. J. Power. Sources, 2004, 126: 229-235.
[7] Chen C, Cheng J R, Yu S W,etal. Hydrothermal synthesis of perovskite bismuth ferrite crystallites[J]. J. Cryst. Growth, 2006, 291(1): 135-139.
