全固态Ag/AgCl参比电极的制备及性能测试
2010-02-23杨百勤
杨百勤, 左 芳
(陕西科技大学化学与化工学院, 陕西 西安 710021)
0 引言
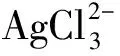
我们在前人研究的基础上制备了一种内阻低,能够耐一定的温度和压力的全固态Ag/AgCl参比电极.
1 实验部分
1.1 仪器和试剂
217C型饱和甘汞电极(江苏江分电分析仪器有限公司);pHS-3C型酸度计(上海雷磁仪器厂);213型铂电极(江苏江分电分析仪器有限公司);CHI660B电化学工作站(上海辰华仪器公司);85-2A型恒温磁力加热搅拌器(金坛市丹阳门石英玻璃厂).
Ф0.5 mm银丝(Ag)纯度>99.8%(上海试剂厂,99.8%以上);丙烯酰胺(C3H5NO)(西安市化学试剂厂);氯化钾(KCl)(天津市福晨化学试剂厂);氯化银(AgCl)(天津市化学试剂二厂);琼脂粉(北京奥博星生物技术责任有限公司);pW缓冲溶液:磷酸、硼酸、苯乙酸按一定比例混合配制;pH5.00、6.86的标准缓冲溶液:由上海雷磁-创益仪器仪表有限公司所售标准pH缓冲剂配制;实验所用试剂均为优级纯;所用水均为二次蒸馏水.
1.2 Ag/AgCl电极的制备
将Φ0.5 mm银丝用金相砂纸打磨,以除去表面的氧化层,然后分别用滤纸和擦镜纸抛光.称取一定量水溶性高分子化合物加入到饱和KCl溶液中,再加入丙烯酰胺以及催化剂,搅拌均匀,加热,沸腾后,趁热将糊状物装入洁净玻璃管中,插入银丝,用胶密封制得裸露式的Ag/AgCl参比电极[3].
2 结果与讨论
2.1 电极的稳定性及重现性
将自制裸露式Ag/AgCl参比电极与饱和甘汞电极插入0.1 mol/L KCl、1 mol/L KCl、饱和KCl、pH5.00、pH6.86的标准缓冲溶液中,连续24 h观察电位随时间的变化关系.
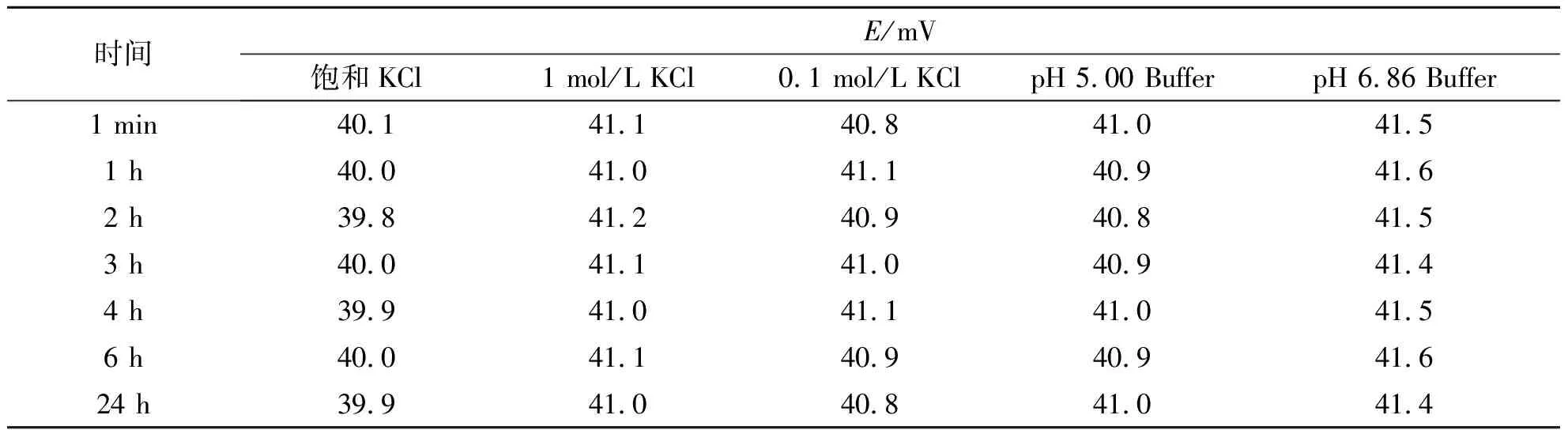
表1 不同介质中Ag/AgCl参比电极的电位值
表1结果表明,自制的Ag/AgCl电极在各种介质中电位稳定,漂移小,说明该电极稳定性及重现性好,能满足pH和电位测量的要求.
2.2 电极的响应时间
温度25 ℃时,将裸露式Ag/AgCl电极和甘汞电极分别放入pW缓冲液、pH5.00及pH6.86的标准缓冲液中,响应时间均小于30 s,可见电极具有较快的响应速度.
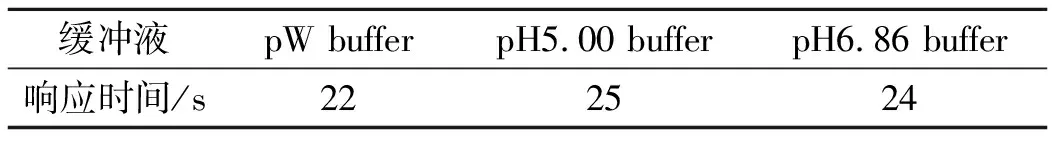
表2 不同缓冲液中Ag/AgCl参比电极的响应时间
2.3 温度对电极的影响
将传感器置于pH=5.00的缓冲溶液中,在水浴中加热,测定温度由20~80 ℃间升温变化,观察其电位E随温度的变化情况.实验结果表明,温度在20~60 ℃时电位值基本不变;温度在65~80 ℃时,温度每上升1 ℃电位值升高≤1 mV(0.01 pH/℃,在误差允许的范围内),说明全固态Ag/AgCl电极在温度20~60 ℃范围内具有较好的稳定性.

表3 不同温度时Ag/AgCl参比电极的电位值
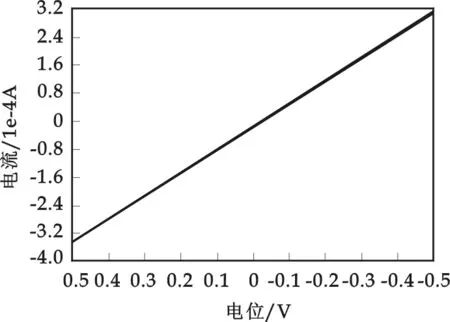
图1 Ag/AgCl电极可逆性曲线
2.4 电极的可逆性
对自制Ag/AgCl参比电极进行小幅度循环伏安极化扫描,在-500~+500 mV的电位范围内正向和反向极化曲线几乎完全重合而且呈良好的线性关系,如图1所示,可见自制的Ag/AgCl参比电极具有良好的可逆性.
2.5 电极寿命
电极在正常使用的情况下,室温下避光保存,寿命至少半年以上.如在0.1 mol/L KCl溶液中保存,寿命可延长至两年以上.
2.6 样品测定
用玻璃电极与自制Ag/AgCl参比电极组成测量电池来测量实际样品的pH值,并配以玻璃pH复合电极组成另一测量电池验证其准确性[4].测试结果如表4所示.
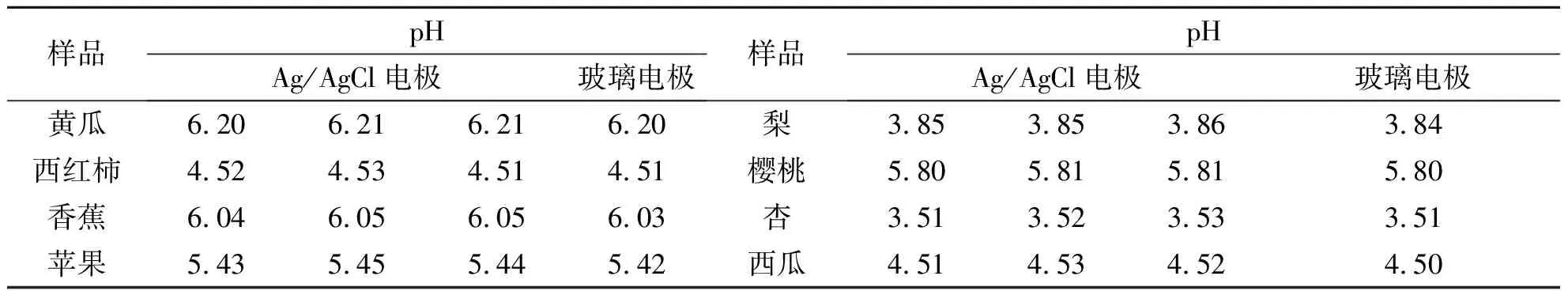
表4 样品测试结果
由表4可知,对样品的pH值测定,pH值之差均小于0.05,在误差允许范围之内,说明自制的全固态Ag/AgCl参比电极具有良好的稳定性、重现性和可逆性.
3 结束语
全固态Ag/AgCl参比电极是对现有的电解型Ag/AgCl参比电极和饱和甘汞参比电极的一大改进.该电极制备工艺简单,不需电镀等繁杂工序,同时可减少汞对环境造成的二次污染,具有良好的稳定性、重现性和可逆性,完全可替代饱和甘汞电极用于电位分析.
[1] 张 清,李 萍,白真权.Ag/AgCl高温参比电极的制备[J].应用科技,2005,32(6): 62.
[2] 谢声洛.离子选择电极分析技术[M].北京:化学工业出版社,1985:122-129.
[3] 黄超伦,任聚杰,徐达峰.新型固体参比电极的研制[J].分析化学,1996,24(7):816-819.
[4] 李向阳,杜宝中,周长强.全固态SiC参比电极的研制及应用[J].化学传感器,2006,26(3):41.
