乙胺嘧啶分子印迹聚合物的制备及其性能研究*
2010-02-08刘发强迟大民苏立强
刘发强,迟大民,苏立强,王 颖
(齐齐哈尔大学 化学与化学工程学院,黑龙江 齐齐哈尔 161006)
分子印迹技术是近年来集高分子合成、分子设计、分子识别、仿生生物工程等众多学科优势发展起来的一门边缘学科分支。分子印迹聚合物由于具有与天然抗体相似的识别选择性和高分子材料的抗腐蚀性能的双重优点,因而正逐步应用于分析化学、生物工程、临床医学、环境监测、食品工业等众多领域。在固相提取、药物的手性分离[1]、传感器等方面展现了广泛的应用前景。
乙胺嘧啶[2]是一种广谱抗菌兽药,主要用于防治鸡球虫病、禽霍乱及仔猪白痢等。乙胺嘧啶在水产养殖业上也有着广泛的应用,适量使用能增强水产动物的抗病能力,但是乙胺嘧啶在水产品体内具有高度的蓄积性,超出一定范围,人食用后破坏人的造血系统,造成溶血性贫血症,甚至有引起潜在致癌性的可能,同时对中枢神经系统有直接的毒性作用。敌菌净属于二氨基嘧啶类药物,是一种抗菌增效剂,主要与乙胺嘧啶和磺胺类药物等抗生素组成复方制剂,抗菌活性增强,在兽医临床上应用十分广泛。因此,在动物产品和水产品体内会同时残留乙胺嘧啶和敌菌净[3],针对乙胺嘧啶有致癌的可能性和对神经中枢的毒害作用将乙胺嘧啶与敌菌净进行分离是十分重要的[4]。
本文采用分子印迹技术,以乙胺嘧啶为模板分子,甲基丙烯酸(MAA)为功能单体,乙二醇二甲基丙烯酸酯(EDMA)为交联剂,偶氮二异丁腈(AIBN)为引发剂,在苯甲醇和乙腈的混合溶液中制备了乙胺嘧啶分子印迹聚合物。把制得的乙胺嘧啶分子印迹聚合物用于液相色谱固定相,在甲醇水为流动相中可将其与结构类似物敌菌净基线分离,吸附实验中印迹聚合物对乙胺嘧啶有特异的吸附性。
1 实验部分
1.1 仪器与试剂
高效液相色谱仪(UV230+紫外可变波长检测器,P230高压恒流泵);Echrom2000色谱工作站(大连依利特分析仪器有限公司);TU-1901型双波长紫外可见分光光度计(北京普析通用仪器有限公司);DK-98-1型电热恒温水浴锅(北京泰克仪器有限公司)。
乙胺嘧啶和敌菌净(纯度>98%,武汉远城科技发展有限公司);乙二醇二甲基丙烯酸酯(A.R.东京化成工业株式会社);偶氮二异丁睛(A.R.北京化工厂);甲基丙烯酸(A.R.北京化工厂)。
1.2 聚合物的制备
称取模板分子乙胺嘧啶0.2487g(1mmol),将其溶于10mL苯甲醇和5mL乙腈混合溶液中,再加入功能单体甲基丙烯酸0.35g(4mmol),加入交联剂EDMA 4.0g(20mmol),引发剂 AIBN 0.05g,超声震荡后将其转入安培管中,反复抽真空脱氧,充N23~5次,最后在N2保护下抽真空封管。采用热引发方式聚合,将安培管放入60℃恒温水浴中,反应48h后取出,将得到的聚合物经过粗研,用索式提取器提取24h,提取液为苯甲醇/乙酸体积比为9∶1,以除去模板分子。将洗脱完的聚合物过300目分样筛,用丙酮反复沉降,移出清液,把剩余固体放在通风橱内自然晾干,以备使用。
制备非印迹聚合物NMIP时,除不加模板分子和无需进行索氏提取以外,其它步骤同上。
1.3 色谱条件
色谱柱:20 cm×4.6 mm i d;检测波长为235 nm;流速为1.0 mL·min-1;流动相为甲醇:水(0.6%冰乙酸)=25:75;进样量 10μL。
2 结果与讨论
2.1 标准曲线的绘制
准确配制一系列浓度为 0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9 mg·mL-1的乙胺嘧啶甲醇溶液,用高效液相色谱进行检测。绘制乙胺嘧啶浓度与色谱峰面积值的工作曲线如图1,回归方程式为y=363.69x+33.702,线性相关系数0.9996。由图1可见,乙胺嘧啶浓度在0.1~0.9 mg·mL-1范围内,两者之间有良好的线性关系。
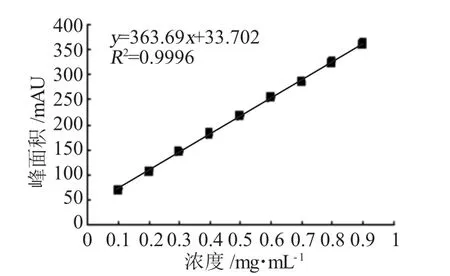
图1 乙胺嘧啶标准曲线Fig.1 Standard curve of pyrimethamine
2.2 MIP对乙胺嘧啶的吸附作用及选择性研究
采用静态吸附法考察所制备的MIPs吸附性能。配制一系列浓度为 0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9 mg·mL-1的乙胺嘧啶甲醇溶液各 10 mL,分别投入50mg乙胺嘧啶分子印迹聚合物,静置过夜。用高效液相色谱测量其峰面积A,依据工作曲线计算出不同峰面积所对应底物的平衡浓度。
根据结合前后溶液中底物浓度的变化,由方程Q=(Co-Ce)V/W计算出聚合物对底物的吸附量Q(mg·g-1),绘出吸附量Q与不同浓度关系的动力学曲线。其中:Co:乙胺嘧啶溶液的初始浓度;Ce:吸附后的浓度;V:加入乙胺嘧啶溶液的体积;W:称取的分子印迹聚合物的质量。
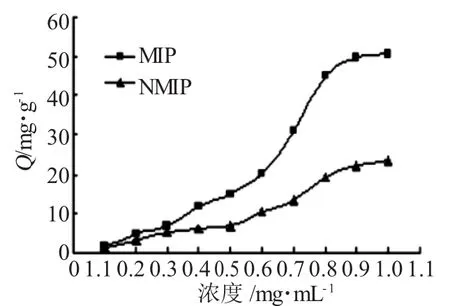
图2 MIP和NMIP的吸附量Fig.2 Adsorbance of MIP and NMIP
由图2可以看出,印迹聚合物对乙胺嘧啶具有特异性吸附。对比二种聚合物的合成过程,可以得出印迹聚合物对乙胺嘧啶具有特异性吸附的原因是,在合成过程中由于乙胺嘧啶的加入而形成了复合物,当洗涤出模板物质后在聚合物内部形成了形状与官能团位置均与乙胺嘧啶相配合的空腔,正是由于这些空腔的存在,使印迹聚合物对模板物质具有良好的选择性结合能力。虽然NMIP和乙胺嘧啶也形成氢键,但由于位置关系,不具有作用位点的匹配,阻碍同其它分子的作用,因此,对乙胺嘧啶的吸附很小,而MIP对乙胺嘧啶确有特异的吸附性。
2.3 流动相的选择
分离实验流动相采用甲醇水体系,经过实验验证,改变流动相中水的含量,将引起分离度的变化,采用甲醇/水为25∶75,达到基线分离。这是因为当流动相中有机相含量占主要的时候,氢键占主要地位,水的加入导致了聚合物与模板氢键强度的减弱,随着有机相中水含量的增加,氢键越来越弱,模板与聚合物的离子键和疏水作用此时却变得越来越强,分子识别逐步由氢键识别机理转化为离子交换机理和疏水作用所控制。在实验的过程中常出现基线漂移现象,在流动相中加入0.6%的冰乙酸能够很好的解决这个问题。本文在进行实验的过程中加入冰乙酸的含量为0.05%~0.80%,含量较低时仍出现基线漂移现象,含量较高时基线漂移现象消失但是分离度下降,这是因为冰乙酸含量过高破坏分子间氢键,分子识别作用变弱。实验证明冰乙酸的含量为0.6%时,能更好的防止基线漂移和杂质离子干扰。
综上所述,乙胺嘧啶和敌菌净的分离实验流动相采用甲醇/水/冰乙酸为25∶75∶0.6%。
2.4 聚合物对模板分子及结构类似物的色谱分离
以聚合物作为色谱固定相,制成色谱柱。利用高效液相色谱法对乙胺嘧啶和结构类似物敌菌净(结构见图3)混合溶液进行检测,见图4、5。

图3 乙胺嘧啶与敌菌净的结构式Fig.3 Molecular graph of pyrimethamine and diaveridine.
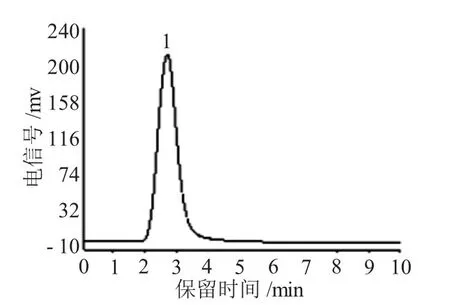
图4 空白聚合物色谱评价图Fig.4 Chromatographic evaluation chart of NMIP
从图4中可以看出,在非印迹柱上,两种物质均无保留,并且色谱峰完全重叠。

图5 印迹聚合物色谱评价图Fig.5 Chromatographic evaluation chart of MIP
从图5中可以看出,在印迹柱上,二者出峰时间均加长了,并且乙胺嘧啶的出峰时间比敌菌净的出峰时间长,乙胺嘧啶的峰有拖尾,这正是烙印型色谱固定相分离的典型特征。二者达到了基线分离,说明所制备的乙胺嘧啶印迹聚合物能够产生很好的孔穴,并且这种孔穴与模板分子的专一匹配程度很好,因此,它能够达到对于乙胺嘧啶与其结构相似物(敌菌净)的分离。
3 结论
以乙胺嘧啶为模板分子,在苯甲醇和乙腈混合溶液中制备了乙胺嘧啶分子印迹聚合物,可以识别模板分子及其类似物,对乙胺嘧啶呈现了很高的选择性。以甲醇水为流动相,色谱分离乙胺嘧啶和敌菌净达到基线分离。绘制不同浓度的吸附量曲线,结果表明印迹聚合物远大于非印迹聚合物的吸附量,说明印迹聚合物对乙胺嘧啶有特异的吸附性。
[1]郭天瑛,张丽影,郝广杰.氨基酸衍生物手性分离分子印迹聚合物[J].化学进展,2004,16(4):638-642.
[2]钱桂平,余建中.高效液相色谱法测定鱼肉中的乙胺嘧啶[J].中国卫生检验杂志,2005,15(6):697-698.
[3]林海丹,林峰.高效液相色谱法测定动物源性食品中甲氧苄胺嘧啶药物残留[J].检验检疫学,2003,13(5):5-6.
[4]吴小平,邹世平,李晓莉,等.鳗鲡血浆与肌肉中乙胺嘧啶检测方法的建立[J].淡水渔业,2007,37(4):65-68.
