电化学调价制备2AFⅡ. Pu(Ⅲ)的电化学氧化研究
2010-01-26叶国安李会蓉
张 虎,叶国安,李 丽,杨 贺,李会蓉
中国原子能科学研究院 放射化学研究所,北京 102413
电化学氧化制备2AF料液时,首先要将还原性物质甲基肼(MMH)和二甲基羟胺(DMHAN)破坏完全,然后开始Pu(Ⅲ)的电解氧化。在电解氧化过程中,阳极首先发生的是甲基肼的电解氧化反应,甲基肼被完全破坏后,二甲基羟胺在阴极发生间接的氧化反应[1],由于反应产生的亚硝酸可以快速氧化Pu(Ⅲ)到Pu(Ⅳ),因此可以利用生成的亚硝酸进行钚的调价。本工作拟研究钚的电解氧化调价,以阐明电解调价过程的反应机理。
1 实验部分
1.1 仪器及装置
LS-6000LL型液体闪烁谱仪,美国Bechman公司;LPS202双路稳压稳流电源,北京TRADEX公司;钛基镀铂网电极为阳极、钛网电极为阴极,阴极和阳极电极几何面积均为8 cm2,阴、阳极之间无隔膜,两极间距为1 cm。
1.2 试剂
二甲基羟胺系实验室合成,气相色谱分析纯度大于95%;甲基肼为航天部一院101所产品,纯度大于99%;1-苯基-3-甲基-4-苯甲酰基吡唑啉酮-5(PMBP)为分析纯,美国百灵威公司产品;二甲苯、HNO3等其它试剂为北京化学试剂公司产品,分析纯。钚储备液:硝酸钚溶液经过氨基磺酸亚铁还原,亚硝酸氧化,2606阴离子交换树脂纯化,得到Pu(Ⅳ)储备液。
1.3 实验方法
电解实验装置参照文献[1],分别取一定体积的甲基肼、二甲基羟胺和钚的储备液于电解池中,接通电源,调节电流(电压)到设定值后开始电解,同时记录电解时间及阴极和阳极的电极电位(相对于饱和甘汞电极)和槽电压。电解过程不加搅拌,实验过程中取电解池中部样品。采用PMBP/二甲苯萃取法分析钚价态随电解时间的变化。
1.4 分析方法[2]
钚的价态分析采用0.05 mol/L PMBP/二甲苯萃取,α液闪计数法测量不同价态钚的含量:取20 μL含钚电解液,加入0.98 mL含尿素的HNO3溶液中,使水相中HNO3初始浓度为1.50 mol/L,尿素初始浓度为0.05 mol/L;向水相中加入等体积的0.05 mol/L PMBP/二甲苯,振荡3 min离心分相,有机相取100 μL测量Pu(Ⅳ)的α计数,水相取出0.5 mL,加入0.4 mol/L NaNO20.25 mL,1.5 mol/L HNO30.25 mL,放置10 min,再加入1.0 mL 0.05 mol/L PMBP/二甲苯,振荡3 min离心分相,水相取100 μL测量Pu(Ⅵ)的α计数,有机相取100 μL测量Pu(Ⅲ)的α计数。
2 结果与讨论
2.1 HNO3初始浓度对钚调价的影响
恒电流电解,电流密度J=22.5 mA/cm2(槽压2.6~3.1 V),考察不同HNO3初始浓度下不同价态钚的相对百分含量随电解时间的变化,结果示于图1。从图1可以看出,在电解开始阶段,由于溶液中存在二甲基羟胺和甲基肼,抑制了Pu(Ⅲ)的阳极氧化,Pu(Ⅳ)的含量呈缓慢增加。当还原剂被电解破坏后,Pu(Ⅲ)被迅速氧化为Pu(Ⅳ),钚价态的变化呈现明显的突跃。电解过程中Pu(Ⅵ)的含量无明显变化,表明由于四价钚氧化到六价的超电位较高,在实验条件下难以发生Pu(Ⅳ)氧化到Pu(Ⅵ)的电极反应。

图1 不同HNO3初始浓度下Pu(Ⅳ)的质量分数与电解时间的关系Fig.1 Mass percentage of Pu(Ⅳ) vs electrolysis time at different initial concentration of HNO3c0(MMH)=0.15 mol/L,c0(DMHAN)=0.10 mol/L,ρ0(Pu)=0.43 g/L,J=22.5 mA/cm2,电解液体积(Electrolyte volume)10.0 mLc0(HNO3),mol/L:■——1.5,●——2.0,▲——3.0,△——3.5
HNO3初始浓度对钚的调价具有十分重要的作用。实验表明,HNO3初始浓度增加可以缩短Pu(Ⅲ)氧化为Pu(Ⅳ)的时间,在c0(HNO3)=1.5 mol/L时,完成钚的调价需要110 min,而c0(HNO3)=3.0 mol/L时,仅需70 min就可以完成钚的调价。这是由于HNO3初始浓度的增加,加快了对二甲基羟胺和甲基肼的破坏,从而缩短了Pu(Ⅲ)氧化的时间。
2.2 电流密度对钚调价的影响
在电解过程中,电流密度反映了电解速率。电流密度过低则电解过程缓慢,而电流密度过高会造成电极上的极化电位升高,副反应增多,电流效率降低。为了使电解调价既能达到一定的速率,缩短电解的时间,又具有较高的电流效率,必须维持适当的电流密度[3]。
配制10.0 mL模拟1BP溶液,在不同电流密度下恒电流电解,考察Pu(Ⅳ)质量分数的变化,结果示于图2。由图2可知,电流密度对钚调价的时间有明显影响。电流密度为11.0 mA/cm2时,完成钚的电解调价需要130 min,电流密度为22.5 mA/cm2时,完成钚的调价需要60 min,电流密度增大有利于加快钚的电解调价。但是当电流密度达到45.0 mA/cm2时,此时槽电压达到4.3 V,较高的超电位对钚价态的影响明显增强,Pu(Ⅳ)的质量分数最高仅约为40%,其余主要为Pu(Ⅲ),而电解液中Pu(Ⅵ)的质量分数始终保持在1%左右。

图2 不同电流密度下Pu(Ⅳ)的质量分数与电解时间的关系Fig.2 Mass percentages of Pu(Ⅳ) vs electrolysis time at different current densityc0(MMH)=0.15 mol/L,c0(DMHAN)=0.10 mol/L,c0(HNO3)=2.5 mol/LJ,mA/cm2:■——11.0,●——22.5,▲——34.0,△——45.0
实验表明,在1BP料液电解调价时,电流密度应控制为10~30 mA/cm2较为适宜,这样既能保持较快的电解速率,又可以实现钚的完全调价,此时槽电压维持为2.6~3.1 V。
2.3 还原剂对钚调价的影响
二甲基羟胺、甲基肼都是还原性较强的有机试剂。实验考察还原剂对钚调价的影响,并对电解调价的机理作进一步的研究。电解实验参数为:180 mA恒电流电解(槽电压2.6 V),电解液中HNO3初始浓度为3.0 mol/L,Pu(Ⅲ)初始质量浓度为0.43 g/L。图3为电解液中不含甲基肼时、二甲基羟胺HNO3溶液中钚价态与电解时间的关系。图3表明,二甲基羟胺在钚电解调价中具有重要作用,在仅有二甲基羟胺存在的HNO3体系中可以迅速将三价钚氧化到四价。

图3 二甲基羟胺HNO3溶液中钚价态与电解时间的关系Fig.3 Plots of valence states of plutonium vs electrolysis timec0(DMHAN)=0.10 mol/L,c0(HNO3)=3.0 mol/L,J=22.5 mA/cm2,ρ0(Pu(Ⅲ))=0.43 g/L

图4 不同浓度电解液中Pu(Ⅳ)质量分数与电解时间的关系Fig.4 Mass percentage of Pu(Ⅳ) vs electrolysis time at different concentration ratio of c0(MMH)/c0(DMHAN)c0(MMH)=0.15 mol/L,c0(HNO3)=3.0 mol/L,J=22.5 mA/cm2,ρ0(Pu(Ⅲ))=0.43 g/Lc0(MMH)/c0(DMHAN):■——15/1,●——15/2,△——15/3
图4为甲基肼初始浓度为0.15 mol/L时,不同摩尔浓度比(c0(MMH)/c0(DMHAN))的电解液在电解时钚价态的变化。实验表明,HNO3溶液中存在少量二甲基羟胺就可以完成钚的完全电解调价。即使二甲基羟胺初始浓度为0.010 mol/L,也可以使大于99%的Pu(Ⅲ)电解氧化到Pu(Ⅳ)。但是当二甲基羟胺初始浓度较低时,当Pu(Ⅳ)浓度达到最高后,在较短的时间内(10 min),会有少量的Pu(Ⅳ)在阴极被还原为Pu(Ⅲ),使得Pu(Ⅳ)的含量有所降低,Pu(Ⅳ)的质量分数降至98.6%。而当二甲基羟胺初始浓度为0.10 mol/L时,在Pu(Ⅳ)浓度达到最高后的30 min内,Pu(Ⅳ)的质量分数始终保持在99.4%以上。因此电解调价时保持一定初始浓度的二甲基羟胺有利于钚的调价。
2.4 阳、阴极电极面积比对钚电解调价的影响
由于电极反应是发生在电极和溶液之间的两相化学反应,两相界面对电化学反应有着重要影响,阳极和阴极电极面积大小及比例是电解设备设计的重要参数,为此考察了阳极、阴极电极面积比对电解过程中钚价态的影响[4]。
实验中固定阳极(钛基镀铂网电极)几何面积(San)为8.0 cm2,改变钛阴极的面积(Scath)。电解液体积为10.0 mL,实验结果示于图5。由图5可以看出,阳极、阴极面积比对钚价态有明显影响,阴极面积减少不利于钚的电解调价。当阴极面积为阳极面积的1/10时,电解过程中Pu(Ⅳ)的含量只是缓慢增加,电解200 min后Pu(Ⅲ)的氧化率仅约为50%;当阳极、阴极面积比为1/1时,在50 min后Pu(Ⅲ)可以被完全氧化到四价,说明钚的电解氧化与阴极的电化学反应密切相关。之前的研究[1]表明,二甲基羟胺在阴极发生间接的氧化反应,生成的亚硝酸可以将Pu(Ⅲ)氧化为Pu(Ⅳ)。当阴极面积减少时,阴极上发生的HNO3电解还原速率降低,生成亚硝酸的量减少,导致了钚电解氧化的速率降低。实验表明阳、阴极面积比为1/1较为合适。
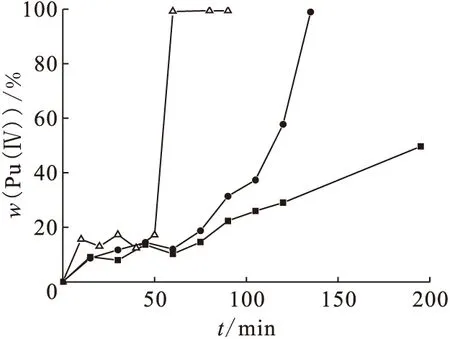
图5 不同电极面积比时Pu(Ⅳ)质量分数与电解时间的关系Fig.5 Mass percentage of Pu(Ⅳ) vs electrolysis time at different area ratio of anode/cathodec0(MMH)=0.15 mol/L,c0(HNO3)=3.0 mol/L,J=22.5 mA/cm2,ρ0(Pu(Ⅲ))=0.43 g/L,San=8.0 cm2San/Scath:■——1/0.1,●——1/0.25,△——1/1
2.5 按照实际1BP浓度进行钚的调价实验
在实际1BP料液中钚的质量浓度约为3.0 g/L。按照1BP的钚浓度进行电解调价实验(图6),大约100 min可以完成钚的电解调价,w(Pu(Ⅳ))>99.7%,w(Pu(Ⅲ))<0.01%,w(Pu(Ⅵ))<0.3%。表明在实验条件下能够实现钚的电解调价。

图6 实际1BP料液中Pu质量分数与电解时间的关系Fig.6 Plots of valence states of plutonium of 1BP vs electrolysis time c0(MMH)=0.15 mol/L,c0(DMHAN)=0.094 mol/L,c0(HNO3)=3.0 mol/L,ρ0(Pu(Ⅲ))=3.0 g/L,J=22.5 mA/cm2
2.6 反应机理[1]
首先在阳极上主要发生甲基肼的电解氧化,少量的Pu3+和二甲基羟胺在阳极被缓慢氧化。在阴极主要发生HNO3的还原、部分在阳极被氧化到四价的钚在阴极又被还原到三价、氢离子的电解还原等反应。当甲基肼电解完全后,HNO3在阴极被电解还原生成HNO2,同时,二甲基羟胺与HNO3反应生成HNO2,HNO2又可以自催化与二甲基羟胺的反应,此时二甲基羟胺被快速消耗。随着阴极区生成的HNO2不断增加,溶液中的HNO2迅速地将Pu3+氧化到Pu4+。
3 结 论
在以钛基镀铂电极为阳极、钛电极为阴极的无隔膜电解体系中,可以实现1BP料液的电解调价。调价后Pu(Ⅳ)的质量分数大于99.7%,Pu(Ⅵ)的质量分数小于0.3%;甲基肼、二甲基羟胺可被完全电解破坏;电解调价过程中无需加入其他试剂。适宜的电解调价参数为:阳极与阴极面积比为1/1;电流密度10~30 mA/cm2,槽电压2.6~3.1 V。
[1] 张 虎,叶国安,李 丽,等.电化学调价制备2AF Ⅰ.二甲基羟胺和甲基肼的电解氧化研究[J].核化学与放射化学,2010,32(2):76-83.
[2] 隗秀芳,张清轩.PMBP萃取法分析HNO3介质中钚的价态[J].原子能科学技术,1991,25(3):62-67.
[3] Pickett D J. Electrochemical Reactor Design[M]. 2rd ed. New York: Elsevier Scientific Publishing Company, 1979: 63-69.
[4] Bard A J, Faulkner L R. 电化学方法——原理和应用[M].第二版.邵元华等,译.北京:化学工业出版社,2005:17-18.
