镍钛记忆合金支架治疗兔外耳道狭窄的实验研究
2010-01-25王孟冬黄志纯顾建兴孙宝宾冯旭
王孟冬 黄志纯 顾建兴 孙宝宾 冯旭
外耳道闭锁(包括伴随的中耳及耳廓畸形)是临床上导致传导性听力障碍的常见原因之一。虽然国内外耳科学者采用了外耳道薄层皮瓣或中厚皮瓣植皮、明胶海绵或碘仿纱条填塞及硅胶管扩张、瘢痕形成后局部类固醇激素注射等方法,都不能完全阻止新造外耳道的再狭窄。其重要原因之一是传统扩张材料如硅胶管等压力不均匀、不易固定、易继发感染等最终导致治疗失败。镍钛记忆合金支架具有优良的生物相容性,耐腐蚀,长期使用无毒副作用,具有超弹性,可通过植入装置植入比本身更狭窄的管腔,不仅可以产生更大的压力,同时也有良好的固定效果[1,2]。因此,镍钛记忆合金支架在临床上已逐步取代了不锈钢及其他成分的扩张材料,成为治疗人体各种腔道狭窄的首选材料。为了探讨使用镍钛记忆合金支架治疗外耳道狭窄的可行性,本研究分别应用镍钛记忆合金支架和硅胶管治疗兔外耳道瘢痕狭窄,并比较其疗效,现报告如下。
1 材料与方法
1.1实验动物的选择和分组 16只外耳道瘢痕狭窄的新西兰大白兔动物模型[3],两组兔外耳道瘢痕狭窄的直径差异无统计学意义。年龄2~3岁,性别不限,随机分为植皮组与不植皮组,每组各8只16耳,采用自身对照的方法进行研究,各组在兔的双侧外耳道分别植入镍钛记忆合金支架和硅胶管。
1.2置入材料 硅胶管的选择:普通白色硅胶管,外径6 mm,内径4 mm,购自南京晚晴公司,每节硅胶管长度为20 mm。镍钛记忆合金支架植入器的研制:支架材料由本研究小组与南京微创医学科技有限公司共同合作,采用通过国家鉴定并在临床使用的镍钛记忆合金初步研制出适合外耳道狭窄使用的镍钛记忆合金支架(以下简称“支架”),长20 mm,外径6 mm,外覆硅胶膜,上有12个直径1 mm的微孔,便于外耳道分泌物的排出。
1.3置入方法 不植皮组:动物0.6%戊巴比妥那(4 ml/kg)全身麻醉后将支架压入置入器外管,插入内芯送至置入器最前端,按刻度指示送至距外耳道口2 cm处,固定置入器内芯并撤出外管,支架自然膨胀固定。将硅胶管置入同一兔的另一侧外耳道后固定,肌肉注射青霉素40万单位/次,2次/日,预防感染。植皮组:同法麻醉动物后,切除少量外耳道瘢痕组织,暴露新鲜创面,于兔耳廓腹侧避开较大血管,切取长条形皮肤长约2 cm,宽约1 cm,深达软骨面,热烧灼止血,外涂0.5%金霉素眼膏。将所取皮肤按不同个体卷成不同直径的皮瓣,前后对称各选2点缝合后再缝合于兔耳根部皮肤上。同法固定支架及硅胶管,并肌肉注射青霉素预防感染。
1.4观察指标与方法
1.4.1大体观察外耳道直径 植皮组在支架置入后第5、15、30、60天时,临时取出扩张管,用耳内窥镜观察实验动物外耳道分泌物及鼓膜情况,游标卡尺分别测量双侧外耳道直径大小。
1.4.2HE染色观察成纤维细胞 不植皮组在支架和硅胶管置入后第5、15、30、60天时,临时取出双侧外耳道的扩张管,分别取双侧外耳道瘢痕组织行HE染色,观察瘢痕中成纤维细胞增生情况。在400倍的视野下,观察6个视野的成纤维细胞的数量,取平均值。
1.4.3RT-PCR检测TGFβ1表达 不植皮组在支架和硅胶管置入后第5、15、30、60天分别取双侧外耳道瘢痕组织,提取RNA,与β肌动蛋白(βactin)一起行RT-PCR,使用ImageMasterVDS图像分析仪进行扫描摄像保存,用Total lab软件分析图谱并将TGFβ1/βactin比值作为半定量数值观察瘢痕中TGFβ1的表达情况。
1.5统计学方法 采用SPSS12统计软件,组内比较采用配对t检验。
2 结果
2.1大体观察外耳道直径 2月后植皮组取出扩张材料,镍钛记忆合金支架侧外耳道植皮表面除有浅表的网状压痕外皮肤表面光滑;硅胶管侧外耳道植皮部分皮肤有皱缩;两侧植入后各时间点外耳道的直径均增大,镍钛记忆合金支架侧外耳道直径较硅胶管侧增大明显,差异有统计学意义(表1)。随着时间的延长,两侧外耳道直径增大越明显,除30天外,各时间点差异均有统计学意义(P<0.05)。
2.2HE染色 不植皮组镍钛记忆合金支架侧和硅胶管侧置入后各时间点外耳道瘢痕组织中成纤维细胞数均逐渐下降,除30天外,各时间点差异均有统计学意义(P<0.05)。在同一时间点,镍钛记忆合金支架侧外耳道瘢痕中成纤维细胞数量较硅胶管侧明显减少,差异有统计学意义(P<0.05)(表2)。
2.3RT-PCR检测 不植皮组镍钛记忆合金支架和硅胶管置入后各时间点所取瘢痕组织中的TGFβ1mRNA/β-actin比值均下降,除术后30天外,各时间点差异均有统计学意义(P<0.05);同一时间点镍钛记忆合金支架侧瘢痕中TGFβ1mRNA/β-actin比值较硅胶管侧明显降低,差异有统统计学意义(P<0.05)(表2)。
3 讨论
人外耳道闭锁术后再狭窄主要是由于创伤修复过程中瘢痕组织中成纤维细胞增生活跃,细胞外基质过度沉积所致[4]。TGFβ1是一种多功能细胞因子,在细胞外基质合成和重塑方面起到关键的作用,同时参与了成纤维细胞的凋亡过程,是组织损伤的上调基因,其作用贯穿于创伤愈合过程的始终[5]。因此,本实验选用TGFβ1作为瘢痕增生的检测指标,由于RT-PCR检测TGFβ1为半定量方法,故采用同时测量内参β-actin并计算比值的方法确定TGFβ1相对值以便于比较。
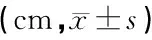
表1 植皮组镍钛记忆合金支架侧与硅胶管侧术后不同时间兔外耳道直径变化比较(n=8耳)
注:*与硅胶管侧同一时间点比较,P<0.05
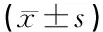
表2 不植皮组镍钛记忆合金支架侧与硅胶管侧各时间点瘢痕组织中成纤维细胞的数量(个)和TGFβ1mRNA/β-actin比值(n=8耳)
注:*与硅胶管侧同一时间点比较,P<0.05
增生性瘢痕的治疗方法很多,如硅胶膜、注射类固醇激素、加压治疗等[6],加压疗法是所有非侵入疗法中最有效和应用最广泛的方法之一。李世荣等[7]报道加压能抑制瘢痕组织增生的机理可能是:①压力造成瘢痕组织相对缺血,使螺旋状胶原重新排列,组织二氧化碳分压升高,氧分压降低,血管数量减少,水肿减轻;②压力使血管内皮细胞退变,使血管壁损伤加重,造成组织缺血,抑制了瘢痕增生;③缺氧状态下细胞内氧分压降低,线粒体的功能减退甚至停止,同时发生形态学改变,如线粒体肿胀、空泡变性等,导致承担细胞生物氧化作用的线粒体不能在氧化磷酸化过程中释放能量,致使成纤维细胞的增生受到抑制,最后发生变性坏死,使生成胶原纤维和基质的能力降低,从而抑制了瘢痕增生。治疗开始时间越早,持续的时间越长,其预防和治疗效果越好[8~10]。
使用硅胶管等材料进行加压扩张,防治外耳道再狭窄,存在以下不足:①硅胶管管壁厚、无弹性,难以与外耳道形状相吻合,对外耳道植皮压力分布不均匀,影响外耳道植皮存活;②不易固定、易脱出;③管壁无缝隙,妨碍了外耳道创面渗液的排出并影响耳内滴药的疗效,术后易继发感染。
镍钛记忆合金支架具有独特的形状记忆性能和超弹性,可以通过低温或物理方法将支架缩小口径,通过原来难以经过或不能到达的部位,然后利用温度或超弹性使支架自然膨胀,达到使狭窄管腔扩大的目的。研究表明镍钛记忆合金支架具有良好的力学性能及优良的生物相容性和耐腐蚀性,是一种理想的医用生物材料[2]。
本课题组与南京微创医学科技有限公司合作,设计了供实验用的镍钛记忆合金支架,该支架具有以下特点:①支架直径适合外耳道大小,有弹性,可弯曲,具有超弹性,植入后对外耳道植皮压力分布较均匀,利于植皮存活;②支架呈网格状,外覆带微孔的被膜,便于外耳道创面分泌物的排出和耳内滴药;③研制配套的支架植入设备,使支架容易放置及取出;④支架易固定、不易脱出。本实验显示支架侧外耳道瘢痕组织中成纤维细胞的数量明显少于硅胶管侧,去除扩张物后支架侧的外耳道直径明显大于硅胶管侧,且植皮生长良好,无感染及再狭窄发生,说明镍钛记忆合金支架对兔外耳道瘢痕组织中成纤维细胞的增生有更明显的抑制作用,能有效地抑制外耳道中瘢痕组织的增生。这可能是由于镍钛记忆合金支架对外耳道的压力比硅胶管更大且更均匀的缘故。亦提示TGFβ1可以作为判断瘢痕增生程度的一项辅助指标,从而证实了镍钛记忆合金支架的优越性。
4 参考文献
1 Stoeckel D,Pelton A,Duerig T.Self-expanding nitinol stents: material and design considerations[J]. Eur Radiol,2004,2:292.
2 Wang G,Shen Y,Cao Y,et al.Biocompatibility study of plasma-coated nitinol (NiTi alloy) stents[J].IET Nanobiotechnol,2007,6:102.
3 王孟冬,黄志纯,顾建兴,等. 建立一种兔外耳道瘢痕狭窄的动物模型[J]. 中华耳科学杂志, 2007,4:432.
4 Haverstock BD. Hypertrophic scars and keloids[J]. Clin Podiatr Med Surg,2001,1:147.
5 Klass BR, Grobbelaar AO, Rolfe KJ. Transforming growth factor beta1 signalling, wound healing and repair:A multifunctional cytokine with clinical implications for wound repair, a delicate balance[J].Postgrad Med J,2009,999:9.
6 Juckett G, Hartman-Adams H. Management of keloids and hypertrophic scars[J]. Am Fam Physician,2009, 3:253.
7 李世荣,杨东运. 压力疗法治疗烧伤后瘢痕[J].中国临床康复,2002, 8:1 086.
8 Macintyre L, Baird M.Pressure garments for use in the treatment of hypertrophic scars-a review of the problems associated with their use[J].Burns,2006,1:10.
9 TParikh DA, Ridgway JM, Ge NN. Keloid banding using suture ligature: A novel technique and review of literature[J].Laryngoscope,2008,11:1 960.
10 Chang LW, Deng WP, Yeong EK, et al. Pressure effects on the growth of human scar fibroblasts[J]. J Burn Care Res,2008,5:835.
