以索拉非尼为基础综合治疗晚期原发性肝细胞肝癌的临床研究
2010-01-24钱建民芮晓晖汪昉睿王乾伟马震宇
钱建民, 芮晓晖, 汪昉睿, 王乾伟, 马震宇
肝细胞肝癌(hepatocellular carcinoma,HCC)是肝硬化患者的主要死亡原因,每年全球范围内有近625 000例新发病例,其在癌症病死率中位居第三[1]。目前对此病可选择的治疗方法很多,包括手术干预、介入治疗、放疗、药物和基因免疫治疗等,但只有40%的患者有机会在早期对肿瘤进行相对根治性的手术治疗。因此,延长晚期HCC患者生存期、提高远期疗效成为HCC治疗的重点之一。索拉非尼(sorafenib)在多项大型随机对照治疗HCC的研究中均提示可以显著提高晚期HCC患者的生存时间,我院2008年11月起在晚期原发性肝细胞肝癌患者中应用索拉非尼进行治疗,现回顾性研究索拉非尼单用及与其他方法联合应用在治疗晚期原发性HCC中的疗效。
1 对象与方法
1.1 研究对象 选取2008年11月至2009年7月间在我院经组织学或影像学诊断的无法根治性切除的原发性肝细胞肝癌患者15例,其中男性13例(86.7%),女性2例(13.3%),平均年龄(54.07±13.651)岁。根据BCLC(巴塞罗那临床肝癌分期系统)进行分级,B级9例(60.0%)、C级3例(20.0%)、D级3例(20.0%)。治疗前Child评分A级11例(73.3%)、B级2例(13.3%)、C级2例(13.3%)。
1.2 治疗方法 所有患者均接受索拉非尼(多吉美,拜耳先灵医药公司)治疗,或单一治疗,或以索拉非尼为基础的综合治疗,持续治疗至少2个月以上。索拉非尼给药方案:索拉非尼400 mg,1日2次。
1.3 观察指标 治疗前后肿瘤大小、数目、血管侵犯、淋巴结转移、肝内播散及远处转移情况,并根据BCLC进行分级;治疗前后的肝功能状态、Child评分结果;生存期;开始应用索拉非尼的时间及应用过程中的副反应的发生情况。
1.4 统计学分析 采用SPSS软件(12.0版)进行统计学处理。计量资料以均数±标准差表示,采用t检验;计数资料行χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 不同BCLC分期下患者的平均生存时间(表1) 随访至2010年1月,BCLC-B级患者的平均生存时间为(11.89±6.153)个月,其中8/9人仍存活,继续索拉非尼治疗中;BCLC-C/D级患者的平均生存时间为(9.50±4.637)个月,其中2/6人尚存活,亦继续索拉非尼治疗。两者在生存时间上差异无统计学意义(P=0.434)。而自2004年至2007年间,在我院诊治的晚期原发性肝癌患者中,BCLC-B/C级患者的1年生存率仅12.5%,BCLC-D级患者的1年死亡率达100%。
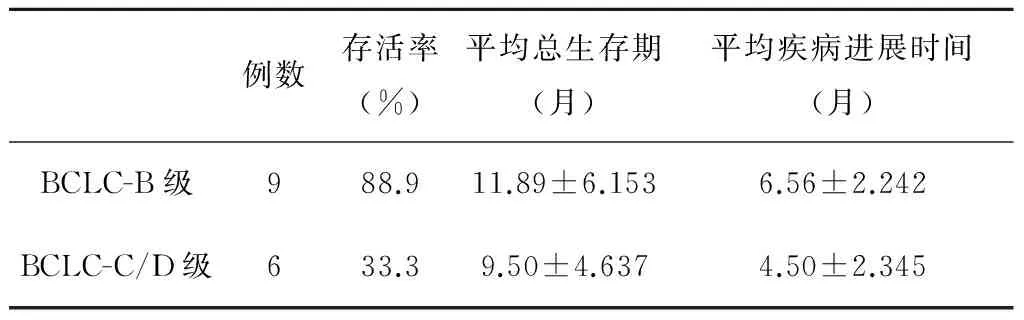
表1 不同BCLC分级的原发性肝癌患者的生存情况
2.2 不同治疗方式的患者生存情况比较(表2) 在15例患者中,4例患者为单用索拉非尼治疗,其余患者均至少联合应用一种其他治疗方式,包括手术、射频消融、射波刀局部照射治疗、静脉化疗、介入治疗。在BCLC-B级患者中仅1例单一治疗,故此处不作讨论。而BCLC-C/D级的患者中,3例(50%)接受索拉非尼单一治疗,平均生存时间8个月,目前1例存活;3例接受综合治疗的患者,平均生存时间11个月,目前也是1例存活。其中1例BCLC-C级患者,诊断后即接受了肝移植手术,移植2个月后出现肿瘤复发及肺部转移病灶,即开始索拉非尼抗肿瘤治疗,同时肺部转移病灶接受了射波刀治疗,之后6个月中,患者肝功能良好,复发及转移病灶均无明显进展,后因肺部病灶进展而死亡,该患者总生存时间13个月。

表2 BCLC-C/D级患者在不同治疗方式下的生存情况
2.3 接受以索拉非尼为基础的综合治疗后的疾病进展时间(表1) 本组患者接受以索拉非尼为基础的综合治疗后,出现6例局部肿瘤扩展,3例新发肺部转移,BCLC-B级患者的平均疾病进展时间为(6.56±2.242)个月,而C、D级患者为(4.50±2.345)个月(P=0.111)。
2.4 索拉非尼应用的耐受情况及副反应报告 索拉非尼应用过程中患者耐受良好,无肝功能异常发生。药物主要的副反应为皮疹(66.7%),发热(13.3%)。仅1例患者因发热予索拉非尼减量至400 mg,每日1次,症状好转后重新加量。
3 讨论
索拉非尼是一种酪氨酸激酶抑制剂、血管生成抑制剂和血管内皮生长因子抑制剂。它具有双重抗肿瘤作用,一方面通过抑制Raf/MEK/ERK信号传导通路直接抑制肿瘤生长[2],另一方面通过抑制几种与新生血管生成和肿瘤发展有关的酪氨酸激酶受体的活性,包括血管内皮生长因子受体22(VEGFR22),血管内皮生长因子受体23(VEGFR23),血小板衍生的生长因子受体2β(PDGFR2β)和c2KIT原癌基因,阻断肿瘤新生血管生成,间接抑制肿瘤细胞的生长,从而起到抗肿瘤作用[3]。索拉非尼是本类化合物中第1个进入临床试验的药物,可在抑制Raf活性的剂量下,显著抑制肿瘤细胞增殖。目前索拉非尼已通过FDA,欧洲医药机构(EMEA)认证,应用于治疗HCC。在2007年ASCO大会公布的一项国际多中心Ⅲ期随机对照治疗肝细胞肝癌的SHARP研究结果(LBAI)[4]提示,索拉非尼显著提高了晚期HCC患者3个月的生存时间,不单单是统计学显著,而且有显著的临床意义,该研究因为治疗组的优势显著而在第二阶段被终止。治疗组的中位生存时间10.7个月,安慰剂组为7.9个月,死亡风险比 0.69,95%CI 0.55~0.87,P<0.001。
在本研究中,所有入组患者均为晚期原发性HCC患者,因肿瘤瘤体过大或肿瘤多发伴肝内播散等原因而失去根治性手术治疗的机会。研究结果显示,本组BCLC-B级患者的平均生存时间为11.9个月,存活率为88.9%,继续综合治疗中;而BCLC分期达C、D级患者的平均生存时间也达到9.5个月。同时我们总结了2004年至2007年我院诊治的晚期原发性肝癌的患者,BCLC-B/C级患者的1年生存率仅12.5%,BCLC-D级患者的1年死亡率达100%。尽管目前接受索拉非尼治疗的患者病例数尚少,但也可得出一个初步的结论,索拉非尼治疗可显著延长晚期HCC患者的生存期。
其次,BCLC-C/D级的患者中,3例接受索拉非尼单一治疗,平均生存时间8个月,3例接受综合治疗,平均生存时间11个月。尽管无显著统计学差异,但仍可看出,在索拉非尼联合手术部分切除肿瘤/射频消融/射波刀局部放疗/静脉化疗/介入治疗时,可能延长原发性肝癌进展期及末期患者的生存时间。但这需要我们进一步增加病例数,延长随访时间,以观察其中的疗效。同时也提示,在索拉非尼抗肿瘤的基础上联合其他治疗的综合治疗可能存在协同作用,这也需进一步研究证实。
[1] Parkin DM, Bray F, Ferlay J, et al. Estimating the world cancer burden: Globocan 2000[J]. Int J Cancer, 2001, 94(2): 153-156.
[2] Wilhelm SM, Carter C, Tang L, et al. BAY 43-9006 exhibits broad spectrum oral antitumor activity and targets the RAF/MEK/ERK pathway and receptor tyrosine kinases involved in tumor progression and angiogenesis[J]. Cancer Res, 2004, 64(19):7099-7109.
[3] Strumberg D. Preclinical and clinical development of the oral multikinase inhibitor Sorafenib in cancer treatment[J]. Drugs Today (Barc),2005,41(12):773-784.
[4] Llovet J, Ricci S, Mazzaferro V, et al. Sorafenib in advanced hepatocellular carcinoma[J].Clin Oncol (2007 ASCO Annual Meeting Proceedings, Part I), 2007, 25(18S). (Abstract LBA1).
