药物基因组学在难治性精神分裂症中的应用
2024-12-31李丽梅罗均何金泉陈婷张志旺


[摘要]"目的"探讨基于药物基因组学选药和基于循证医学选药对难治性精神分裂症(treatment-resistant"schizophrenia,TRS)在疗效及安全性方面的差异。方法"选取2023年1月至2023年10月笔者医院就诊TRS患者100例,分为观察组即基因导向选择抗精神病药物组(男22例,女28例)和对照组即循证医学导向选择抗精神病药物组(男23例,女27例)。观察组用采样刷无创采集口腔黏膜上皮细胞行抗精神病药物基因检测,根据检测结果选用正常代谢、应答佳、不良反应小的抗精神病药,对照组由指定医师根据《中国精神分裂症防治指南2015年修订版》选择药物。使用阳性和阴性症状量表(positive"and"negative"syndrome"scale,PANSS)在基线时及治疗后第4、8周末进行抗精神病治疗疗效评估。使用治疗中需处理的药物不良反应量表药物不良反应量表(treatment"emergent"symptom"scale,TESS)在治疗后第4、8周末评定不良反应。结果"治疗8周末观察组在中枢神经、自主神经、内分泌、心血管、消化方面的不良反应发生率均低于对照组,差异有统计学意义。观察组及对照组在基线时阳性症状、阴性症状、一般精神病理症状得分差异无统计学意义。治疗4周末观察组与对照组的阳性症状、阴性症状、一般精神病理症状得分均低于对照组,差异有统计学意义。治疗8周末观察组与对照组的阳性症状、阴性症状、一般精神病理症状得分差异有统计学意义。治疗后第8周末,观察组的有效率高于对照组,差异有统计学意义(44%"vs."24%,P=0.035)。采用两因素重复测量方差分析,提示两组患者基线时、治疗后4周末、8周末PANSS评分随时间而改变,差异有统计学意义(F时间=697.139,Plt;0.05);PANSS评分组间差异有统计学意义(F组间=5.398,Plt;0.05);PANSS评分随着治疗方法的不同而有所不同,差异有统计学意义(F交互=3.008,Plt;0.05)。结论"基因导向选择抗精神病药在提高有效率及减少药物不良反应方面可能优于循证导向选择抗精神病药。
[关键词]"药物基因组学;个体化用药;难治性精神分裂症;安全性
[中图分类号]"R749.3""""""[文献标识码]"A""""""[DOI]"10.3969/j.issn.1673-9701.2024.23.006
Application"of"pharmacogenomics"in"treatment-resistant"schizophrenia
LI"Limei,"LUO"Jun,"HE"Jinquan,"CHEN"Ting,"ZHANG"Zhiwang
Department"of"Clinical"Psychology,"Chenzhou"First"People’s"Hospital,"Chenzhou"423000,"Hunan,"China
[Abstract]"Objective"To"explore"the"differences"in"efficacy"and"safety"of"drug"selection"based"on"pharmacogenomics"and"evidence-based"medicine"for"treatment-resistant"schizophrenia"(TRS)."Methods"A"total"of"100"patients"with"TRS"in"our"hospital"from"January"2023"to"October"2023"were"divided"into"observation"group"(gene-oriented"antipsychotic"drug"selection"group,"22"males"and"28"females)"and"control"group"(evidence-based"medicine"oriented"antipsychotic"drug"selection"group,"23"males"and"27"females)."Oral"mucosal"epithelial"cells"of"the"observation"group"were"noninvasive"collected"with"a"sampling"brush"and"antipsychotic"drug"gene"detection"was"performed."Antipsychotic"drugs"with"normal"metabolism,"good"response"and"little"toxic"side"effects"were"selected"according"to"the"test"results,"and"the"drugs"of"the"control"group"were"selected"by"the"designated"physician"on"the"basis"of"the"Chinese"Guidelines"for"the"Prevention"and"Treatment"of"Schizophrenia,"2015"revision."Antipsychotic"efficacy"was"evaluated"before"treatment"and"4"weeks,"8"weeks"after"treatment"with"positive"and"negative"syndrome"scale"(PANSS)."Treatment"emergent"symptom"scale"(TESS)"was"used"to"assess"adverse"reactions"at"the"4th"and"8th"weekend"after"treatment."Results"After"8"weeks"of"treatment,"the"incidence"of"adverse"reactions"in"central"nervous"system,"autonomic"nervous"system,"endocrine"system,"circulatory"system"and"digestive"system"in"the"control"group"was"higher"than"that"in"the"observation"group."The"difference"was"remarkable."The"scores"of"positive"symptoms,"negative"symptoms"and"general"psychopathological"symptoms"between"the"observation"group"and"the"control"group"at"baseline"were"basically"the"same"(Pgt;0.05)."After"4"weeks"of"treatment,"the"scores"of"positive"symptoms,"negative"symptoms"and"general"psychopathological"symptoms"in"the"observation"group"were"lower"than"those"in"the"control"group."The"difference"was"remarkable."After"8"weeks"of"treatment,"the"scores"of"positive"symptoms,"negative"symptoms"and"general"psychopathological"symptoms"in"the"observation"group"were"lower"than"those"in"the"control"group."The"difference"was"remarkable."At"the"end"of"the"8th"week"after"treatment,"the"effective"rate"of"the"observation"group"was"higher"than"that"of"the"control"group,"the"difference"was"remarkable"(44%"vs."24%,"P=0.035)."Two-factor"repeated"measurement"analysis"of"variance"was"used,"indicating"that"PANSS"scores"of"the"two"groups"changed"with"time"at"baseline,"4"weeks"and"8"weeks"after"treatment,"and"the"difference"was"remarkable"(F-time=697.139,"Plt;0.05);"The"difference"of"PANSS"among"groups"was"remarkable"(F-groups=5.398,"Plt;0.05);"PANSS"score"was"different"with"different"treatment"methods,"and"the"difference"was"remarkable"(F-interaction=3.008,"Plt;0.05)."Conclusion"Gene-directed"antipsychotic"selection"maybe"is"superior"to"evidence-based"antipsychotic"selection"in"improving"effective"rate"and"reducing"adverse"drug"reactions.
[Key"words]"Pharmacogenomics;"Individualized"medication;"Treatment-resistant"schizophrenia;"Safety
精神分裂症表现为慢性退行性病程,多数患者表现出社会功能减退、认知功能下降。难治性精神分裂症(treatment"of"resistance"to"schizophrenia,TRS)是指过去5年内至少服用过2种抗精神病药物足量、足疗程(4~6周)治疗后均未充分缓解[1]。以往抗精神病药选择主要参考精神分裂症诊疗指南,但是临床实践中精神分裂症患者对抗精神病药物的反应有个体化差异,药物基因组学(pharmacogenomics,PGx)表明药物治疗效果的个体差异与转运体、药物作用受体、药物代谢酶的基因多态性有关[2]。基因多态性检测有利于制定个体化的用药方案,个体化用药将成为未来精神分裂症治疗的主导模式[3]。抗精神病药物基因多态性的研究当前多局限在单个基因的多态性与药物效果的探讨,尚无依据多个基因多态性与精神病类药物疗效及安全性的研究。本研究对目前国内外已达成共识的抗精神病药物代谢、应答、不良反应相关的30个基因多态位点进行检测分型,并依抗精神病药基因检测结果选药,对比基因导向选择抗精神病药和循证医学导向选择抗精神病药的疗效及安全性差异,探讨抗精神病药物基因检测的临床价值,从而为对TRS患者实施精准的个体化治疗提供理论依据。
1""资料与方法
1.1""一般资料
选取2023年1月至2023年10月在笔者医院就诊的100例TRS患者纳入研究。入组标准[1]:①符合《国际疾病分类第11版》精神分裂症的诊断标准;②阳性和阴性症状量表(positive"and"negative"syndrome"scale,PANSS)总分gt;70分;"③过去5年内至少服用过2种抗精神病药物足量、足疗程(4~6周)后均未充分缓解;④年龄12~60岁。排除标准:①非功能性精神障碍者;②物质滥用者;③患病其他精神障碍者;④精神发育迟滞者。采用随机数字法分为观察组即基因导向选择抗精神病药组,对照组即循证医学导向选择抗精神病药组。观察组50例,其中,男22例,女28例,平均年龄(22.12±3.83)岁,平均病程(3.60±1.43)年;对照组50例,其中,男23例,女27例,平均年龄(22.20±3.46)岁,平均病程(3.43±1.54)个月。两组性别比例、年龄、病程比较,差异均无统计学意义(Pgt;0.05)。见表1。本研究经笔者医院伦理委员会审核批准(伦理审批号:科研第2023001号),所有患者、家属均签署知情同意书。
1.2""检测与治疗方法
1.2.1""药物基因组学检测""观察组用采样刷无创采集口腔黏膜上皮细胞的方法进行标本收集,由顺丰快递冷藏下48h内送至上海康黎医学检验所有限公司进行药物基因组学检测72~96h内出结果,该公司使用MassARRAY"DNA飞行时间质谱基因分析系统对目前国内外已达成共识的抗精神病药物代谢相关基因(CYP1A2、CYP2D6、CYP3A4),应答相关基因(DRD2-1、DRD2-II、COMT、RGS4、EPM2A、CACNA1C、CNTN4、ERBB4、NFKB1-1、NFKB1-II、NFKB1-III、PCDH7、SLC1A1、HTR1A-1、HTR1A-II、DRD2-IV),不良反应相关基因(CYP1A2-1、MC4R、HTR2C-1、ANKK1、HLA-DQB1、HLA-DRB3、HSPG2、PTPRD、RABEP1、SLC18A2、HTR2C-II)的多态位点进行检测分型。
1.2.2""药物干预方案""对照组首选氯氮平(200~"600mg/d)联合重复经颅磁刺激治疗,如治疗4周后未能获得满意疗效则联用利培酮(3~10mg/d)治疗;如无法耐受氯氮平的不良反应则停用氯氮平改为奥氮平(5~20mg/d)联合利培酮(3~10mg/d)治疗。
观察组药物基因检测结果会将药物根据代谢情况分为正常代谢、快代谢、慢代谢;根据药物疗效分为应答佳、应答不佳;根据不良反应分为不良反应风险较低、不良反应风险较高。在药物基因检测结果未出之前按对照组的原则选用药物,待药物基因检测结果出来后选用正常代谢、应答佳、不良反应风险较低的单种药联合重复经颅磁刺激治疗,优先选择二代抗精神病药,在二代抗精神病药中优先级别从高到低是:氯氮平(200~600mg/d)、奥氮平(5~20mg/d)、利培酮(3~10mg/d)、氨磺必利(400~800mg/d)、阿立哌唑(15~30mg/d);治疗后4周未获得满意疗效则联合上述另一种作用机制不同的正常代谢、应答佳、不良反应风险较低的抗精神病药。
1.2.3""量表评估""PANSS含7条阳性症状条目、7条阴性症状条目和16条一般精神病理症状条目,每个条目依症状轻到重评为1~7分,阳性及阴性症状量表得分范围为7~49分、一般精神病理症状量表的得分范围为16~112分,总分为3个分量表得分之和,得分越高提示症状越严重。治疗后第4、8周末两组分别与各自基线时的PANSS总分、阳性症状得分、阴性症状得分、精神病理得分进行组内比较;于基线时及治疗后第4、8周末进行PANSS量表总分、阳性症状得分、阴性症状得分、精神病理得分组间比较。PANSS减分率=[(基线分-该访视点得分)/基线分]×100%,PANSS减分率≥50%为有效,PANSS减分率lt;50%为无效。所有量表评估均由同一位医师执行。
1.2.4""安全性评估""药物不良反应量表(treatment"emergent"symptom"scale,TESS)用于评估抗精神病药的行为毒性、心血管系统、神经系统、自主神经系统等方面的不良反应,得分越高提示药物不良反应越多。于基线时及治疗后第4、8周末进行血常规、肝肾功能、心电图检查,使用TESS在治疗后第4、8周末评定不良反应。
1.3""统计学方法
采用SPSS"22.0统计学软件对数据进行处理分析,符合正态分布的计量资料以均数±标准差( )表示,组间比较采用t检验,多个时间点内组间和组内差异比较采用重复测量的方差分析。计数资料用例数(百分率)[n(%)]表示,组间比较用χ²检验。缺失数据用末次观察结转法补充。Plt;0.05为差异有统计学意义。
)表示,组间比较采用t检验,多个时间点内组间和组内差异比较采用重复测量的方差分析。计数资料用例数(百分率)[n(%)]表示,组间比较用χ²检验。缺失数据用末次观察结转法补充。Plt;0.05为差异有统计学意义。
2""结果
2.1""TESS发生率比较
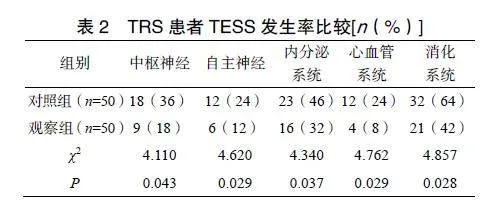
观察组在中枢神经、自主神经、内分泌系统、心血管系统、消化系统方面的不良反应发生率均低于对照组,差异有统计学意义(均Plt;0.05)。见表2。
2.2""PANSS量表评分比较
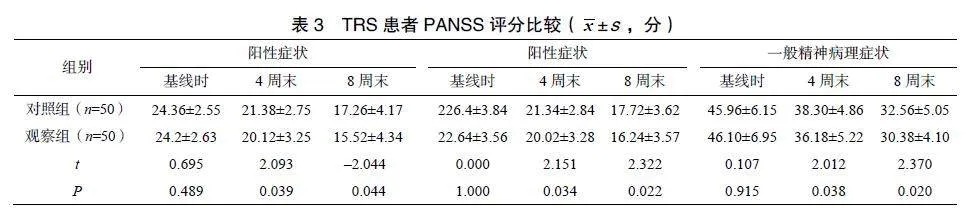
两组患者治疗前阳性症状、阴性症状、一般精神病理症状得分比较,差异无统计学意义,(均Pgt;0.05);治疗4周末、8周末时观察组的阳性症状、阴性症状、一般精神病理症状得分均低于对照组,差异有统计学意义(均Plt;0.05)。见表3。
2.3""治疗8周末有效率比较
治疗8周末对照组有效12例,有效率为24%,观察组有效22例,有效率为44%,两组比较,差异有统计学意义(χ2=4.456,P=0.035)。
2.4""两因素重复测量方差分析结果
采用两因素重复测量方差分析,判断依据药物基因导向选药及依据循证医学导向选药随着时间变化对精神分裂症严重程度的改善作用。两组患者基线时、治疗后4周末、8周末PANSS评分随时间而改变,差异有统计学意义(F时间=697.139,Plt;0.05)。PANSS评分组间差异有统计学意义(F组间=5.398,Plt;0.05),PANSS评分随着治疗方法的不同而有所不同,差异有统计学意义(F交互=3.008,Plt;0.05)。见表4。
3""讨论
精神分裂症在成年人群中的终生患病率接近1%,23%~58%的患者最终成为TRS[4-5]。TRS主要是通过抗精神病药物进行治疗,但临床中不同TRS患者对同一种抗精神病药物的疗效及不良反应存在个体差异。PGx通过研究药物代谢酶、转运体和作用靶点的基因多态性对药代学与药效学的影响,可以提供个体化用药建议[6]。
本研究提示治疗4周末、8周末时观察组的阴性症状、阳性症状、一般精神病理症状得分均低于对照组,差异有统计学意义(Plt;0.05)。对照组的有效率24%,观察组的有效率44%,差异有统计学意义(Plt;0.05)。与兰吴沅等[7]的研究结论一致,其研究发现治疗1个月后,根据药物基因检测用药的TRS患者阴性症状、阳性症状、一般精神病理症状评分均低于对照组。潘丽红等[8]予精神分裂症患者服用利培酮8周后发现DRD2基因rs1801028位点不同基因型在阴性症状减分率上差异有统计学意义(F=15.29,Plt;0.001),rs6277位点在阳性症状减分率上差异有统计学意义(F=14.74,Plt;0.001)。08CYP2D6基因检测为TT、10CYP2D6基因检测为GG、06CYP2D6基因检测为CC、基因型分析结果为*10/*10,代谢型为IM的精神分裂症患者选用利培酮系统治疗,可取得较好的临床疗效[9]。ANKK1"rs1800497基因多态性与奥氮平治疗精神分裂症的疗效(尤其是阳性症状)有关联[10]。研究表明,ANKK1"CpG位点387的甲基化水平可能与阿立哌唑治疗精神分裂症的疗效有关,HTR1A"rs6295多态性可能影响抗精神分裂症药物对阴性症状的改善,但不影响总体症状或阳性症状的改善。氯氮平疗效与HTR2A基因多态性的关系的研究中发现His452Tyr位点多态性与氯氮平临床疗效相关[11-13]。PGx通过对TRS患者抗精神病药应答相关基因多态性的检测,预测TRS患者应用抗精神病药的效果,临床医师根据预测结果选择应答好的抗精神病药,可明显提高治疗效果。
本研究观察组在神经系统、自主神经、内分泌系统、心脏系统、消化系统方面的不良反应发生率均低于对照组,差异有统计学意义(Plt;0.05)。兰吴沅等[7]研究亦发现基于PGx用药有利于降低TRS患者使用抗精神病药物的不良反应发生率。研究表明HTR2C基因-759位有T等位基因(TT或CT)的患者比没有T等位基因的精神分裂症患者使用抗精神病药后体重增加更少。HTR1A的C等位基因携带者在氟哌啶醇单药治疗2周后,比TT基因型患者静坐不能严重程度更高。氯氮平血药浓度依赖的不良反应与CYP3A4的基因多态性有关,在CYP3A4低表达者中氯氮平血药浓度更高,过高的氯氮平血药浓度与高血糖、肥胖的发生率有关。ANKK1基因功能多态性rs2734849与抗精神分裂症药物诱导的高催乳素血症相关[14-17]。徐静文等[10]研究发现ANKK1"rs1800497基因的T等位基因可能增加奥氮平发生肥胖和高血糖的风险。PGx通过对TRS患者基因多态性的检测,预测抗精神病药的不良反应,临床医生可以根据不良反应的预测选择不良反应小的抗精神病药。
综上所述,基于PGx的个体化用药有利于降低抗精神病药物的不良反应,提高抗精神病药物的疗效。但本研究仅100例,研究的周期仅8周,尚需大样本量、多中心、长期随访研究进一步探讨基于PGx的个体化用药对TRS患者的疗效及安全性。
利益冲突:所有作者均声明不存在利益冲突。
[参考文献]
[1] 陆林,"方贻儒,"江开达,"等."沈渔邨精神病学[M]."6版."北京:人民文书出版社,"2021:"328.
[2] HAUFROID"V,"PICARD"N."Pharmacogenetics"biomarkers"predictive"of"drug"pharmacodynamics"as"an"additional"tool"to"therapeutic"drug"monitoring[J]."Ther"Drug"Monit,"2019,"41(2):"121–130.
[3] 岳伟华,"王强."药物基因组学在精神分裂症精准医疗中的应用[J]."中华精神科杂志,"2020,"53(6):"469–472.
[4] MURRAY"C"J"L,"LOPEZ"A"D."Measuring"global"health:"motivation"and"evolution"of"the"global"burden"of"disease"study"[J]."Lancet,"2017,"390(10100):"1460–1464.
[5] 司天梅,"于欣."难治性精神分裂症的研究进展[J].nbsp;中华精神科杂志,"2018,"51(3):"157–162.
[6] 谢秋芬,"种姗,"胡琨,"等."国内外药物基因组学相关指南的现状[J]."中国临床药理学杂志,"2022,"38(16):"1954–1957.
[7] 兰吴沅,"胡伟明,"兰智勇."药物基因组学检测在难治性精神分裂症患者中的临床效能[J]."中华全科医学,"2023,"21(2):"238–241.
[8] 潘丽红,"王继军,"姚琳,"等."精神分裂症患者多巴胺D2受体基因多态性与利培酮治疗效应的关联分析[J]."临床精神医学杂志,"2019,"29(3):"161–164.
