丹参酮ⅡA磺酸钠经脱磺化反应制备丹参酮ⅡA的研究
2024-10-29吴良江锡铭俞伟
摘 要 本文报告一种以丹参酮ⅡA磺酸钠为原料经脱磺化反应制备高纯度丹参酮ⅡA的方法。通过对酸试剂、溶剂、温度以及溶剂用量的系统筛选,得到较优的条件,以浓盐酸等作为反应试剂,乙腈为溶剂,80 ℃下反应3 h,能够以最高大于90%的收率获得大于99%纯度的丹参酮ⅡA。反应操作简单,收率高,具有工业化生产前景。
关键词 丹参酮ⅡA磺酸钠 丹参酮ⅡA 脱磺化
中图分类号:TQ460.6; TQ463.42 文献标志码:A 文章编号:1006-1533(2024)17-0077-05
引用本文 吴良, 江锡铭, 俞伟. 丹参酮ⅡA磺酸钠经脱磺化反应制备丹参酮ⅡA的研究[J]. 上海医药, 2024, 45(17): 77-80; Ⅲ.
Preparation of tanshinoneⅡA by desulfonation reaction of sodium tanshinoneⅡA sulfonate
WU Liang, JIANG Ximing, YU Wei
(Shanghai NO.1 Biochemical and Pharmaceutical Co., Ltd., Shanghai 200240, China)
ABSTRACT This study reported a method for preparing high-purity tanshinoneⅡA by desulfonation reaction using sodium tanshinoneⅡA sulfonate as raw material. The relatively optimal reaction conditions were obtained by screening the acid reagents, temperature, solvents and their dosages. Using concentrated hydrochloric acid as a reaction reagent, acetonitrile as a solvent and reacting at 80 ℃ for 3 hours, tanshinoneⅡA with a purity of over 99% were obtained with a maximum yield of over 90%. The reaction operation of this method is simple, the yield is high, and it has the prospect of industrial production.
KEY WORDS sodium tanshinoneⅡA sulfonate; tanshinoneⅡA; desulfonation
中国药典2020年版中记载药材丹参是唇形科鼠尾草属植物丹参的干燥根及根茎,是我国传统常用中药,具有悠久的使用历史[1]。丹参的活性成分包括脂溶性的丹参酮类化合物,目前已经成功分离出数十种化合物,其中含量最多的成分为丹参酮ⅡA,占比约为0.3%~0.8%,且药理活性较高[2-4]。近年来丹参酮ⅡA及类似物的合成也受到了越来越多的关注与研究[5-8]。
目前获得丹参酮ⅡA的主要方法是从丹参药材中提取,主要包括超声提取法、醇提取法、索氏提取法等。王承学等[9]利用超临界二氧化碳萃取法,通过对压力、温度、时间、乙醇流量等条件的优化,在最优条件下能够得到丹参酮ⅡA的混合物,其中丹参酮ⅡA的纯度约为28%。马磊等[10]利用乙醇回流方法提取丹参酮ⅡA,考察了溶剂类型、用量以及提取时间等,实现了丹参酮ⅡA的高效提取,提取率大于90%,丹参酮ⅡA纯度约为4%。刘明娣等[11]用利用分子蒸馏法提取丹参中丹参酮ⅡA,能够获得最高84%的提取率丹参酮ⅡA纯度约为21%。杨立勇[12]等报道了丹参酮ⅡA的微波提取法,得到丹参酮ⅡA的混合物,但纯度较低。
目前采用上述常规方法提取分离丹参酮ⅡA的提取率较高,但是只能获得低纯度的丹参酮ⅡA混合物,综合效率较低,如果要进一步提高纯度,就要用到制备液相等手段,这样就会大大提高成本,并且无法大规模制备。随着近年来丹参酮ⅡA需求量的增加以及我国对药品注册要求的提高,制备高纯度丹参酮ⅡA显得尤为重要。本研究在酸存在的条件下,通过对丹参酮ⅡA磺酸钠进行脱磺化反应制备高纯度的丹参酮ⅡA,能解决丹参酮ⅡA含量较低的问题。
1 材料和方法
1.1 试剂和仪器
丹参酮ⅡA磺酸钠(自制,纯度>99%,批号71D230319);异丙醇(CINC公司);四氢呋喃(Fisher公司);其余化学试剂均为市售产品。LC-2030C Plus高效液相色谱仪(日本岛津公司)。
1.2 实验方法
1.2.1 HPLC测定方法
参考李博等[13]方法操作。该方法线性范围1.6~39.2 mg/mL(r=0.999 9),最低检测限10 ng/mL,回收率99.1%(n=9),精密度(RSD)为0.44%(n=6)。
1.2.2 合成方法
称取丹参酮ⅡA磺酸钠396 mg(1.0 mmol,1.0 equiv,纯度99.2%)置于100 mL单口烧瓶中,加入磁子及相应溶剂,搅拌,随后加入酸,加热到相应温度,反应一段时间后,冷却到室温后减压除去溶剂,加入二氯甲烷溶解,再用纯化水萃取洗涤2次(100 mL×2)。随后用无水硫酸钠干燥后过滤,滤液减压除去溶剂,在45℃真空减压干燥,得到红色固体丹参酮ⅡA。
反应规模放大。称取丹参酮ⅡA磺酸钠1 584 g(40 mmol,1.0 equiv)于10 L反应瓶中,加入6.5 L乙腈,搅拌,随后缓慢加入37%浓盐酸33.2 mL(40 mmol,1.0 equiv)加热至80 ℃,搅拌反应6 h,冷却到室温后减压除去溶剂,加入3 L二氯甲烷溶解,再用水萃取洗涤3次(1 L×3)。用无水硫酸钠干燥4 h,过滤并减压除去溶剂,真空减压干燥约5 h,得到红色固体丹参酮ⅡA。
2 结果
2.1 条件优化
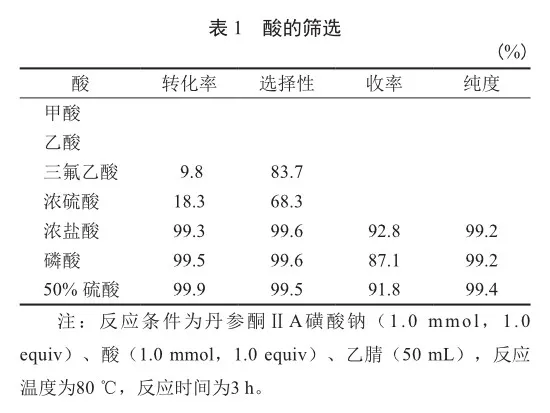
酸的种类对脱磺化反应起到至关重要的作用,因此我们首先考察了不同的酸对丹参酮ⅡA磺酸钠脱磺化反应的影响(表1)。结果表明甲酸或者乙酸无法促进反应的进行,当以三氟乙酸和浓硫酸作为酸时,也只能获得微量的脱磺化产物。令我们高兴的是,浓盐酸能够高效地促进反应的进行,以92.8%的收率获得纯度为99.2%的目标产物丹参酮ⅡA;磷酸也能促进反应的进行,但收率略有下降。当将浓硫酸用水稀释到50%时,脱磺化反应能够顺利进行。这表明丹参酮ⅡA磺酸钠脱磺化反应需要游离的H+存在,反应才能发生,因此初步选用浓盐酸为酸试剂。
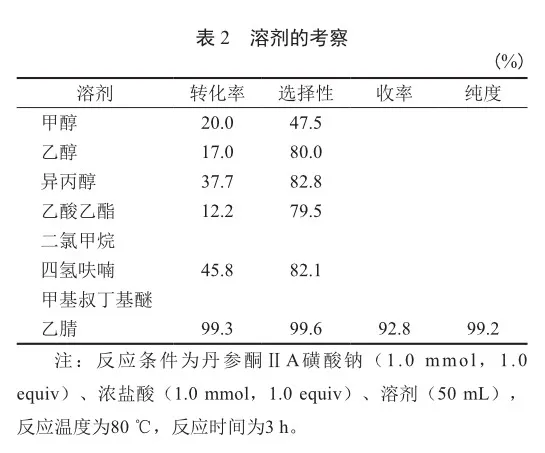
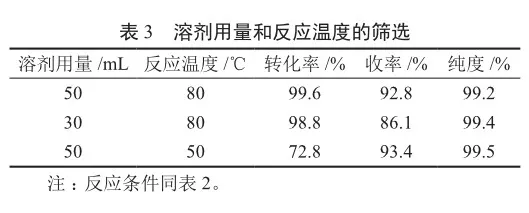
随后我们筛选了不同溶剂对反应的影响(表2)。当以甲醇、乙醇作为溶剂时,仅获得小于20%的转化率,且选择性较差;以异丙醇为溶剂时,转化率有所提高,但选择性还是不理想;当在二氯甲烷和甲基叔丁基醚中反应无法进行;当选用醚类溶剂四氢呋喃时,仅获得45.8%的转化率。结果表明,只有以乙腈为溶剂时,反应能够高效进行,且获得大于99%的转化率以及大于99%的选择性。减少乙腈的用量,反应收率略有下降,降低温度到50 ℃时,反应收率有明显下降,但对目标产物的纯度几乎没有影响(表3)。
最后我们得到相对较优的条件为:浓盐酸作为酸试剂,乙腈为溶剂,80 ℃下反应3 h能够以92.8%的收率得到纯度大于99%的脱磺化产物丹参酮ⅡA。
2.2 反应放大
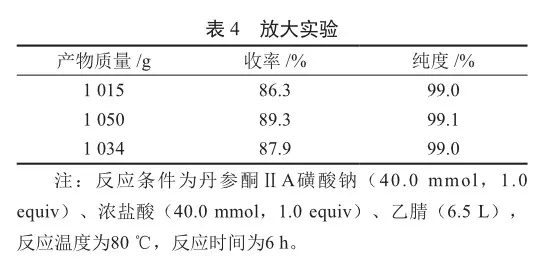
在较优条件下,对反应规模进行了放大。丹参酮ⅡA磺酸钠1 584 g,进行脱磺化反应,得到红色固体1 015 g,产率为86.3%,纯度99.0%。再次重复以上实验2次,结果如表4所示。该方法具有工业化应用前景。
2.3 纯度测定
后处理得到的脱磺化红色固体丹参酮ⅡA经HPLC检测,保留时间8.358 min处的峰为丹参酮ⅡA磺酸钠、20.515 min处的峰为丹参酮ⅡA;丹参酮ⅡA磺酸钠原料基本反应完,产物丹参酮ⅡA的纯度大于99%(图1)。
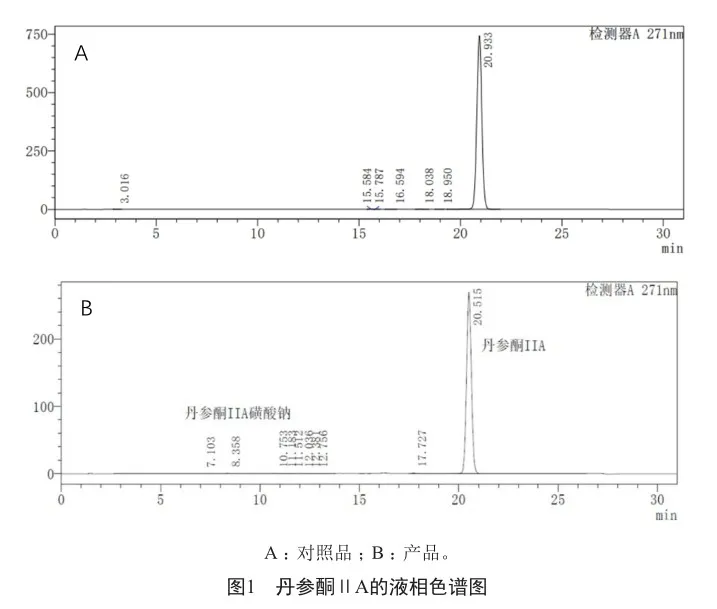
2.4 结构鉴定与解析
将丹参酮ⅡA磺酸钠和丹参酮ⅡA分别进行NMR分析,用氘代甲醇为溶剂。丹参酮ⅡA磺IVCr2pTHVedFRxA2HiaQuwDBbnN8LXTg6eVYnQ+HHAc=酸钠的核磁数据如下:1H NMR(600 MHz,Methanol-d4)δ 7.81(d,J=8.4 Hz,1H),7.74(d,J=8.4 Hz,1H),3.18(t,J=6.6 Hz,2H),2.47(s,3H),1.86~1.79(m,2H),1.73~1.66(m,2H),1.33(s,6H);13C NMR(151 MHz,Methanol-d4)δ 184.1,177.1,161.7,153.0,152.0,145.5,135.1,128.2,128.1,122.0,121.3,121.0,39.1,35.8,32.2,31.2,20.2,9.7。丹参酮ⅡA数据如下:1H NMR(600 MHz,Methanol-d4)δ7.77(d,J=7.8 Hz,1H),7.62(d,J=7.8 Hz,1H),7.45(dd,J=2.4,1.2 Hz,1H),3.17(t,J=6.0 Hz,2H),2.23(d,J=1.2 Hz,3H),1.84~1.79(m,2H),1.70~1.67(m,2H),1.33(s,6H);13C NMR(151 MHz,Methanol-d4)δ 184.6,151.4,145.4,143.3,135.1,128.8,127.7,122.2,121.5,49.6,39.1,35.7,32.2,31.2,20.3,8.8。对比两者的数据,在氢谱中产物丹参酮ⅡA在化学位移为7.45的位置多了一个氢,为丹参酮ⅡA磺酸钠连接磺酰基的15位脱磺化后多出的一个氢(图2)。
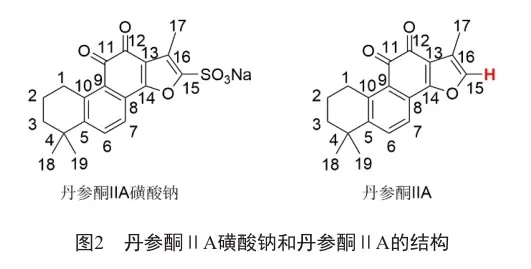
随后将丹参酮ⅡA磺酸钠和丹参酮ⅡA分别进行高分辨质谱分析。丹参酮ⅡA磺酸钠的高分辨质谱数据如下:其分子离子峰C19H17NaO6S (M+H)+=397.072 2。丹参酮ⅡA的高分辨质谱数据如下:其分子离子峰C19H18O3(M+H)+=295.133 4。对比两者数据,发现相差一个磺酰基的分子量。
综合上述数据可知,反应得到的红色固体为脱磺化产物丹参酮ⅡA。
3 讨论
丹参酮ⅡA制备的传统方法主要是从丹参药材中进行提取,本研究提供的一种高纯度丹参酮ⅡA的制备方法。在酸存在的乙腈溶剂中,丹参酮ⅡA磺酸钠经脱磺化,以及简单的后处理,能够得纯度大于99%的丹参酮ⅡA产物。与传统工艺相比,这一反应操作简便,条件温和,产品收率高,同时其副产物少,容易分离,产品纯度高。但是本方法用到浓盐酸,反应温度较高,具有一定的危险性。计划将该反应设计成连续流合成工艺,提高安全性。
通过文献调研和实验结果,我们推测丹参酮ⅡA磺酸钠脱磺化的机理如图3所示。丹参酮ⅡA磺酸钠在反应条件下解离得到中间体1,使得其芳环电子云密度增大,随后H+进攻芳环结构得到中间体2,最后SO3离去得到脱磺化产物丹参酮ⅡA。研究表明乙腈中氰基中C、N之间以sp杂化三键相连,杂化轨道中s成分越多,其电负性越大,体现在整个分子上,氰基更为吸电子,故其偶极矩更大,在该反应中起到促进磺酰基离去的作用,使反应能够顺利发生。
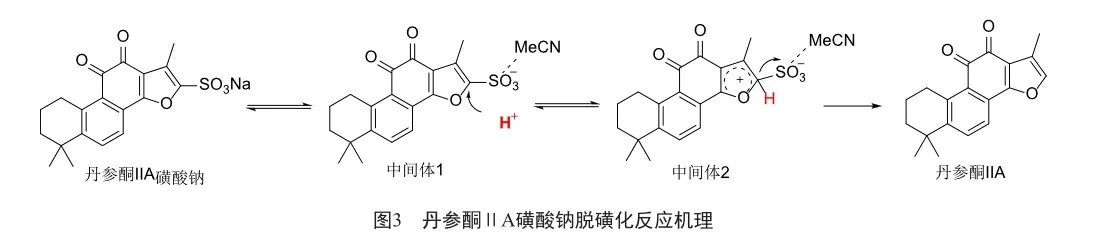
致谢:感谢上海交通大学分析测试中心在高分辨质谱和磁共振测定中提供的帮助。
参考文献
[1] 国家药典委员会. 中华人民共和国药典2020年版一部[M].北京: 中国医药科技出版社, 2020: 126.
[2] 刘春晓. 丹参酮ⅡA分离纯化工艺的研究[J]. 中国民族民间医药, 2012, 21(16): 52-53.
[3] 杜冠华, 张均田. 丹参现代研究概况与进展(续一)[J]. 医药导报, 2004, 23(6): 355-361.
[4] 杜冠华, 张均田. 丹参现代研究概况与进展[J]. 医药导报, 2004, 23(7): 435-440.
[5] 黄鹤. 丹参酮ⅡA及类似物的合成和生物活性研究[D]. 河南: 郑州大学, 2021.
[6] 姚连琦, 秦立玙, 李雯, 等. 丹参酮ⅡA衍生物的合成[J]. 现代生物医学进展, 2018, 18(2): 205-209.
[7] 许昌胜, 陈莉. 丹参酮ⅡA及其类似物的全合成和结构修饰研究进展[J]. 药学进展, 2013, 37(2): 58-65.
[8] 姚占静, 郭睿, 张春生, 等. 丹参酮ⅡA磺酸钠合成工艺研究[J]. 天然产物研究与开发, 2009, 21(3): 506-508.
[9] 王承学, 刘锐. 超临界CO2萃取丹参酮ⅡA提取工艺[J]. 长春工业大学学报(自然科学版), 2007, 28(4): 457-460.
[10] 熊加伟, 葛松兰, 马磊. 丹参中丹参酮ⅡA 和丹酚酸B的提取与纯化工艺研究[J]. 天然产物研究与开发, 2017, 29(8): 1396-1402.
[11] 刘明娣, 王华芳. 分子蒸馏法提取丹参中丹参酮ⅡA工艺的研究[J]. 三门峡职业技术学院学报. 2018, 17(2): 144-148.
[12] 潘胜菊, 杨立勇, 徐剑, 等. 基于多指标评价的丹参微波提取与传统提取的工艺对比研究[J]. 辽宁中医杂志, 2016, 43(10): 2160-2163.
[13] 李博, 陈磊, 刘明理, 等. RP-HPLC法测定注射用丹参酮ⅡA磺酸钠含量和有关物质[J]. 药物分析杂志, 2007, 27(7): 965-967.
