TiO2光催化改性方法研究进展
2024-09-20高同舟刘维于涛铭

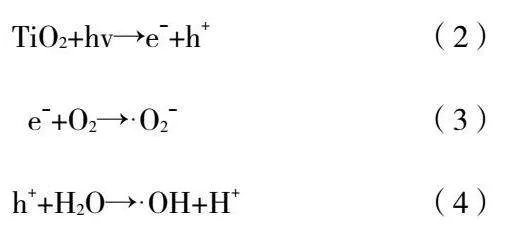
摘 要:TiO2光催化技术凭借TiO2优良的光电性能,在消除水环境有机污染物方面有着广泛的应用前景,其作为光催化剂时通过紫外光或小范围太阳光生成的·OH和·O2-,几乎能够将有机物完全矿化,且无二次污染。介绍了高级氧化法中的光催化氧化的基本原理,详细论述了近年来国内外TiO2光催化改性方法应用现状,提出多种改性方法协同的发展方向。
关 键 词:TiO2;··OH;光催化氧化;原理
中图分类号:O472 文献标识志码: A 文章编号: 1004-0935(2024)08-1265-04
在经济高速发展的同时,难免以牺牲环境为代价,化石燃料的不断使用加剧了环境恶化。其中,水资源作为人类赖以生存的必需品,不仅极其短缺,而且污染较为严重。所以,回收再利用水资源是当前改善环境的重要方向,传统的物理、化学法在处理污水上效果并不好,尤其面对难去除的小分子污染物,而且容易反复,难以长时间保持。
高级氧化技术又称作深度氧化技术,通过光、电、催化剂和氧化剂,产生羟基自由基(·OH),·OH具有极强的氧化性,氧化电位为2.8eV,羟基自由基的反应能可以达到400 MJ·mol-1以上,远大于一般有机物的键能[1]。而且对污染物的选择性小,与有机物反应至接近完全矿化的程度,是处理水中污染物的优良选择。高级氧化技术包括光催化氧化法、催化湿式氧化法、声化学氧化法、臭氧氧化法和Fenton氧化法以及在Fenton基础上逐渐发展的类Fenton法,目前已成为水污染治理的研究方向。
1 TiO2光催化机理
光催化氧化是用可见光或者紫外光照射半导体催化剂,充满电子的低能价带(VB)和空的高能导带(CB)之间的区域称为禁带宽度,当照射光的能量大于半导体催化剂的禁带宽度时,它会使VB上的电子跃迁至CB,并留下空穴,形成电子-空穴 对[2]。一般粒径越小,比表面积越大,光催化性能更好,但是比表面积增大到一定程度也会使TiO2表面的复合中心增加,使吸收光谱发生蓝移,可利用的可见光范围减小。目前来说,TiO2作为半导体催化剂的研究依然是最多的。
20世纪70年代FUJISHIMA和HONDA在《Nature》杂志上发表了关于TiO2分解水并产生氢气和氧气的文章,揭开了TiO2作为光催化剂研究的序幕。TiO2通常以锐钛矿、金红石和板钛矿等晶型形式存在,带隙能量依次为3.2、3.0、3.3eV。金红石型和锐钛矿型是光催化剂主要形态,锐钛矿型没有金红石矿型稳定,当制备过程中温度达到500~600℃时,会促使锐钛矿型向金红石矿型转化。锐钛矿型空穴位较多,光催化性能更强[3]。刘峰强等[4]利用水热法制得的TiO2溶胶为锐钛矿型,在紫外光下160min对甲基橙的降解率可达到91.4%。半导体吸收波长与能量的关系式如下所示:
λ=1240/Eg(1)
当用能量大于3.2eV的光照射时,代入关系式,即波长小于387.5nm的光照射,价带电子才会被激发产生跃迁,在TiO2表面会形成电子-空穴对,电子-空穴对在TiO2表面反应生成羟基自由基(·OH)和超氧自由基(·O2-),·OH和·O2-氧化能力极强,可以破坏有机物的C—C、C—H、C—O等化学键,将大部分有机污染物矿化生成二氧化碳和水等物质,羟基自由基(·OH)和超氧自由基(·O2-)生成原理方程式如下所示:
TiO2+hv→e-+h+(2)
e-+O2→··O2-(3)
h++H2O→··OH+H+ (4)
2 TiO2制备方法
TiO2的制备方法根据反应物系的不同分为固相法、气相法和液相法。目前应用较多的方法有溶胶凝胶法、水热法、微乳液法。溶胶凝胶法主要经过凝胶、干燥、焙烧和固化4个阶段,操作简单,而且制备纯度较高,是目前应用较多的一种制备方法;水热法是在密闭体系中,一定温度和压力进行反应,晶粒分布均匀无团聚,但是成本较高;微乳液法是首先水、油和表面活性剂形成微乳液稳定体系,其次通过成核、聚结、团聚和热处理制得,具有装置简便、能耗低等特点。
3 TiO2改性方法
尽管TiO2是当前选择较多的光催化剂,且具有成本低、抗腐蚀、无毒和化学性质稳定等优点。但是它同时存在易失活、凝聚、对太阳光利用率较低、电子-空穴对复合严重等缺点[5]。目前对TiO2改性的方法主要有离子掺杂、贵金属沉积、半导体复合构建异质结和染料敏化等。
3.1 离子掺杂改性
3.1.1 金属离子掺杂
金属离子掺杂主要包括过渡金属掺杂和镧系稀土金属掺杂。过渡金属掺杂机理认为是过渡金属具有多种价态,d轨道的电子跃迁进入TiO2晶格,影响TiO2的光催化活性。金属离子取代Ti4+,在TiO2晶格中引入缺陷或改变结晶度等,形成杂质能级,扩大可见光的反应范围;利用氧化还原势正于TiO2导带的金属短暂捕获导带中电子,形成浅俘获阱,可以抑制光生电荷载流子的复合,增加了活性位点,从而使TiO2的催化效率提高。史弘宇等[6]研究表明控制实验条件为反应时间150min、pH=9.2和Ag/TiO2投加量0.4g时,Ag/TiO2在可见光下降解40g·L-1亚甲基蓝的效果与单一TiO2在紫外光降解条件下的降解效果相当,说明Ag掺杂提高了TiO2的可见光响应范围。张毛进等[7]实验发现Fe/TiO2经过NaOH处理后,提高了催化剂的比表面积,禁带能量减小到1.80eV,且优于单一TiO2对亚甲基蓝的降解效果。马涛等[8]证明稀土Ce的掺杂有效抑制了电子空穴对的复合。目前,对于金属离子掺杂改性TiO2的研究中Fe、Zn和Cu离子的研究较多[9]。
镧系稀土金属具有不完全的d轨道和f轨道,稀土元素掺杂会增加二氧化钛表面吸附羟基的数目,羟基进一步和光生空穴反应产生更多的·OH[10]。陈恩伟等[11]采用溶胶凝胶法制备得到镧系元素掺杂的TiO2,PLS谱和SPS谱显示的结果一致,即镧系元素的掺杂减少了电子-空穴对的再复合,促进了其分离,研究发现铽离子掺杂活性高于其他离子,并且2%为最优掺杂量。VIET等[12]制备经La掺杂后的La-TiO2在光照下对苯酚的降解率由64.%提升到93.4%,可见光响应范围增加到470nm,禁带宽度降低到2.64eV。
3.1.2 非金属离子掺杂
非金属离子掺杂认为是非金属替代了TiO2晶格中的O,非金属中能级与O的2P轨道能量接近的P轨道与O的2P轨道发生轨道杂化,形成杂化能级,降低了TiO2的带隙能,使可照射光范围发生红移,提高了TiO2对可见光的吸收,从而提高对太阳光的吸收效率。相较于金属元素,非金属元素掺杂更能减少电子复合率。陆成龙等[13]通过控制在最佳焙烧温度550℃制得N-TiO2催化剂,对紫外光照射下对20mg·L结晶紫的降解率高于纯TiO2。崔龙哲等[14]使用硫脲为原料,在以甲醇为电子供体的光还原反应体系中,控制反应条件为S掺杂量为7%(摩尔分数)、煅烧温度为250℃时采用溶胶凝胶低温煅烧法制备得到的S/N-TiO2,在15A全波段光照条件下反应150min,对溶液中Cr(Ⅵ)离子的催化还原效果几乎达到100%。
3.1.3 金属与非金属共掺
某些金属离子和非金属离子共掺可能会同时增加活性位点和提高可见光范围的吸收。杜聪聪等[15]通过溶胶凝胶法以及降解实验得到了Mn-N-TiO2制备过程中的最佳配比,即硝酸锰、尿素、无水乙醇和冰醋酸与钛酸四丁酯的物质的量比值为0.0006、0.24、10、6,焙烧温度为400℃,此时制得的Mn-N-TiO2对甲基橙溶液(60mg·L-1)达到了92%的降解率,并且高于单掺和不掺。杨茂楠等[16]用不同金属离子和N离子共掺TiO2,通过对结晶紫的降解实验测得ln、N共掺TiO2在紫外光照射下降解率达到80%,高于N离子单掺和不掺,并且降解速率符合准一级动力学。但也发现一些离子掺杂效果并不理想,Mn、N共掺和Ce、N共掺的降解性能低于纯TiO2,考虑原因是Mn和Ce充当电子陷阱捕获电子,加快电子-空穴对的复合。周志超等[17]通过溶胶凝胶法制备的Zn-N-TiO2光催化性能低于纯TiO2,经过扫描电镜分析发现,原因可能是共掺使其尺寸变大,禁带宽度减小,氧化还原电位降低,电子空穴对产率和光催化速率随之降低。
元素掺杂也有目前不可避免的缺点,例如金属元素会破坏TiO2的热稳定性以及在饮用水处理中不得不考虑金属渗出的毒性;非金属元素会影响TiO2的化学稳定性。虽然存在一些缺点,但是目前多种元素共掺改性,利用多种元素之间的协同作用,克服了单一元素掺杂的部分缺点,受到了越来越多的关注。另外,离子掺杂种类也具有很大的发展前景。
3.2 贵金属沉积改性
贵金属的费米能级低于TiO2,在TiO2和贵金属表面会形成肖特基势垒,贵金属原子簇吸引光生电子,肖特基势垒阻挡电子跨越,将电子和空穴分别定域在贵金属和半导体上,从而达到电子-空穴对分离的目的。郑苗苗[18]用溶胶凝胶法和水热法制备TiO2的Ag-TiO2附着于棉织物表面,对大肠杆菌和金黄色葡萄球菌的抑菌率分别为94.8%、93.1%,远远高于无附着和单一TiO2附着,经过25次洗涤后对大肠杆菌和金黄色葡萄球菌的抑菌率分别为87.2%和86.4%,体现了其优异的光催化能力和可重复使用性。付勇等[19]通过溶胶凝胶法制得的Ag-TiO2/AC相较于TiO2/AC在可见光照射下对10、20 mg·L-1的亚甲基蓝溶液和10 mg·L-1的Cr(Ⅵ)溶液的降解率分别提高了14%、47%、137%,并且测得Ag掺杂增强了材料对污染物的吸附性。对比于普通金属,贵金属的导电能力更强,但是由于贵金属的成本较高,导致目前贵金属在TiO2改性领域应用受到限制。
3.3 构建异质结
异质结是由两层及以上不同的半导体材料构成,分为同型异质结(P-p或N-n结)或异型异质结(P-N结),P型半导体空穴浓度较高,N型半导体自由电子浓度较高。在浓度差作用下,P型半导体中空穴向N型半导体扩散,而N型半导体中自由电子向P型半导体扩散。当浓度达到动态平衡时,P-N结形成[20]。异质结的构建不仅可以有效提高TiO2的可见光吸收范围,并能够促进光生电子-空穴的分离,这归因于半导体能级不同。许雅如等[21]制备了TiO2/MnS、TiO2/CdS、TiO2/ZnS和TiO2/CuS异质结,通过太阳光照射25min对甲基橙的降解实验发现TiO2/CuS异质结(TiO2与CuS物质的量比3∶1)的降解效率达到97.3%。卢召娣等[22]研究发现WO3/TiO2-SiO2比TiO2-SiO2光催化活性更高,并且得到实验条件的最佳配比为n(W)∶n(Ti)=1.5∶1时制得的WO3/TiO2-SiO2光催化能力达到最佳,40 min光照对亚甲基蓝的降解率可达99%。张娜娜等[23]制备得到微米结构g-C3N4/TiO2,根据UV-Vis图谱发现吸收边缘带提高到440nm,禁带宽度下降到2.83eV,吸收边带发生明显红移,对可见光产生更大响应。
3.4 染料敏化
染料敏化指将与TiO2能带相匹配的染料吸附到TiO2表面,受太阳光照射由基态跃迁到激发态,当染料激发态电势比半导体导带电势更负时,可以将光生电子传输到TiO2导带,对可见光产生强吸收作用,将TiO2的响应范围延伸到可见光区域。温玉鑫等[24]制备rGO质量分数为20%的D-TiO2/rGO,控制实验条件即温度为40℃、溶液pH为7、光源距离为10 cm时对亚甲基蓝的去除率可达97.67%,5次循环实验仍能对亚甲基蓝保持90%以上的去除率,证明了其具有良好的可重复利用性。
文献中此技术较多应用于太阳能电池,构成染料敏化太阳能电池(DSC),类似于植物光合作用,以TiO2和染料为主要原料,激发到TiO2导带上的通过外电路传输到对电极,电解质还原被氧化的染料敏化剂分子,而电解质中的氧化部分传输到对电极发生还原,至此完成循环。DSC相较于传统的太阳能电池具有使用寿命长、生产成本低和使用范围广等优点。石明吉等[25]将制备好的TiO2纳米管阵列薄膜应用于DSSC光阳极中,发现随着阳极氧化电压的升高,锐钛矿(101)晶面特征衍射峰逐渐增强,降低了开路电压(Voc),增大了TiO2的表面积,短路电流(Isc)和填充因子(FF)增大,光电转换效率提高。目前对染料的研究多为天然植物染料和化工合成染料,另外应更多研究较大的最大激发波长的光敏化剂。
4 结束语
TiO2作为目前研究最多的光催化剂,针对其目前存在的一些问题,总结了离子掺杂、贵金属沉积和构建异质结等改性方法,有效地提高了TiO2的光催化效率。但是,TiO2在大规模生产和应用方面仍然较少,研究更为低廉、简单的改性方法仍然是一种趋势。同时,单一的改性方法提高的效果较为有限,今后应更深入研究各种改性方法的机理,将多种改性方法有效结合,充分利用太阳能资源,更好地提高TiO2可见光响应范围及更有效抑制电子-空穴对的复合率。
参考文献:
[1] 孙若阳,赵显一. 二氧化钛光催化剂的制备及应用进展[J]. 当代化工,2023,52(1):202-208.
[2] LIANG H C, LI X Z. Visible-induced photocatalytic reactivity of polymer-sensitized titania nanotube films[J].Applied Catalysis B:Environmental, 2009, 86(1-2): 8-17.
[3] 刘壮壮. 阴离子改性二氧化钛的制备及光催化性能研究[D]. 长春: 长春工业大学,2022.
[4] 刘峰强,王黎明,徐丽慧,等.锐钛矿相二氧化钛纳米棒的制备及其光催化性能研究[J].化工新型材料,2023,51(7):282-285.
[5] WANG H, ZHANG L, CHEN Z, et al. Semiconductor heterojunction photocatalysts: design, construction, and photocatalytic performances[J].Chem Soc Rev, 2014, 43(15): 5234-5244.
[[6]]史弘宇,李桂镇,李建敏,等.银掺杂二氧化钛光催化降解亚甲基蓝性能研究[J].云南民族大学学报(自然科学版),2024,33(3): 314-319.
[7] 张毛进,常薇,王红红,等. Fe掺杂改性介孔TiO2的制备及表征[J]. 纺织高校基础科学学报,2017,30(4):535-540.
[8] 马涛,王军丽. 改性纳米TiO2的制备及光催化降解重金属废水的研究[J]. 功能材料,2022,53(11):11126-11130.
[9] 郭文轩,陈文刚,郝星星,等. 纳米二氧化钛的光催化与减摩性能研究进展[J]. 润滑与密封,2023,48(2):172-181.
[10] 付雅君,韩彬,张宁,等. 纳米TiO2的制备及其稀土元素掺杂的光催化性能研究进展[J]. 沈阳师范大学学报(自然科学版), 2022, 40(5):392-397.
[11] 陈恩伟,银董红,宋慧娟,等. 镧系离子掺杂TiO2的制备及其对咪唑降解反应的光催化活性[J]. 催化学报,2006,27(4):344-348.
[12] VIET N M, MAI HUONG N T, THU HOAI P T. Enhanced photocatalytic decomposition of phenol in wastewater by using La-TiO2nanocomposite[J].Chemosphere, 2023, 313: 137605.
[13] 陆成龙,胡开文,王琼,等. N掺杂对TiO2光催化剂性能的影响[J]. 湖北理工学院学报,2022,38(5):36-40.
[14] 崔龙哲,文景琳,林晓宇,等. 硫氮掺杂TiO2的制备及其在可见光下对Cr(Ⅵ)的催化还原[J]. 武汉纺织大学学报,2021,34(3):30-36.
[15] 杜聪聪,李石,李萌. Mn-N/TiO2光催化剂的制备及甲基橙的降解[J]. 化工环保,2015,35(6):625-629.
[16] 杨茂楠,李莉,杨长龙,等. 金属与N元素共掺杂TiO2复合材料光催化结晶紫[J]. 广州化学,2021,46(2):34-38.
[17] 周志超,段学臣,朱奕漪,等. 溶胶凝胶法制备掺杂纳米TiO2粉末及其光催化性能[J]. 粉末冶金材料科学与工程,2013,18(3): 434-440.
[18] 郑苗苗.Ag-TiO2整理棉织物的抗紫外和抑菌性能[J]. 印染助剂, 2021,38(5):43-46.
[19] 付勇,徐文奇,赵强,等. 银掺杂二氧化钛/活性炭复合材料的制备及其光催化性能研究[J]. 无机盐工业,2022,54(2):117-122.
[20] 薛延,许娜,谈立伟,等. 基于TiO2异质结在光电化学传感领域的应用[J]. 盐城工学院学报(自然科学版), 2014, 27(2):73-78.
[21] 许雅如,江禹燕,陈星仪,等. TiO2/CuS异质结的制备及光催化降解染料废水的研究[J]. 中国无机分析化学,2021,11(5):31-35.
[22] 卢召娣,任龙霞,何静. WO3/TiO2-SiO2粉体结构和光催化性能研究[J]. 山东理工大学学报(自然科学版),2022,36(5):56-59.
[23] 张娜娜,金开锋,周志坚,等. g-C3N4/TiO2异质结光催化材料的制备及性能研究[J]. 新技术新工艺,2022(1):67-71.
[24] 温玉鑫,鲍利红,凌嘉雯. 染料敏化二氧化钛/石墨烯复合材料的光催化性能[J]. 印染,2021,47(12):7-12.
[25] 石明吉,刘斌,王建,等. TiO2纳米管的制备及其在染料敏化太阳能电池中的应用[J]. 南阳理工学院学报,2016,8(6):72-75.
