SDBS优化改性沸石去除微污染水中氨氮试验实验研究
2024-09-20刘禹铮杨辉董美玲




摘 要: 为了提高沸石对于微污染水中氨氮的去除能力,研究不同改性剂对于沸石的改性效果,并选取最佳的改性剂,对沸石进行优化改性,探讨沸石粒径、改性剂浓度以及改性时间对沸石去除氨氮的影响。结果表明,十二烷基苯磺酸钠(SDBS)对于沸石的改性效果最佳,十六烷基三甲基溴化铵(HDTMA)改性后的沸石对氨氮的无明显作用。在优化改性试验实验中,沸石粒径对于沸石吸附氨氮影响最大。粒径为1-~2mm的沸石,采用30g·L-1/L的SDBS溶液改性10h后,可获得最佳的改性沸石。反应后的沸石用1mol·L-1/L的氢氧化钠和氯化钠溶液进行解吸并再生,经3次解吸和再生后,沸石的再生率为86.3%。也针对不同温度、pH、沸石投加量等分析单因素的变化对氨氮去除效果的影响。
关 键 词:氨氮; 沸石; 优化改性; 再生
中图分类号:TU991.21文献标志码: A 文章编号: 1004-0935(2024)08-12100009-0×4
在地表水体中,氮元素是生物新陈代谢所需的营养物和产物,是天然存在的,但是由于社会的快速发展和人类活动的影响,导致含氮有机物进入水体中,在微生物的作用下,水体中氨氮浓度上升。氨氮的污染,存在季节污染的规律[1],北方因其极寒冷冻天气,冬日水中微生物对营养物的利用较低,会导致氮含量上升;夏季因水表和水底的较大温差,使得水库存在翻水的现象,从而造成氮含量的升高。针对低温条件下的氨氮污染的北方水源水[2],研究合理的处理工艺,对水源水进行处理,保证饮用水安全是很有必要的。
目前针对水中氨氮的处理技术较多,主要有吹脱法[3]、电化学法、生物法、膜分离法、折点氯化法、生物法、吸附法[4]等,相较于其他去除方法,通过改性的方法提高沸石对于氨氮的吸附效果更加的经济和环保[5,-6],本文通过研究不同溶液对于沸石的改性效果,综合选取最合适的改性溶液,通过正交实验考察不同改性条件对于沸石改性效果的影响。并研究在pH、温度等外界影响下,改性后的沸石去除氨氮的性能,最终分析研究解决沸石的再生问题。
1.实验部分方法与材料
1.1试验实验原水
以东北地表水污染现状为依据,试验实验以氯化铵与蒸馏水配置成质量浓度为5mg·L-1/L的氨氮原水,原水中仅氨氮超过我国《生活饮用水卫生标准》(GB5749—2022),水中无其他影响污染物。
1.2试验实验材料与分析方法
天然沸石:化学式Na2O·Al2O3·xSiO2·yH2O,是一种天然、无毒、无味,且对环境没有影响的离子交换剂,是呈骨架状结构的多孔性铝硅酸盐晶体,试验实验使用的沸石粒径为2-~4mm。
主要药品和试剂:氯化铵(NH4Cl)、氢氧化钠(NaOH)、十二烷基苯磺酸钠(C18H29NaO3S)、十二烷基磺酸钠(C12H25SO3Na)、三聚磷酸钠(Na5P3O10)、十六烷基三甲基溴化胺(C19H42BrN)、酒石酸钾钠(C4H4O6KNa··4H2O)、碘化汞(HgI2)、碘化钾(KI2),均为分析纯。
试验实验方法:将NH4Cl晶体配制成5mg·L-1/L的储备液,在常温下密闭避光存放于棕色瓶中,配置酒石酸钾钠溶液和纳氏试剂作为显色剂。试验实验时,称取1g的改性沸石,放入装有50mL氨氮溶液的锥形瓶中(氨氮质量浓度为5mg·L-1/L);静置24h小时,定时测量溶液中氨氮的含量,测量时取一定量的上清液,按需稀释并依次加入酒石酸钾钠溶液和纳氏试剂并静置10min后,测定溶液中剩余的氨氮含量。氨氮的测定采用纳氏试剂分光度法测定[7]。
试验实验仪器:SHA-BA水浴恒温振荡器、UV--1800PC型紫外可见分光光度计、PHB--4便携式pH计(上海雷磁)等。
1.3改性试验实验
本试验实验选用氢氧化钠、十二烷基苯磺酸钠(SDBS)、十二烷基磺酸钠(SLS)、十六烷基三甲基溴化胺(HDTMA)、壳聚糖、和三聚磷酸钠溶液分别作为碱、阴离子表面活性剂、络合剂改性剂,通过不同改性剂对沸石进行改性操作。分别配置1mol·/L-1氢氧化钠溶液、20g·L-1/L十二烷基苯磺酸钠溶液、12g·/L-1十二烷基磺酸钠溶液、16g·L-1/L三聚磷酸钠溶液、20g·L-1/L十六烷基三甲基溴化铵溶液。取20g天然沸石放到200mL锥形瓶中,向锥形瓶各加入100mL上述改性溶液,将锥形瓶置于恒温振震荡箱振震荡6h后,用蒸馏水将沸石冲洗干净后烘干备用。
1.4吸附试验实验
配置5mg·/L-1的氨氮溶液,取50mL置于150mL的锥形瓶中,向其中分别加入1g不同的改性沸石,静置24h小时,定时测定溶液中氨氮的含量,测定时过滤取一定量的上清液,在室温、pH值为7的条件下,检测改性沸石对氨氮的去除效果。
1.5优化改性试验实验
选取吸附实验中最佳的改性溶液进行优化改性试验实验,配置50mg·/L-1的氨氮溶液,试验实验时,取50mL置于150mL的锥形瓶中,根据正交试验实验的设计,分别投加不同类型和不同粒径的改性沸石1g于锥形瓶中。室温下,将锥形瓶在振荡器中(180r·/min-1)充分反应6h后,滤出沸石,取上清液测定其中剩余的氨氮浓度,计算氨氮的去除率和沸石的吸附容量。所有试验实验均重复两次取平均值,以减小试验实验误差。
1.6沸石再生试验实验
沸石吸附饱和后,其吸附能力和交换性能随之消失,因此次需要进行沸石的解吸再生实验,沸石的再生方法有物理再生法、化学再生法、电化学再生法、生物再生法等。本文采用化学再生法进行沸石再生,化学再生方法一般采用KCl、NaCl、HCl或NaOH溶液两两组合或采用单一溶液对沸石进行浸泡,达到解吸再生的目的,本试验实验分别将1mol·/L-1NaOH溶液、1mol·/L-1V(NaOH)+∶V(NaCl)(v1:v2=1:∶1)溶液作为再生液,将饱和沸石与再生液1g:∶20mL放入锥形瓶,置于25℃、150r·/min-1振荡器中充分反映应5h后,将沸石滤出,取解吸液的上清液,测定其中的氨氮总量,计算沸石的再生率。
2.结果与讨论
2.1改性效果分析
由图1可知,除HDTMA外,其余改性溶液都对沸石去除氨氮有促进作用,分析HDTMA改性效果差的原因是其使沸石表面带正电荷,与铵根离子相斥,影响氨氮的吸附。
由图1可知,除HDTMA外,其余改性溶液都对沸石去除氨氮有促进作用,分析HDTMA改性效果差的原因是其使沸石表面带正电荷,与铵根离子相斥,影响氨氮的吸附。SLS和SDBS对于沸石的改性效果优于氢氧化钠,其原因是钠离子起到促进离子交换作用,且其作为阴离子表面活性剂,使沸石表面带负电荷,增强对氨氮的吸附效果。但SDBS在价格方面比SLS低,故开展对于SDBS的优化改性试验实验。
2.2优化改性试验实验
为了探究改性的各种因素影响,采取正交试验实
验[8]进行分析,正交试验实验采用三因素三水平,三因素分别为沸石粒径、改性溶液浓度、改性时间,按L9(3^4)正交表安排试验实验,如表1所示。正交试验实验结果如表2所示。由表2可知第3组的改性沸石对氨氮的去除效果最好,其水平组合为A1B3C3,吸附容量为2.75mg·/g-1。
计算可知,三因素中,A(沸石目数)的极差为1.41,B(改性剂浓度)的极差是0.3,C(改性时间)的极差是0.2。由此可知,在本试验实验设定的因素水平下,沸石粒径对沸石改性的影响最大,改性剂浓度的影响稍弱,改性时间对改性效果的影响不明显。
2.3不同影响因素对去除氨氮的影响
2.3.1沸石投加量的影响
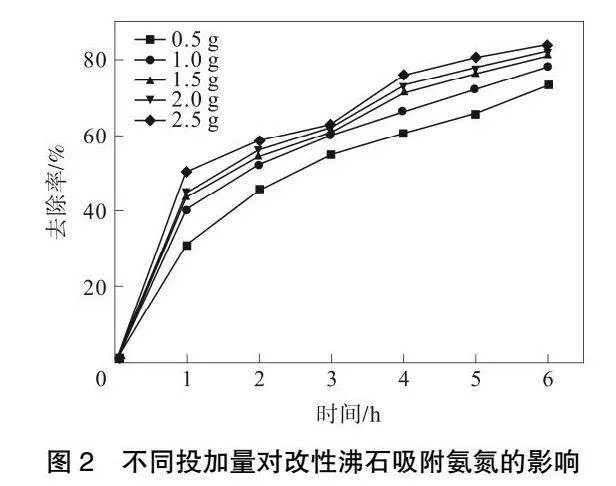
(配置5mg·L-1/L的氯化铵溶液,向150mL锥形瓶中加入50mL溶液,控制改性沸石投加量为0.5g、1.0g、1.5g、2.0g、2.5g。在室温、pH值为7的条件下,在恒温振荡器中振荡振荡器中震荡后,滤出沸石,测定上清液中氨氮的浓度,计算出去除率,如图2所示。
由图2可知,不管在何种投加量下,该改性沸石的氨氮去除率随时间推移而升高,对氨氮的吸附速度也随时间增长慢慢下降。增加投加量,在氨氮的去除前期,确实能够达到很好的效果,很明显,当投加量为2.5g时,仅仅需要1h,氨氮的去除率就能达到51%左右。但是投加量从1.5g开始往上,投加量的增加所带来的优势就渐渐减小。
2.3.2温度的影响
配置5mg·/L-1的氯化铵溶液,向150mL锥形瓶中加入50mL溶液,投加1g改性沸石,控制水温分别为15、20、25、30、35℃。pH值为7的条件下,在恒温振荡器中振震荡后,滤出沸石,测定上清液中氨氮的浓度,计算出去除率,如下图3所示:。
由图3可知,随着反应的进行,SDBS改性沸石对氨氮的去除率是随时间逐渐增加至平稳的,当反应进行到1h左右时,35℃条件下的改性沸石对氨氮去除率能达到55%左右,超出其余两个相对较低温度许多。
实际中,北方水厂的取水口水温,冬天在3~6℃,夏天最高温度能达到20℃左右[9-10],基于这样的温度条件,SDBS改性沸石能够达到很好的处理效果。
由图3可知,随着反应的进行,SDBS改性沸石对氨氮的去除率是随时间逐渐增加至平稳的,当反应进行到1h左右时,35℃条件下的改性沸石对氨氮去除率能达到55%左右,超出其余两个相对较低温度许多。
实际中,北方水厂的取水口水温,冬天在3~6℃,夏天最高温度能达到20℃左右[9,10],基于这样的温度条件,SDBS改性沸石能够达到很好的处理效
2.3.3 pH值的影响
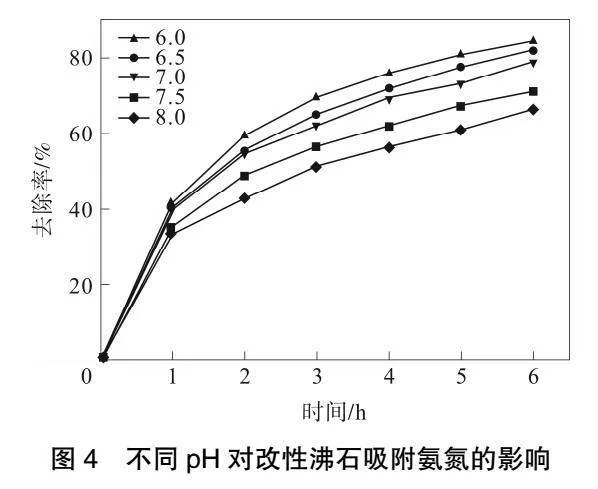
配置5mg·L-1/L的氯化铵溶液,向150mL锥形瓶中加入50mL溶液,投加1g改性沸石,原水pH值分别调至6.0、6.5、7.0、7.5和8.0。在室温条件下,在恒温振荡器中振荡振荡器中震荡4h小时后,滤出沸石,测定上清液中氨氮的浓度,计算出去除率,如下图4所示:
不管在何种pH值下,改性沸石的氨氮去除率都是随着反应时间的增加而增加的,在pH值为小于等于7的条件下,曲线较为接近;是因为在这个条件下具有大量铵根离子[11],由于改性沸石带负电,在电荷作用下,大量的铵根离子被吸引到其表面,所以,氨氮的浓度在一开始下降得很快,然后铵根离子进入改性沸石的孔道中进行离子交换,二者结合,完成这一高效率的吸附过程[12];而随着pH值的升高,水中的铵根离子减少,游离氨增多,此时改性沸石对游离氨的吸附主要是以弱于电荷作用的分子间作用力为主,因此在pH值为7.5和8.0的条件下,改性沸石的吸附效率反而下降。
2.4沸石的再生
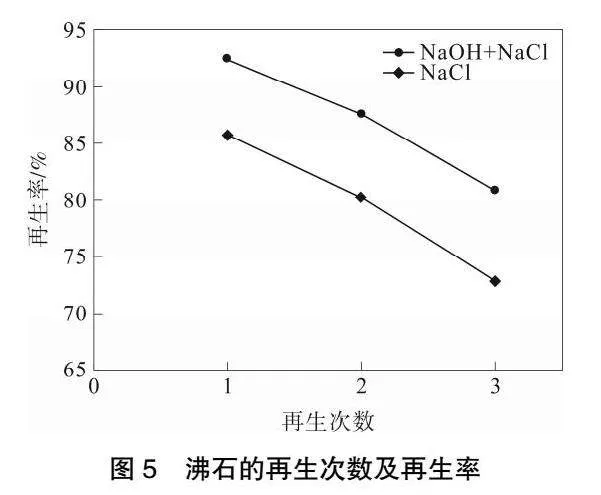
沸石吸附饱和后,其吸附能力和交换性能随之消失,因此需要进行沸石的解吸再生实验,沸石的再生方法有物理再生法[13]、化学再生法[14]、电化学再生法[15]、生物再生法等。本试验实验分别研究氯化钠和氯化钠+氢氧化钠溶液再生法对于沸石的再生效果。
由图5可知,再生沸石的吸附容量和解吸率都随着解吸回用次数的增加逐渐降低。原沸石经过3次解吸后,解吸率仍高达86.3%,选择钠离子溶液对饱和吸附沸石进行逆向吸附,可还原沸石结构,使之再生并通过钠离子的补充增加对氨氮的交换能力。经过多次反复交换,沸石骨架结构会受到一定程度的破坏,其再生效果会逐渐降低。
4 3结 论
(1)通过改性试验实验可知,阴离子表面活性剂SDBS与SLS对于沸石进行改性后,提高了沸石对于氨氮的去除效果。
(2)通过正交试验实验可知,改性沸石对氨氮的去除效果主要受沸石粒径的影响,粒径越小,沸石的比表面积越大,改性后对于氨氮的吸附效果越好。
(3)通过对SDBS改性沸石去除氨氮影响因素的研究,得出温度为35℃时,对氨氮的去除效果最好可达到82.39%;pH值为6.0时,对氨氮的去除率最高为84.44%。
(4)Wy7Yunimrw7yvf0DLYS0QjZNK15E1wGpgqFCT+XMh5Q=对吸附饱和的沸石进行解吸并再生回用,采用NaOH+NaCl溶液再生沸石,经过三次的解吸与回用后,再生率仍有86.3%,再生和吸附能力保持良好。
参考文献:
[1] 袁犇.葠窝水库内源污染研究[D].沈阳:辽宁大学,2019.
[2] 李晓波.北方微污染水源水中氨氮的预处理去除技术研究[D].哈尔滨:哈尔滨工业大学,2021
[3] 宗刚, 杨凯. 资源化回收废水中氨氮的研究进展[J]. 应用化工, 2016, 45(12):2336-2338.
[4] 汤云姣, 陈琳, 郭颖慧. 活性炭-人工沸石复合材料的吸附性能研究[J]. 四川化工, 2017, 20(6):4-8.
[5] 姚睿. 改性沸石的制备及对水源水中氨氮的去除效能研究[D]. 哈尔滨: 哈尔滨工业大学,2021.
[6] 陈玉波.基于沸石复合改性优化技术的水库供水水质净化试验实验[J].水利技术监督,2022,(07).
[7] 刘大志, 李艳会. 水中氨氮测定过程中若干问题分析[J]. 环境保护与循环经济, 2018, 38(6):67-69.
[8] 何钰莹, 杨舸, 张丹一, 等. 沸石的优化改性及其对水中氨氮去除性能[J]. 净水技术, 2019, 38(4): 59-64.
[9] 郜玉楠, 李懋锋, 包顺宇, 等. 壳聚糖改性沸石分子筛对氨氮的动态吸附研究[J]. 沈阳建筑大学学报(自然科学版), 2021, 37(1): 187-192.
[10] 王朦,谢宏华,姚淑霞,等.斜发沸石对微污染浅层地下水氨氮的吸附特性研究[J].科技通报,2020,36(06):20-23.
[11] 左思敏,荆肇乾,陶梦妮,等.天然沸石和改性沸石在废水处理中的应用研究[J].应用化工,2019,48(05):1136-1139+1145.
[12] 刘丽芳,林子厚,杨克敏,等.改性沸石滤料吸附氨氮性能研究[J].给水排水,2022,58(S1):679-686.
[13] 陈静.沸石吸附—再生处理低温低浓度氨氮废水研究[D].广州:华南理工大学,2020.
[14] 张帅,叶芳芳,李长刚,等.饱和吸附氨氮沸石的化学再生方法研究[J].工业水处理,2019,39(08):73-76.
[15] 杨云,宋梦然,于萍,等.人造沸石对氨氮废水的吸附及其电化学再生研究[J].工业水处理,2017,37(10):65-68.
