例举数形结合的几种类型
2024-06-30伍阔伦
伍阔伦
数形结合不仅考查学生对基本的化学概念、原理的理解,同时还考查了学生的证据推理及分析解决问题的能力。通常考查图像与变化的对应关系,初中化学常见的类型有:溶解度曲线、金属与酸反应的曲线、金属与盐溶液反应的曲线、酸碱中和反应溶液pH变化曲线等。
一、构建溶解度曲线
溶解度曲线是表示物质溶解度随温度的变化而变化的曲线。随温度的升高:少数固体物质的溶解度变化不大,如:氯化钠;绝大多数固体物质的溶解度变大,如:硝酸钾;极少数估计物质的溶解度变小,如:氢氧化钙。
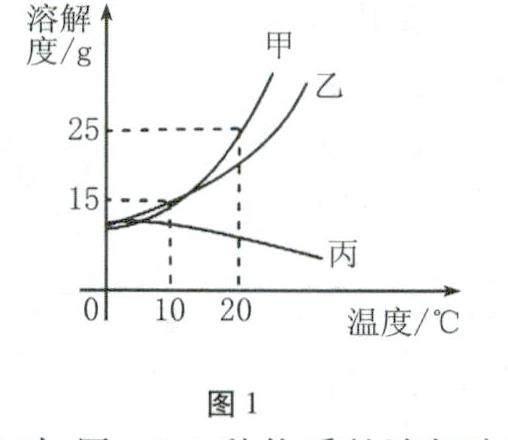
例题1 (2023年娄底)如图1是甲、乙、丙3种固体物质在水中的溶解度曲线。下列说法正确的是( )。
A.20℃时,甲、乙2种物质的溶解度相同
B.可用降温结晶的方法将丙从它的饱和溶液中结晶出来
C.20℃时,将12.5g乙物质溶于50g水中,充分溶解后溶质的质量分数小于20%
D.10℃时,将乙、丙2种饱和溶液升温到20℃,此时2种溶液都变成了不饱和溶液
解析 A项由溶解度曲线可知:10℃时,甲、乙2种物质的溶解度相同,A错;B项丙的溶解度随温度升高而减小,所以可用蒸发结晶的方法将丙从它的饱和溶液中结晶出来,B错;C项20℃时,乙的溶解度小于25g,所以12.5g乙物质溶于50g水中,不能全部溶解,已经达到饱和,溶解度是25g时,饱和溶液的溶质质量分数是20%,所以20℃时,将12.5g乙物质溶于50g水中,充分溶解后溶质的质量分数小于20%,C正确;D项10℃时,将乙、丙2种饱和溶液升温到20℃,乙溶解度变大,变为不饱和溶液,丙的溶解度变小,析出晶体,溶液仍然是饱和溶液,D错。故选C。
二、构建金属与酸反应的曲线
1.酸过量
总结:等质量的不同金属与足量酸反应,化合价相同时,生成氢气质量与相对原子质量成反比(“人小志气大”)。化合价不相同时,与价量比成正比。
2.金属过量
总结:等酸足金,生成氢气相等。
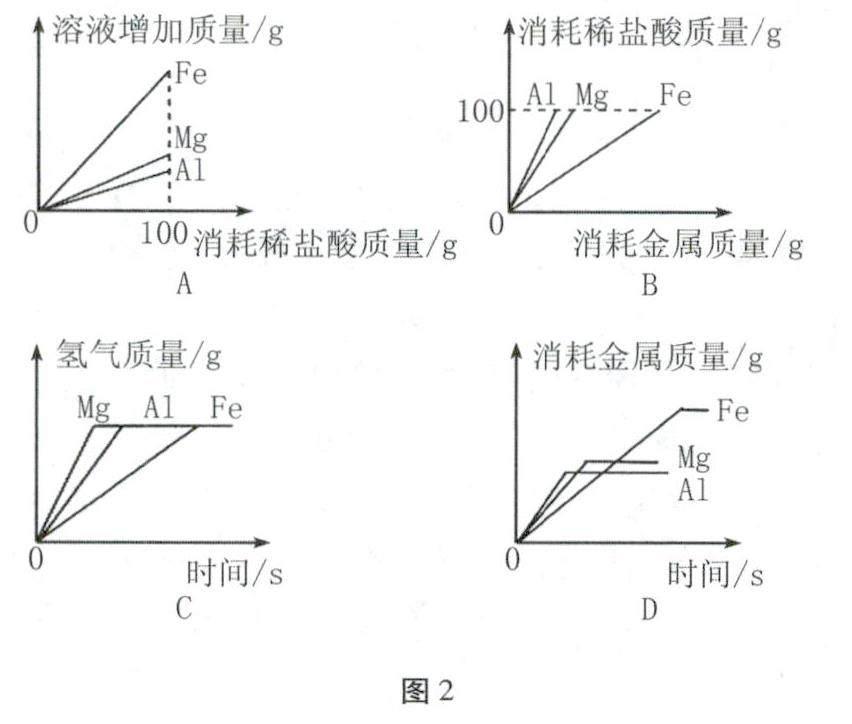
例题2 (2023年广西)向3个烧杯中分别放入足量的Mg、Al、Fe粉末,同时加入质量分数相同的100g稀盐酸,充分反应。如图2所示反应的有关图像错误的是( )。
解析 A项向3个烧杯中分别放入足量的Mg、Al、Fe粉末,同时加入质量分数相同的100g稀盐酸,若消耗盐酸相同,则生成氢气质量相同,根据化学方程式的质量关系可知消耗相同质量的盐酸,同时消耗金属的质量关系为Fe>Mg>Al,溶液质量增加关系为Fe>Mg>Al,选项图像正确。B项金属与酸反应时氢气来源于酸中的氢元素,因为酸的量相同,金属过量,最终生成的氢气应该相等,生成等质量的氢气,消耗的金属的质量为Fe>Mg>Al,选项图像正确。C项金属活动性为Mg>Al>Fe,则镁的反应速率最快,至完全反应所需时问短,铝的次之,最后是铁;向3个烧杯中分别放入足量的Mg、Al、Fe粉末,同时加入质量分数相同的100g稀盐酸,充分反应,最后生成的氢气的质量相等,选项图像正确。D项金属活动性为Mg>Al>Fe,所以相同时间消耗金属的质量关系为:Mg>Al>Fe,根据化学方程式的质量关系可知消耗相同质量的盐酸,同时消耗金属的质量关系为Fe>Mg>Al,选项图像错误。故选D。
三、构建金属与盐溶液反应的曲线
将金属加入2种盐的溶液中时,若金属与2种金属的盐均能发生置换反应,金属先与活动性更弱的金属的盐溶液反应。
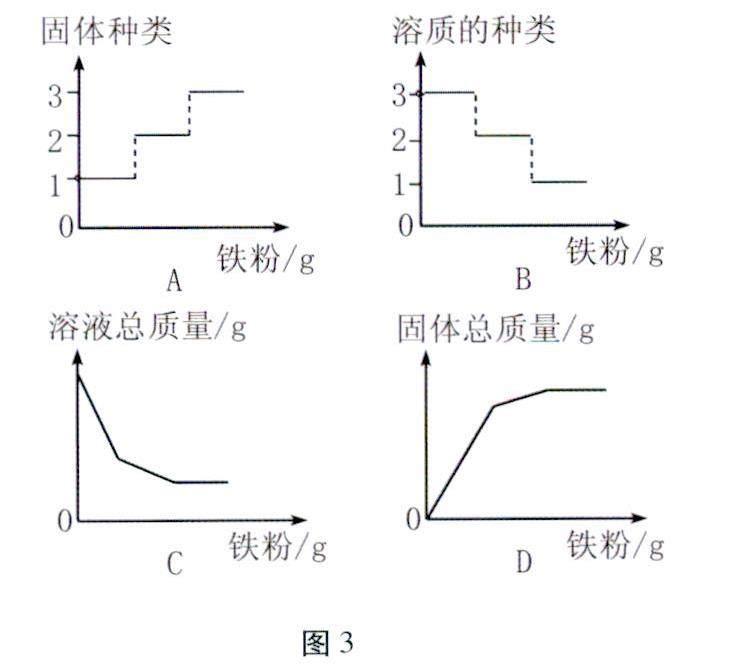
例题3 向装有一定量硝酸铜和硝酸银混合溶液的试管中,缓慢加入细铁粉,充分反应。图3所示试管中物质的变化关系图错误的是( )。
解析 A项向装有一定量硝酸铜和硝酸银混合溶液的试管中,慢慢将细铁粉加入,铁粉先和硝酸银反应生成硝酸亚铁和银,开始试管中只有银一种金属;硝酸银反应完后,铁粉再与硝酸铜反应生成硝酸亚铁和铜,这时试管中有银和铜2种金属;当硝酸铜也反应完之后,继续加入铁粉,没有物质反应,此时试管中有银、铜、铁3种金属。选项图像正确。B项一开始没有加入铁粉时,溶质只有硝酸银和硝酸铜2种,开始加入铁粉后,铁粉和硝酸银反应生成银和硝酸亚铁,溶质有硝酸银、硝酸铜和生成的硝酸亚铁3种,随着硝酸银反应完,溶质有硝酸铜和硝酸亚铁2种,硝酸铜也反应完后,溶质只有硝酸亚铁,选项图像正确。C项铁、铜、银3种金属的相对原子质量由大到小的顺序是:银>铜>铁,一开始铁置换硝酸银中的银时,溶液总质量减小的快,硝酸银反应完后,铁置换硝酸铜中的铜时,溶液总质量减小的慢,完全反应后,溶液总质量小变,选项图像正确。D项铁、铜、银三种金属的相对原子质量由大到小的顺序是:银>铜>铁,一开始铁置换硝酸银中的银时,固体总质量增加的快,硝酸银反应完后,铁置换硝酸铜中的铜时,同体总质量增加的慢,完全反应后,随着铁粉的不断加入,固体总质量不断增大,选项图像错误。故选D。
四、构建酸碱中和反应溶液pH变化曲线
在酸碱中和反应中,若在碱溶液中滴入酸溶液其酸碱度呈现的变化分别为pH>7,pH=7,pH<7;若在酸溶液中滴入碱溶液其酸碱度呈现的变化分别为pH<7,pH=7,pH>7。
例题4 向含有酚酞的氢氧化钠溶液中慢慢滴入稀硫酸,该过程中溶液pH的变化如图4所示。下列分析正确的是( )。
A.P点时的溶液呈碱性
B.N点时的溶液呈红色
C.N→P过程中溶液的酸性逐渐增强
D.M→P过程中生成的硫酸钠不断增加
解析 A项P点时溶液的pH小于7,溶液显酸性,选项说法错误。B项Ⅳ点时溶液的pH等于7,N点时的溶液呈无色,选项说法错误。C项N→P过程中溶液的pH从等于7逐渐减小,则N→P过程中溶液的酸性逐渐增强,选项说法正确。D项M→P过程中,M→N,稀硫酸与氢氧化钠反应生成水和硫酸钠,硫酸钠的质量逐渐增加;N→P,正好完全反应后继续滴加稀硫酸,生成硫酸钠不变,选项说法错误。故选C。
(收稿日期:2024-02-10)
