例谈新情境下信息型氧化还原反应离子方程式的书写方法
2024-06-30甘春云
甘春云


一、解题方法
第一步,根据题干信息或流程图,判断氧化剂、还原剂、氧化产物、还原产物,按“氧化剂+还原剂——还原产物+氧化产物”写出初步的化学方程式。
注意:在高考中许多产物不明确给出,所以需要把常见的氧化剂和还原剂的产物记住。
第二步,先标出氧化剂、还原剂、氧化产物、还原产物中有变价元素的化合价,再标出升高和降低数。
第三步,根据得失电子守恒规律,用最小公倍数法把涉及化合价升高降低的氧化剂、还原剂、还原产物、氧化产物的相应化学计量数配上(一般先不要管氧原子和氢原子)。
第四步,根据电荷守恒,结合介质溶液的酸碱性,酸性添加H+、碱性添加OH-,使化学方程式两端的电荷守恒。
第五步,根据元素守恒,通过在反应式两端添加H2O(或其他小分子)使其两端的原子守恒,最后将“-”改成“=”。(一般化学方程式哪端缺氢原子,哪端就补水)
二、典例精析
例题1 我国生产的铜主要取自黄铜矿(CuFeS2),湿法炼铜工艺的核心是黄铜矿的浸出,目前主要有氧化浸出、生物浸出、配位浸出、电化学浸出等方法。
Ⅰ.氧化浸出
(1)在硫酸介质中用双氧水将黄铜矿氧化,测得有SO2-4生成。
①该反应的离子方程式为____。
②该反应在25-50℃下进行,实际生产中双氧水的消耗量要远远高于理论值,试分析其原因为____。
Ⅱ.生物浸出
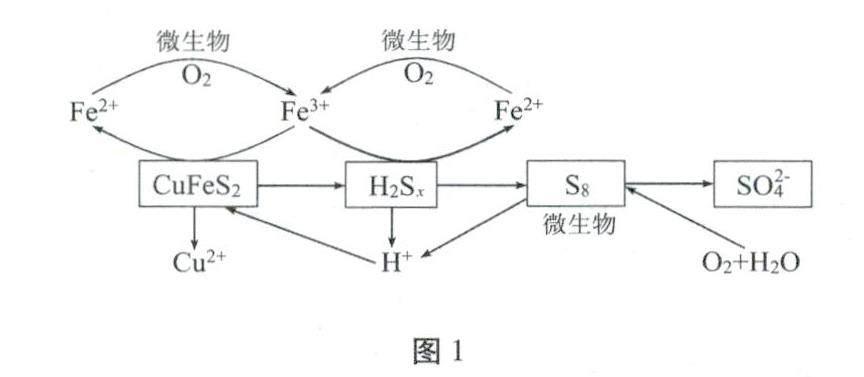
在反应釜中加入黄铜矿、硫酸铁、硫酸和微生物,并鼓入空气,黄铜矿逐渐溶解,反应釜中各物质的转化关系如图1所示。
(2)在微生物的作用下,可以循环使用的物质有____(填化学式),微生物参与反应的离子方程式为____(任写一个)。
(3)假如黄铜矿中的铁元素最终全部转化为Fe3+,当有96g SO2-生成时,理论上消耗O2的物质的量为____。
解析Ⅰ(1)①离子方程式书写步骤为:
第一步,根据题干信息,判断双氧水与黄铜矿发生反应的氧化剂、还原剂、氧化产物、还原产物,并写出初步的化学方程式。
