液相色谱串联质谱法测定鸡蛋中金刚乙胺残留量的研究
2024-06-23高兴运
高兴运
摘 要:目的:建立液相色谱串联质谱法测定鸡蛋中金刚乙胺残留量的分析方法,为鸡蛋食品安全检测工作提供技术支持。方法:采用液相色谱串联质谱法测定鸡蛋中金刚乙胺的残留量。结果:在质量浓度为1~
20 ng·mL-1,金刚乙胺的线性关系良好,相关系数为0.999 8,回收率为84.3%~91.6%,定量限为1 μg·kg-1。结论:该方法检测效果良好,可以应用于鸡蛋中金刚乙胺含量的实际监测工作中。
关键词:液相色谱串联质谱法;鸡蛋;基质效应;金刚乙胺
Study on the Determination of Residual Amantadine in Eggs by Liquid Chromatography Tandem Mass Spectrometry
GAO Xingyun
(Suixi County Market Supervision and Inspection Institute, Huaibei City, Anhui Province, Huaibei 235199, China)
Abstract: Objective: To establish an analytical method for the determination of rimantadine residue in eggs by liquid chromatography-tandem mass spectrometry, and to provide technical support for the detection of egg food safety. Method: The residue of rimantadine in eggs was determined by liquid chromatography-tandem mass spectrometry. Result: The linear relationship of rimantadine was good at the mass concentration of 1~20 ng·mL-1, the correlation coefficient was 0.999 8, the recovery was 84.3%~91.6%, and the limit of quantitation was 1 μg·kg-1. Conclusion: The method has good detection effect and can be applied to the actual monitoring of rimantadine content in eggs.
Keywords: liquid chromatography tandem mass spectrometry; eggs; matrix effect; diamond ethylamine
在母鸡养殖中,养殖企业为获取较高利润,存在投喂母鸡金刚乙胺的现象。若鸡蛋中金刚乙胺含量超标,会严重影响孕妇、老年人的身体健康。因此,确保鸡蛋的食用安全至关重要。鸡蛋作为人们日常生活中的常见食物,为确保鸡蛋的食用安全,应对其金刚乙胺残留含量进行有效测定。测定金刚乙胺残留量的方法有多种,包括气相色谱法、液相色谱法等,但二者皆具有灵敏度低、预处理烦琐等问题。而液相色谱串联质谱法不仅具有较高的灵敏度,还具有高选择与高通量的特点,可以广泛应用于农药残留、兽药残留等检测工作中。因此,在检测鸡蛋内金刚乙胺残留量时,可选择液相色谱串联质谱法进行测定,可获得较好的测定效果。基于此,本文建立液相色谱串联质谱法测定鸡蛋中金刚乙胺残留量的方法,旨在为鸡蛋食品安全检测工作提供技术支持。
1 材料与方法
1.1 材料、试剂与仪器设备
鸡蛋,采购于附近超市。
金刚乙胺、甲醇、甲酸、乙酸铵、正己烷、三氯乙酸、乙腈、美金刚D6标准品和纯净水等。
液质联用仪,美国沃特世公司;涡旋仪、N-EVAP氮吹仪,美国Organomation公司;高速冷冻离心机,平凡仪器仪表有限公司;电子天平,瑞士Mettler-Toledo企业;尼龙微孔滤膜,天津市津腾实验设备有限公司;固相萃取小柱,美国安捷伦科技公司。
1.2 标准溶液配制
(1)金刚乙胺标准中间液配制(100 ng·mL-1)。吸取金刚乙胺标准溶液(100 μg·mL-1)100 μL至
100 mL容量瓶中,用甲醇定容至刻度线,于-18 ℃的环境中避光保存。
(2)美金刚D6工作溶液(100 ng·mL-1)。量取100.0 μL美金刚D6标准溶液(100 μg·mL-1)于
100 mL容量瓶中,用甲醇定容至刻度线,于-18 ℃保存。
(3)金刚乙胺标准工作溶液。吸取0.1 mL、
0.2 mL、0.5 mL、1.0 mL和2.0 mL的金刚乙胺标准中间液于10 mL容量瓶中,并向其中加入0.20 mL美金刚D6工作溶液,用初始比例流动相定容至刻度线,配制成质量浓度分别为1 ng·mL-1、2 ng·mL-1、
5 ng·mL-1、10 ng·mL-1和20 ng·mL-1的金刚乙胺标准工作溶液[1]。
1.3 样品预处理
①利用四分法获取200 g鸡蛋,并将其粉碎至均匀,冷藏存放备用。②称取2.00 g样本于离心管中,加入100 μL美金刚D6工作溶液与10 mL 1%乙酸-乙腈混合液,涡旋处理30 s后,利用超声振荡器处理20 min。以8 000 r·min-1离心5 min,并将上清液提取至离心管内。再次添加10 mL 1%乙酸-乙腈混合液,进行重复操作,得到上清提取液。③将提取液放置于活化后的PCX柱中,分别用5 mL水与甲醇进行淋洗。倒出液体,并用真空泵抽干,再用6 mL 5%氨水甲醇溶液进行洗脱与收集。经45 ℃氮吹浓缩操作后,过0.22 μm滤膜,供仪器分析[2]。
1.4 色谱条件
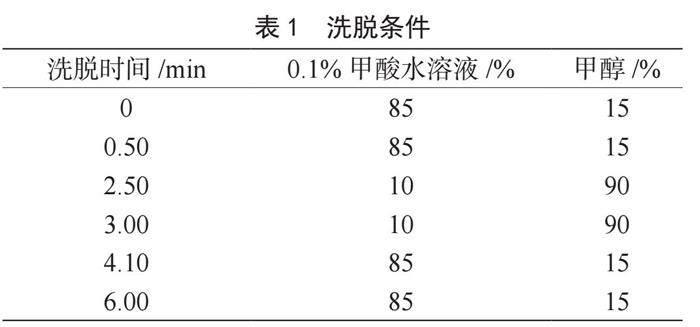
色谱柱柱温为40 ℃,流速为0.3 mL·min-1,样品体积为2.0 μL,流动相A为0.1%甲酸水溶液,流动相B为甲醇[3]。洗脱条件如表1所示。
1.5 质谱条件
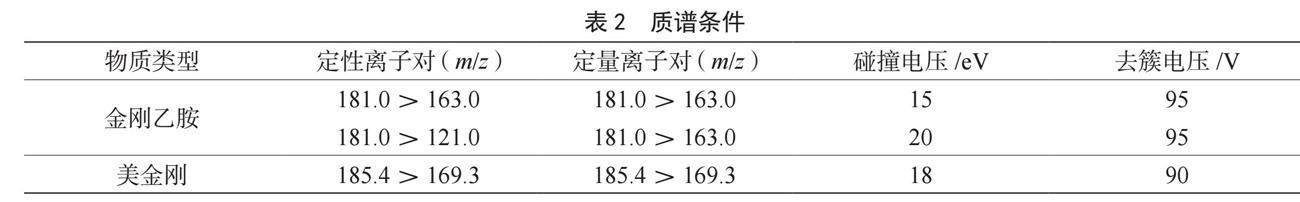
质谱采用电喷雾离子源进行正离子扫描,离子模式皆为多反应监测模式。雾化器压力为40 psi,毛细管的电压值为4.5 kV,干燥器温度为300 ℃,流速为11 L·min-1[4]。其他质谱条件如表2所示。
2 结果与分析
2.1 提取效果的对比
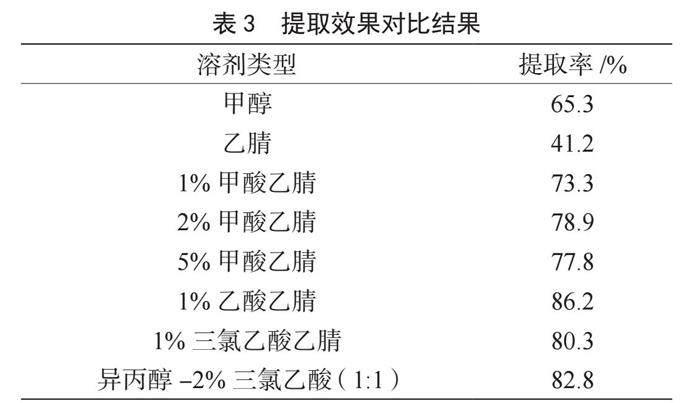
金刚乙胺内部含有极性氨基基团,能够溶于极性有机溶剂,在酸性条件下,便于对其进行解离提取。鸡蛋内部含有大量的蛋白质、磷脂等物质,通过乙腈的使用可以促进蛋白质沉淀,有效降低基质的影响,三氯乙酸也可以帮助蛋白质沉淀。以《出口动物组织中抗病毒类药物残留量的测定 液相色谱-质谱/质谱法》(SN/T 4253—2015)为依据,试验利用空白样品加标的方法比较8种溶剂[甲醇、乙腈、1%甲酸乙腈、2%甲酸乙腈、5%甲酸乙腈、1%乙酸乙腈、1%三氯乙酸乙腈、异丙醇-2%三氯乙酸(1∶1)]对金刚乙胺提取率的影响[5],加标浓度为10 μg·kg-1。由表3可知,1%乙酸乙腈的提取效果最好,提取率为86.2%。因此,试验将1%乙酸乙腈作为萃取液。
2.2 净化方式的对比
试验通过HLB柱、MCX柱、PCX柱、SCX柱、C18柱和PSA柱等方式进行净化,比较回收率结果。由表4可知,PCX柱的净化效果最好,回收率为81%。因此,将PCX柱作为净化柱。
2.3 色谱条件的对比
因金刚乙胺内部含有氨基,在流动相中加入一定量的酸可以通过离子化效应提升响应值。试验分别比较流动相为甲醇-0.1%甲酸水溶液、甲醇-1%甲酸水溶液、甲醇-水、乙腈-水、乙腈-0.1%甲酸水溶液和乙腈-1%甲酸水溶液时对10 ng·mL-1金刚乙胺的分离效果。结果表明,甲醇-0.1%甲酸水溶液的峰型与峰宽最好。因此,将甲醇-0.1%甲酸水溶液作为本试验的流动相。
此外,试验分别比较了柱温为25 ℃、30 ℃、35 ℃和40 ℃时对金刚乙胺出峰效果的影响。结果表明,柱温为40 ℃时,流动相的溶解度达到最大,且柱压下降。因此,柱温选择40 ℃。
2.4 标准曲线的建立
试验以目标物浓度为横坐标,以对应的峰面积为纵坐标,绘制标准曲线。结果表明,在质量浓度为1~20 ng·mL-1,金刚乙胺的线性方程为Y=1.091 053x-0.015 113,相关系数为0.999 8,信噪比(S/N)为19.437,定量限为1 μg·kg-1。
2.5 基质效应的处理
基质效应一般存在于残留物质分析过程中,会对残留物检测结果的精确性造成影响。鸡蛋样品在通过预处理工作后,仍会存在少量的磷脂、胆固醇等基本物质,会对待测物造成基质增强或基质抑制效应,从而导致金刚乙胺的检测结果出现偏离。基质效应ME=空白基质标曲斜率/(溶剂标曲斜率-1)×100%。当ME值大于0时,会形成基质增强效应。当ME值小于0时,会形成基质减弱效应。一般而言,弱基质效应的ME值为-20%~20%,此时的基质干扰程度比较低。中等程度的基质效应的ME值处于-50%~-20%或20%~50%。当ME值低于-50%或高于50%,则可以判断其为强基质效应,应采取相应措施来进行基质效应的补偿。通过对鸡蛋样品金刚乙胺的基质效应计算,其ME值为-21.80%,处于中等程度的基质效应。基于此,检测人员可通过同位素内标法加以解决,这是因为同位素与化合物性质相似,可提高测量结果的准确性[6]。美金刚D6是金刚乙胺的同位素,因此,实验可通过美金刚进行内标校正,进而有效降低基质效应,确保检测效果的真实有效。
2.6 回收率与精密度试验
在阴性鸡蛋样品中分别添加质量浓度为1 ng·mL-1、2 ng·mL-1和10 ng·mL-1的金刚乙胺标准工作溶液,平行测定6次,计算回收率以及精密度。由表5可知,金刚乙胺的回收率在84.3%~91.6%,相对标准偏差在3.3%~6.8%。
2.7 实际样品测定
为验证方法的可行性,在超市随机选择40批鸡蛋进行检测。结果表明,40批鸡蛋中均未检出金刚乙胺残留物。
3 结论
本文采用液相色谱串联质谱法测定鸡蛋中的金刚乙胺含量。结果表明,在1~20 ng·mL-1,金刚乙胺的线性关系良好,相关系数为0.999 8,回收率在84.3%~91.6%,定量限为1 μg·kg-1。该方法的检测效果良好,可有效检测鸡蛋中金刚乙胺的含量。
参考文献
[1]林柯璐,王玲,舒畅,等.超高相液相色谱串联质谱法分析鸡蛋中金刚乙胺含量残留[J].食品工业,2024,45(1):260-263.
[2]孙玲玲,霍江莲,陈冬东,等.液相色谱-串联质谱法同时测定鸡蛋中4种抗病毒药物残留[J].质量安全与检验检测,2023,33(5):6-13.
[3]欧阳思雨,蓝伟,贾佳,等.超高效液相色谱-串联质谱法同时测定鸡肉、鸡蛋中尼卡巴嗪、金刚烷胺、金刚乙胺残留量[J].现代食品,2022,28(23):138-141.
[4]张美,朱莉莎,徐飘飘,等.高效液相色谱-串联质谱法同时检测鸡蛋中金刚乙胺和金刚烷胺药物残留研究[J].中国家禽,2023,45(2):71-76.
[5]姜英杰,葛子欣,翟玮玮,等.EMR-Lipid固相萃取结合液相色谱串联质谱法快速测定鸡蛋中金刚烷胺和金刚乙胺残留量[J].中国食品添加剂,2022,33(11):
218-224.
[6]李巧莲,刘鑫,刘瀛,等.QuEChERS-液相色谱-串联质谱法测定鸡蛋中金刚烷胺和金刚乙胺残留量[J].现代食品,2022,28(20):185-190.
