清除胎盘后子宫重建术在胎盘植入患者中的临床应用价值研究
2024-05-12管华平游兴文
管华平 游兴文 杨 敏 唐 俐
河南省濮阳市油田总医院产科 457000
胎盘植入主要与剖宫产或其他子宫手术后的瘢痕子宫、前置胎盘、高龄妊娠等因素有关,常表现为反复无痛的阴道流血、子宫压痛、下腹痛等症状,目前胎盘植入已成为产科严重不良结局的重要原因。对于胎盘植入或合并剖宫产指征患者,临床通常建议行剖宫产术,若胎盘植入较深或面积较大,则建议行子宫切除术,但子宫切除后,患者需定期接受子宫颈细胞学检查,监测远期子宫颈残端癌的风险,且大部分患者有保留子宫的意愿,因此,研究安全有效的子宫保留手术方案具有重要临床价值。目前保留子宫的常见手术方案为胎盘原位保留+子宫动脉栓塞术,胎盘原位保留是指在胎盘植入患者经过剖宫产或阴道分娩终止妊娠时,将胎盘部分或全部保留,减少大出血风险,但仍有可能发生难以控制的晚期产后出血、严重感染、败血症等并发症[1-2]。对于胎盘植入患者,我院采取清除胎盘后子宫重建术,在保留患者子宫的同时,能避免胎盘原位保留的缺点,止血效果好,并发症少。基于此,本文就清除胎盘后子宫重建术在胎盘植入患者中的应用效果报道如下。
1 资料和方法
1.1 一般资料 回顾性分析2019年1月—2022年1月我院收治的80例胎盘植入患者临床资料,根据手术方式不同分为A组42例和B组38例。其中A组年龄21~38岁,平均年龄(30.26±3.45)岁;孕周33~38周,平均孕周(35.84±1.64)周;初产妇27例,经产妇15例;合并前置胎盘35例。B组年龄23~38岁,平均年龄(30.57±3.09)岁;孕周33~38周,平均孕周(35.68±1.62)周;初产妇22例,经产妇16例;合并前置胎盘32例。两组患者一般资料比较差异无统计学意义(P>0.05)。纳入标准:(1)彩色多普勒超声或磁共振成像检查提示胎盘植入高度疑诊者[3];(2)术中检查发现胎盘部分或完全未自行剥离;(3)术后病理学组织检查,发现绒毛侵入子宫肌层深处者;(4)患者有强烈的子宫保留意愿;(5)单胎妊娠。排除标准:(1)患有精神障碍或器质性病变者;(2)凝血功能异常或有严重心肺功能障碍,对手术无法耐受者;(3)多胎妊娠。
1.2 方法 A组患者采用清除胎盘后子宫重建术:(1)椎管内麻醉,患者取仰卧位,于患者下腹部正中做一纵切口,分离膀胱和子宫下段间粘连,下推膀胱至子宫颈内口以下,使子宫下段充分暴露。(2)术中探查,在取出胎儿时尽量避开以胎盘或者胎盘薄处为切口。(3)在胎儿娩出后,将子宫移动至腹腔外,并在宫颈内口水平以下使用血浆管捆扎,充分阻断子宫血流供给,血流阻断后,进行胎盘清除,切除无肌层子宫壁。(4)施行2-0可吸收线进行全层缝合,收拢肌层,重建结点呈渔网状排布,修复重建子宫下段,使子宫由葫芦状恢复为倒置梨形。(5)松开血浆管,对出血处或子宫壁膜薄弱处进行加固缝合,放置宫腔球囊,置引流管后关腹,术后静脉滴注卡贝缩宫素(南京星银药业集团有限公司,国药准字H20193159,1mL∶100μg×5支)100μg。B组患者采用胎盘原位保留后子宫动脉栓塞术:(1)椎管内麻醉后进腹,尽量避开胎盘取出胎儿,取出后尽量保留整个或部分胎盘,切除自然剥离部分,保留未剥离部分;(2)行子宫动脉栓塞术:使用穿刺针于股动脉处穿刺,置入4F动脉导管,应用数字减影成像技术,确定导管插入双侧子宫动脉后,注入100mg甲氨蝶呤(广东岭南制药有限公司,国药准字H20074238,5mg/瓶),使用吸收性明胶海绵进行子宫动脉栓塞。若两组患者在术中发现胎盘植入范围大,或术中出现大出血时,需及时进行子宫切除手术处理,术后予抗生素预防感染。
1.3 观察指标 (1)围术期指标:统计两组患者手术时间、住院时间、人绒毛膜促性腺激素(β-HCG)转阴时间、子宫保留率。β-HCG水平使用全自动发光免疫分析仪(江苏德朗电子设备有限公司)检测,β-HCG<5mU/mL为阴性。(2)术后并发症:观察两组患者术后产褥感染、膀胱损伤、晚期产后出血等并发症发生情况。(3)血清指标:分别于术前和术后1个月,于患者空腹状态下取静脉血3mL,经高速离心后留上清液待测,使用RPW-2103型多功能酶标仪(沃尔福实业有限公司)检测患者血清血管内皮生长因子(VEGF)、可溶性血管内皮生长因子受体-1(sFlt-1)水平变化。(4)妊娠情况:术后随访6个月,观察两组患者的妊娠情况。

2 结果
2.1 两组患者围术期指标比较 两组患者手术时间比较差异无统计学意义(P>0.05);A组患者子宫保留率高于B组,住院时间和β-HCG转阴时间均短于B组(P<0.05)。见表1。
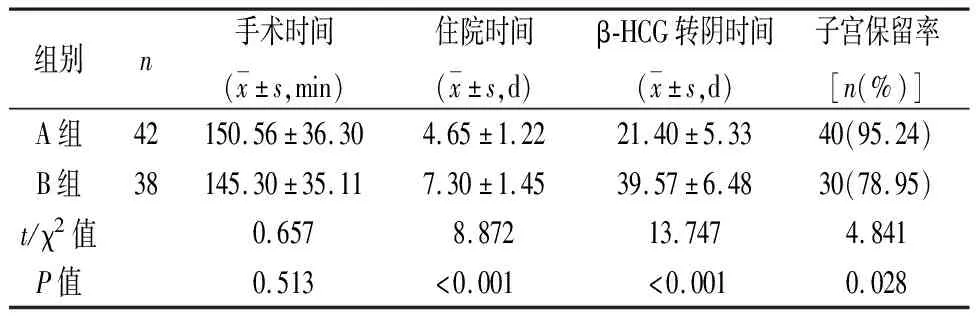
表1 两组患者围术期指标比较
2.2 两组患者术后并发症比较 A组患者术后并发症总发生率显著低于B组患者(P<0.05)。见表2。
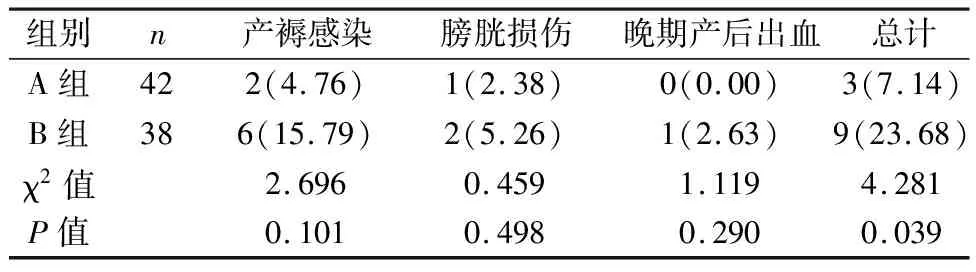
表2 两患者术后并发症比较[n(%)]
2.3 两组患者血清指标比较 术后1个月,两组患者血清VEGF水平升高,且A组高于B组(P<0.05);两组患者sFlt-1水平降低,且A组低于B组(P<0.05)。见表3。
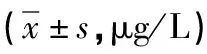
表3 两组患者血清VEGF、sFlt-1水平比较
2.4 两组患者再次妊娠情况比较 A组患者宫内妊娠2例(4.76%),B组患者宫内妊娠1例(2.63%),两组患者再次妊娠率比较差异无统计学意义(χ2=0.251,P=1.000)。
3 讨论
胎盘原位保留是现有保子宫治疗的手术策略之一,但胎盘在待吸收或排出期间,容易造成反复感染和产后出血,需要进行再次手术切除子宫或清除胎盘,容易对患者造成二次创伤。因此,如何在保留子宫的前提下,避免再次手术对患者造成的创伤仍是产科医生的研究重点。
清除胎盘后子宫重建术是将植入胎盘完全切除后,仅切除无肌层子宫壁,重塑薄弱肌层,促进子宫下段形态和厚度的恢复[4]。本文结果显示,A组患者子宫保留率为95.24%,显著高于B组的78.95%,且A组患者住院时间、β-HCG转阴时间短于B组,术后并发症总发生率低于B组,说明相较于胎盘原位保留后子宫动脉栓塞术,清除胎盘后子宫重建术能提高胎盘植入患者的子宫保留率,加快术后恢复时间,且术后并发症少。主要原因为以下几点:(1)控制术中出血量为保留子宫的前提,在切开子宫前,充分分离膀胱和子宫下段间粘连,在胎儿娩出后立即使用血浆管捆扎,使所有胎盘于捆扎水平以上,不仅能避免子宫下段直接下推膀胱,避免对膀胱造成损伤,还能充分阻断子宫血流循环,有效控制术中出血,保证视野清晰度,确保手术过程的安全性[5];(2)在血流阻断后,通过渔网状缝合,关闭血窦的同时还能使肌层相互牵制,从而增加子宫肌壁张力,再将胎盘植入累及的子宫壁和薄弱肌层进行修复和重建,在完全清除胎盘的同时,能恢复子宫肌壁张力,有利于后续宫腔填塞[6];(3)子宫动脉栓塞术是利用阻断子宫动脉血流供给,使植入性胎盘组织坏死、吸收或脱落,但在其吸收和脱落时间较长,容易引发产褥感染、晚期术后出血等并发症,严重者还会导致子宫坏死[7],因此采用清除胎盘手术能避免胎盘吸收和脱落时引发的并发症。
VEGF能结合血管内皮细胞上的受体,促进血管内皮细胞的增殖,从而促进胎盘新生血管的形成,因此,VEGF在胎盘发育过程占有重要地位;sFlt-1能阻断促血管生长因子(PIGF)和VEGF的生物学效应,抑制胎盘血管生长,导致血管内皮功能障碍,滋养细胞的增殖和浸润能力减弱,引起胎盘缺血、缺氧,而缺氧的胎盘组织又能释放sFlt-1,进一步抑制VEGF活性表达,因此,患者血清内sFlt-1水平升高,VEGF水平降低,则提示存在胎盘植入风险。本文结果显示,术后1个月,两组患者血清VEGF水平升高,sFlt-1水平降低,且A组患者血清VEGF、sFlt-1水平优于B组,提示清除胎盘后子宫重建术能显著改善患者血清VEGF、sFlt-1水平,可能与阻断子宫血流供应后,直接进行胎盘清除,避免胎盘残留有关,另外,术后随访6个月,两组患者再次妊娠率比较差异无统计学意义,但目前对于胎盘植入患者子宫保留后的生育功能尚有争议,且本文为回顾性研究,缺乏充足的样本量确定术后妊娠的安全性,后续需跟进研究。
综上所述,清除胎盘后子宫重建术对于有强烈保留子宫意愿的胎盘植入患者的子宫保留率高,能加快术后恢复、且并发症少,是一种安全有效的手术方案,但该手术需在医疗设备和资源充足的医院实施。
