慢性乙型肝炎患者接受核(苷)酸类似物抗病毒治疗后血清HBV-DNA的表达及临床意义
2024-05-11李慧
李慧
(河南省人民医院 检验科,河南 郑州 450000)
慢性乙型肝炎(chronic viral hepatitis B,CHB)为临床常见的肝脏感染性疾病,由乙型肝炎病毒(hepatitis B virus,HBV)持续感染6个月以上引起,如疾病早期未得到有效控制,病情持续进展可导致肝硬化、肝癌等严重后果[1]。积极的抗病毒治疗可抑制HBV病毒复制,减轻肝细胞坏死、变性和炎症反应,防止或控制肝脏纤维化,从而改善患者预后[2]。核(苷)酸类似物(nucleoside analogues and nucleotide analogues,NAs)是国内外指南一致推荐的抗病毒口服治疗方案,临床应用十分广泛[3]。但相关研究指出,部分CHB患者对NAs药物的反应不甚理想,需尽早调整治疗方案[4]。而由于NAs耐药检测费用高昂,临床急需客观指标对CHB患者NAs抗病毒治疗效果进行预测。Wang等[5]研究表明,血清乙型肝炎病毒脱氧核糖核酸(HBV deoxyribonucleic acid,HBV-DNA)与导致HBV持续感染的共价闭合环状DNA(covalently closed circular DNA,cccDNA)呈正相关关系,但其在评估抗病毒治疗血清学应答方面的价值还需进一步明确。基于此,本研究旨在观察血清HBV-DNA水平在CHB患者NAs抗病毒治疗过程中的变化,并探讨其对血清学应答的预测价值,以期为临床早期调整治疗方案提供依据。
1 资料与方法
1.1 一般资料
回顾性分析2021年1月至2022年10月河南省人民医院83例采用NAs抗病毒治疗的CHB患者临床资料,其中男53例,女30例;年龄25~68岁,平均(44.16±11.60)岁。纳入标准:符合《慢性乙型肝炎防治指南(2019年版)》[6]中相关诊断标准;乙型肝炎病毒e抗原(hepatitis B e antigen,HBeAg)阳性;首次接受抗病毒治疗,完成相关治疗;年龄≥18岁;就诊资料、治疗资料等保存完整。排除标准:合并肝硬化、脂肪性肝病、自身免疫性肝病、药物性肝病等其他肝病;合并其他慢性病毒感染;合并严重心、脑、肺、肾等器官功能障碍;近半年使用过免疫抑制剂;合并恶性肿瘤。
1.2 基线资料
收集患者NAs抗病毒治疗前的基线资料,包括年龄、性别(男、女)、体重指数、家族史(有、无)、吸烟史(有、无)、饮酒史(有、无)、基础疾病(高血压、糖尿病)。收集患者NAs抗病毒治疗前的实验室检测指标,检测方法如下:采集患者空腹静脉血5 mL,以3 000 r·min-1离心10 min,取上清液,根据电化学发光法测定乙型肝炎病毒表面抗原(hapatitis B surface antigen,HBsAg)、HBeAg水平,试剂盒厂家为罗氏诊断产品(上海)有限公司;根据丙氨酸底物法测定谷丙转氨酶(glutamic-pyruvic transaminase,GPT)水平,根据天门冬氨酸底物法测定谷草转氨酶(glutamic-oxaloacetic transaminase,GOT)水平,根据亚硝酸盐氧化法测定总胆红素(total bilirubin,TBil)水平,试剂盒厂家为美康生物科技股份有限公司。
1.3 治疗及检测方法
口服恩替卡韦片(齐鲁制药有限公司,国药准字H20203225),每次0.5 mg,每日1次,连续治疗12个月。分别于治疗前及治疗3、6、12个月时,采集患者空腹静脉血3 mL,以3 000 r·min-1离心处理10 min,取上清液,根据荧光定量聚合酶链式反应法测定HBV-DNA水平,试剂盒购自广州达安基因股份有限公司。于治疗结束后,参照《慢性乙型肝炎抗病毒治疗药物临床试验技术指导原则专家意见》[7]评价血清学应答情况:血清HBeAg阴转或HBeAg血清学转换,以及HBsAg阴转或HBeAg血清学转换为血清学应答,否则为未应答。
1.4 观察指标
(1)应答组和未应答组基线资料;(2)应答组和未应答组治疗前及治疗3、6、12个月时血清HBV-DNA表达;(3)治疗3、6个月时血清HBV-DNA对CHB患者NAs抗病毒治疗未应答的预测价值。
1.5 统计学方法

2 结果
2.1 基线资料
83例CHB患者中完全血清学应答46例,占比55.42%,纳入应答组;不完全血清学应答37例,占比44.58%,纳入未应答组。两组患者年龄、性别等基线资料比较,差异无统计学意义(P>0.05)。见表1。
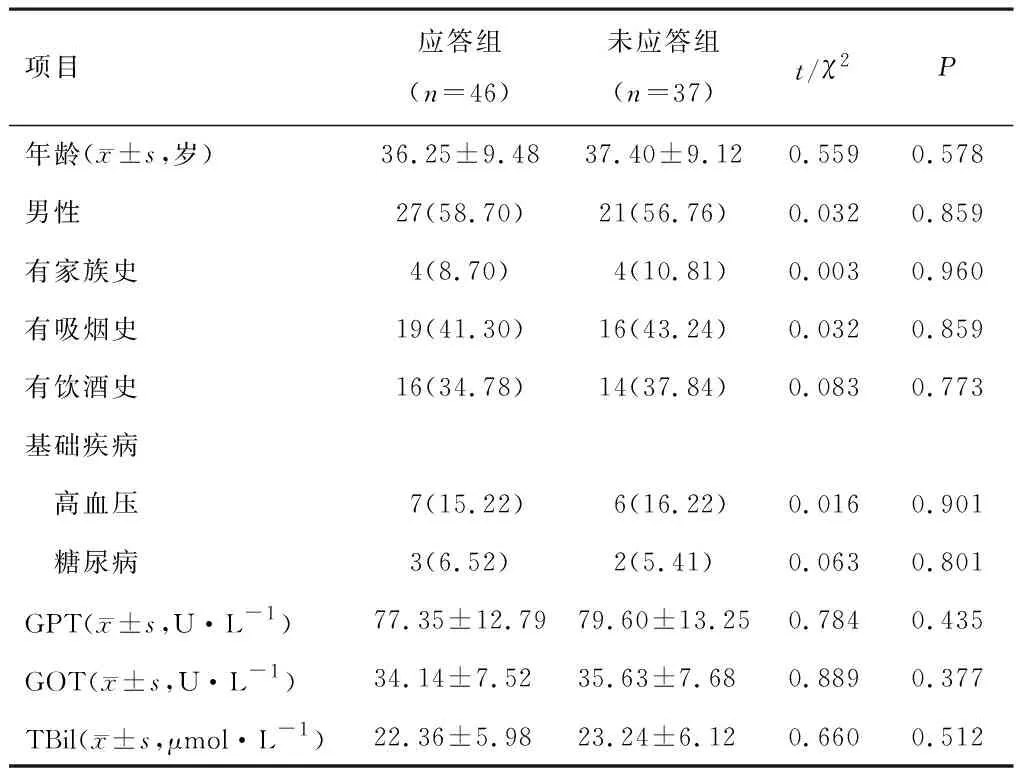
表1 应答组和未应答组基线资料比较
2.2 应答组和未应答组血清HBV-DNA表达
治疗前,应答组和未应答组HBV-DNA比较,差异无统计学意义(P>0.05);两组治疗前至治疗12个月的HBV-DNA呈逐渐下降趋势,组间、时点、交互效应有统计学意义(P<0.05)。见表2。
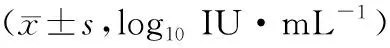
表2 应答组和未应答组血清HBV-DNA表达比较
2.3 血清HBV-DNA对CHB患者NAs抗病毒治疗未应答的预测价值
将CHB患者NAs抗病毒治疗效果作为状态变量(应答=0,未应答=1),将治疗3、6个月时血清HBV-DNA作为检验变量,绘制ROC曲线,结果显示,治疗3个月时HBV-DNA对CHB患者NAs抗病毒治疗未应答的预测价值较低(AUC=0.694,P=0.002),治疗6个月时HBV-DNA对CHB患者NAs抗病毒治疗未应答具有一定预测价值(AUC=0.751,P<0.001)。见表3。
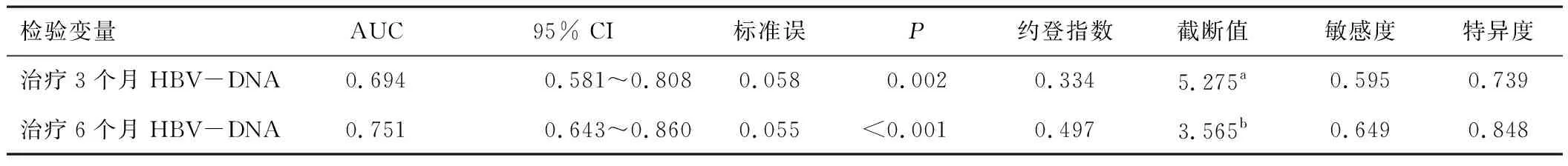
表3 治疗3个月及治疗6个月HBV-DNA的预测效能分析
3 讨论
随着国家肝炎监测工作的全面加强,一般人群感染HBV的风险下降,尽管如此,中国在全世界范围内仍属于CHB高流行区域[8]。NAs是临床公认的抗HBV治疗药物,主要以恩替卡韦等为主,能有效控制CHB患者病情,减少并发症发生[9]。但由于NAs无法直接作用于肝内cccDNA、HBV易发生耐药变异、CHB患者免疫耐受程度个体差异大等原因,临床CHB功能性治愈率仍较低,患者病情易反复,导致肝衰竭的发生风险日益加剧[10]。本研究结果显示,83例CHB患者中,治疗后不完全血清学应答的患者有37例,未应答率达44.58%,提示CHB患者NAs抗病毒治疗后未应答率较高,临床需要加以关注。
本研究结果显示,两组治疗前HBV-DNA比较差异不显著,两组治疗前至治疗12个月时血清HBV-DNA水平均逐渐下降,充分证实了NAs抗病毒治疗的有效性。吴凤萍等[11]研究分析恩替卡韦单药治疗CHB期间HBV-DNA的动态变化发现,随着治疗时间的延长,HBV-DNA逐渐下降,本研究结果与之一致。恩替卡韦为第三代NAs药物,属于鸟嘌呤核苷类似物,进入人体后会逐步三磷酸化,通过模拟可合成DNA的脱氧核苷三磷酸,与HBV多聚酶的天然底物三磷酸脱氧鸟嘌呤苷竞争,从而在逆转录合成过程中直接抑制HBV-DNA正链合成,进而降低HBV-DNA水平[12-13]。
本研究结果显示,应答组在治疗3、6、12个月时HBV-DNA均高于未应答组,HBV-DNA表达上调导致CHB患者抗病毒治疗未应答风险增加,提示血清HBV-DNA水平与患者治疗效果密切相关。在CHB发生、发展过程中,HBV进入机体后主要在肝细胞内进行复制并形成cccDNA;而cccDNA是HBV复制的源头,其存在是CHB无法完全治愈的关键原因,故监测cccDNA可反映CHB患者抗病毒治疗效果,但其只能通过肝穿刺测得,取材困难且风险高,临床难以推广[14]。HBV-DNA作为病毒血清学标志物,与肝内cccDNA密切相关,可在一定程度上反映cccDNA的存在及转录活性,且血清HBV-DNA越高提示肝内cccDNA含量升高,这意味着HBV处于大量复制的状态,从而影响恩替卡韦对HBV的杀伤效果[15]。本研究进一步分析发现,治疗3个月时HBV-DNA对CHB患者NAs抗病毒治疗未应答的预测价值较低,治疗6个月时HBV-DNA对CHB患者NAs抗病毒治疗未应答具有一定预测价值,提示治疗6个月时HBV-DNA可作为抗病毒治疗未应答的预测指标。临床可在患者采用NAs抗病毒治疗6个月时检测其血清HBV-DNA水平,当HBV-DNA>3.565 log10IU·mL-1时,需警惕抗病毒治疗未应答情况的发生,考虑尽早调整治疗方案,从而改善CHB患者临床预后。
4 结论
血清HBV-DNA表达在CHB患者NAs抗病毒治疗前后变化明显,治疗前血清HBV-DNA可作为治疗后未应答的预测指标。本研究的局限性在于,研究样本量较小,且数据均来自河南省人民医院,增加了选择偏倚的风险,还需在未来开展多中心、大样本研究,改进本研究不足,进一步明确血清HBV-DNA对CHB患者的临床指导意义。
