芜菁多糖铁配合物的合成工艺研究
2024-05-07阿曼妮萨麦提如则吴美美海力茜陶尔大洪
阿曼妮萨·麦提如则, 吴美美, 王 鑫, 刘 瑾, 徐 茜, 海力茜·陶尔大洪
(新疆医科大学1药学院, 2基础医学院, 乌鲁木齐 830017)
新疆芜菁(BrassicarapaL.)为十字花科属种植物芜菁的根茎,其主要化学成分为黄酮、多糖、生物碱、皂苷、挥发油等[1-2],具有抗衰老、抗辐射、预防心血管疾病的作用[3-4]。其中的多糖具有抗氧化、抗衰老、抗疲劳等作用[5-7]。多糖铁配合物(Polysaccharide-iron complex,PIC)是生物多糖与铁离子通过三氯化铁共热法复合而成的一种多糖和铁元素的配合物,用作补铁剂时,不仅结构稳定、溶解性好、对胃肠道刺激性小,还具有铁螯合能力强、生物利用度广等优点,补铁的同时,还能起到促进血液循环、降血糖、调节血压等作用[8-9]。本研究采用芜菁多糖与FeCl3共热法建立BP-Fe(Ⅲ)配合物的最佳合成方法,测定铁的含量,现报道如下。
1 材料与方法
1.1 试药芜菁干燥片(新疆艾力努尔有限公司);铁标准溶液(北京嘉世玉禾化工技术研究院,083183);三氯化铁(天津鑫伯特化工有限公司,20221108);枸橼酸钠(天津永晟精细化有限公司,20140416);1.10-菲啰啉(天津天新精细化工开发中心,20191102);氯化羟胺(天津天新精细化工开发中心,20140102);乙酸钠(天津鑫伯特化工有限公司,202200706);无水乙醇(天津鑫铂特化工有限公司,20211208);硫氰酸钾(成都科隆化学品有限公司,2017050101);氢氧化钠(天津盛奥化学试剂有限公司,20160307);95%乙醇(天津凯通化学试剂有限公司,20221125);冰乙酸(天津富宇精细化工有限公司,20120911)。
1.2 仪器800T型多功能粉碎机(永康敏业工贸有限公司);AB135-8型分析天平(常州幸运电子设备有限公司);N-1001型旋转蒸发仪(上海爱朗仪器有限公司);电热恒温水浴锅(北京永光明医疗仪器有限公司);SHB-lll型循环水式多用真空泵(郑州长城科工贸有限公司);BY111-0-100酒精计(河北省武强县滏阳仪表厂);UV-2700型紫外分光光度计(岛津仪器有限责任公司)。
1.3 芜菁多糖的提取与除蛋白方法
1.3.1 芜菁粗多糖的提取方法 取脱脂后的芜菁100 g,加水3 L,在90℃温度条件下回流提取提取3次,每次120 min,将提取液浓缩,加入无水乙醇至浓度为 80%(v/v),在4℃条件下放置12 h。抽滤溶液,将沉淀室温下晾干后,用蒸馏水复溶,将溶液倒入7 000 Da分子量的透析袋,透析完毕后将袋内溶液冻干,即得芜菁粗多糖。
1.3.2 芜菁粗多糖的除蛋白方法 采用AB-8大孔吸附树脂湿法装柱(柱床体积700 mL),吸取“1.3.1”项下芜菁粗多糖上清液缓慢上样,静态吸附15 min,控制流速,收集流出液。用7 000 Da的透析袋透析,浓缩,冷冻干燥,即得到芜菁多糖。
1.4 BP-Fe(Ⅲ)配合物的合成方法取“1.3.2”项下芜菁多糖0.2 g和枸橼酸钠0.1 g于烧杯中,加入50 mL蒸馏水溶解,加入2 mol/L FeCl3溶液和20%的NaOH溶液,使溶液pH值为8,观察反应液,当反应液中生成的沉淀不再溶解时停止加FeCl3溶液和NaOH溶液,继续反应2 h。待反应完全后将反应液转移到离心管中,8 000 r/min离心25 min,弃去沉淀,将上清液用3倍体积的无水乙醇醇沉,在4℃条件下放置12 h。将醇沉混悬液至于离心管中,8 000 r/min离心5 min,弃去上清液,将沉淀物用无水乙醇洗涤,8 000 r/min离心3次,每次5 min。取出沉淀自然干燥,即得到BP-Fe(Ⅲ)配合物。用适量蒸馏水溶解BP-Fe(Ⅲ)配合物,充分溶解后,将所得溶液置于透析袋中除盐,浓缩后冷冻干燥,即得BP-Fe(Ⅲ)配合物。
1.5 BP-Fe(Ⅲ)配合物合成单因素实验设计考察不同时间、温度、反应液pH值、枸橼酸钠和芜菁多糖质量比(m1/m2)对BP-Fe(Ⅲ)配合物中铁含量的影响,单因素实验设计见表1。
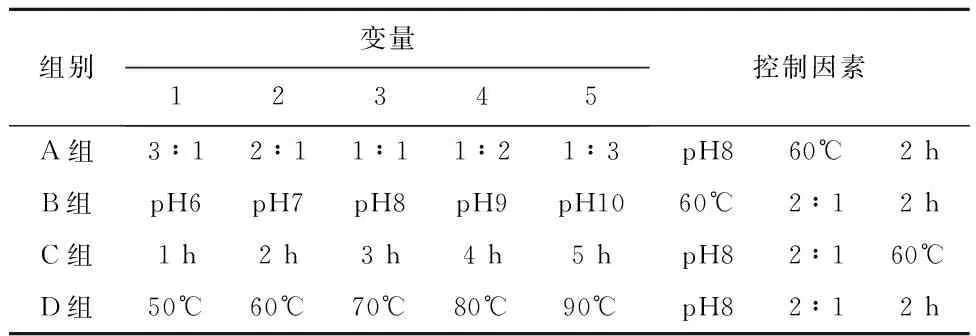
表1 单因素实验设计表
1.6 BP-Fe(Ⅲ)配合物合成工艺的正交实验设计根据“1.5”项下所得结果,对BP-Fe(Ⅲ)配合物的合成工艺进行优化,正交实验设计见表2。

表2 L9(34)正交实验因素水平表
1.7 BP-Fe(Ⅲ)配合物中铁含量的测定吸取0、1.00、2.00、4.00、6.00、8.00、10.00 mL标准铁溶液(10 μg/mL)至50 mL容量瓶中,分别加入1.0 mL 10%氯化羟胺溶液,混合均匀,放置5min后,加入0.15%1.10-菲啰啉2.0 mL,1.0 mol/L的乙酸钠溶液5.0 mL ,加蒸馏水定容至刻度,混匀,静置显色20 min,测定510 nm处A值[10],以铁的质量浓度为横坐标,吸光度为纵坐标绘制标准曲线,回归方程为:Y=0.195 3X+0.000 7,R2=0.999 9。配制300 μg/mL的样品溶液,从中移取5 mL,转移至25 mL容量瓶中,按标准曲线方法进行相同操作,将测得结果代入标准曲线中,计算BP-Fe(Ⅲ)配合物中的铁含量。铁含量/%=MFeM多糖铁×100%。
1.8 方法学考察
1.8.1 精密度实验 量取“1.7”项下标准铁溶液5 mL按照“1.7”项下方法,连续测定510 nm处A值5次,计算RSD值。
1.8.2 稳定性实验 量取“1.7”项下供试品溶液5 mL按照“1.7”项下方法, 分别在0、 30、 60、 90、 120 min时在510 nm处A值,计算RSD值。
1.8.3 重现性实验 将同一样品溶液平行配置6份按“1.7”项下方法,测定510 nm处吸光度A值,计算RSD值。
1.8.4 加样回收率实验 取“1.7”项下样品溶液(0.3 mg/mL)分别吸取9份溶液,每份0.2 mL,每3份1组,分别加铁标准溶液(0.01 mg/mL) 0.86、1.10、1.30 mL于3组溶液中,摇匀,加水至2.0 mL,按照“1.7”项下方法测定510 nm处的A值,计算RSD值。
1.9 铁离子特征反应分别配置10 mg/mL的BP-Fe(Ⅲ)配合物溶液和三氯化铁溶液,分别取5 mL加1 mL 10%硫氰酸钾,振荡,观察现象。
1.10 BP-Fe(Ⅲ)配合物和芜菁多糖的红外光谱测定采用溴化钾压片法,将干燥的BP-Fe(Ⅲ)配合物和芜菁多糖样品分别与溴化钾混合,磨粉压片,在4 500~500 cm-1处扫描,扫描10次,测得BP-Fe(Ⅲ)配合物和芜菁多糖的红外光谱图。
2 结果
2.1 反应pH值、时间、温度和橼酸钠与多糖的质量比对BP-Fe(Ⅲ)配合物中铁含量的影响当反应时间为2 h,反应温度为60℃,枸橼酸钠与多糖的质量比为1∶2时,随着pH增大,BP-Fe(Ⅲ)配合物中铁含量降低,当pH为6时BP-Fe(Ⅲ)配合物中铁含量最高为3.41%,见图1。
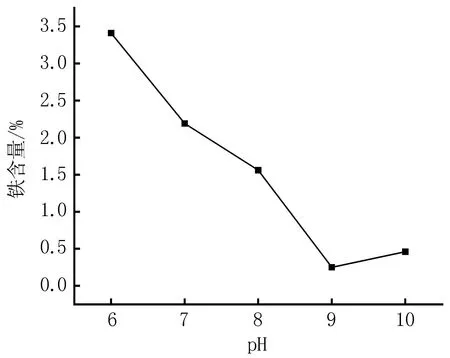
图1 pH值对BP-Fe(Ⅲ)配合物中铁含量的影响
2.2 反应时间对BP-Fe(Ⅲ)配合物中铁含量的影响当反应温度为60℃,枸橼酸钠与多糖的质量比为1∶2,pH值为8时,随着反应时间增长,BP-Fe(Ⅲ)配合物中铁含量降低,在1 h时BP-Fe(Ⅲ)配合物中铁含量最大为1.6%,见图2。
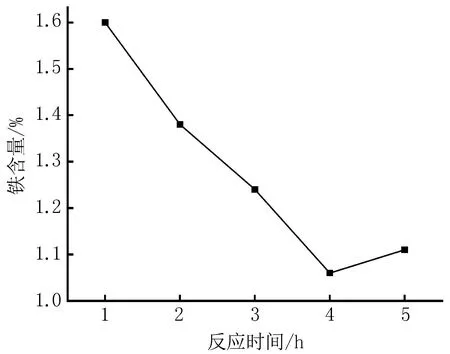
图2 反应时间对BP-Fe(Ⅲ)配合物中铁含量的影响
2.3 反应温度对BP-Fe(Ⅲ)配合物中铁含量的影响当反应时间为2 h,pH值为8,枸橼酸钠与多糖的质量比为1∶2时,随着反应温度升高,BP-Fe(Ⅲ)配合物中铁含量先升高后降低,当温度小于60℃时,随温度的升高BP-Fe(Ⅲ)配合物铁含量逐渐升高,在60℃时铁含量最高为3.89%。反应温度大于60℃时,铁含量降低,见图3。
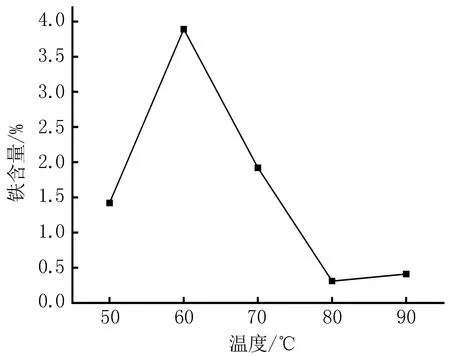
图3 反应温度对BP-Fe(Ⅲ)配合物中铁含量的影响
2.4 枸橼酸钠与多糖的质量比对BP-Fe(Ⅲ)配合物中铁含量的影响当反应时间为2 h,pH值为8,反应温度为60℃时,随着枸橼酸钠与多糖质量比增加,BP-Fe(Ⅲ)配合物中铁含量升高,当枸橼酸钠与多糖质量比为2∶1时BP-Fe(Ⅲ)配合物中铁含量最大为1.81%,见图4。

图4 枸橼酸钠与多糖的质量比对BP-Fe(Ⅲ)配合物中铁含量的影响
2.5 BP-Fe(Ⅲ)配合物合成正交实验结果正交实验结果显示,影响BP-Fe(Ⅲ)配合物中铁含量因素的顺序为枸橼酸钠和芜菁多糖质量比(A)大于反应液pH值(B)大于反应时间(C)大于反应温度(D)。最优合成工艺条件为A3B1C3D2,即枸橼酸钠和多糖质量比2∶1,反应时间3 h,反应液pH=6,反应温度60℃为最佳工艺条件,见表3。
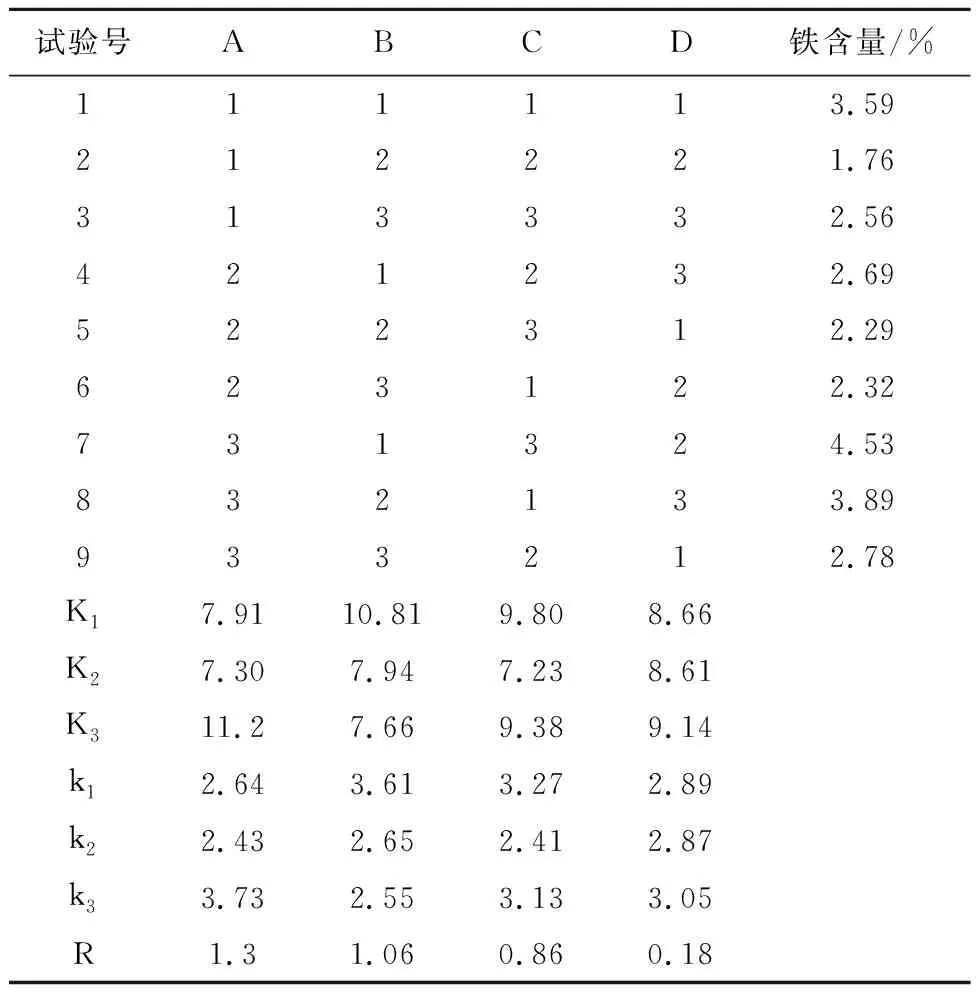
表3 BP-Fe(Ⅲ)配合物合成正交实验结果
2.6 方法学考察结果
2.6.1 精密度实验 精密度实验结果表明RSD为1.6%(n=6)<2.0%,表明仪器精密度良好,见表4。

表4 精密度实验
2.6.2 稳定性实验 稳定性试验结果表明RSD为1.8%(n=5)<2.0%,表明方法稳定性良好,见表5。

表5 稳定性实验
2.6.3 重现性实验 重现性试验结果表明RSD为0.9%(n=6)<2.0%,表明方法重现性良好,见表6。

表6 重复性实验
2.6.4 加样回收率实验 平均回收率为88.3%~104.7%,RSD在0.4%~1.4%之间,表明方法准确可行,见表7。
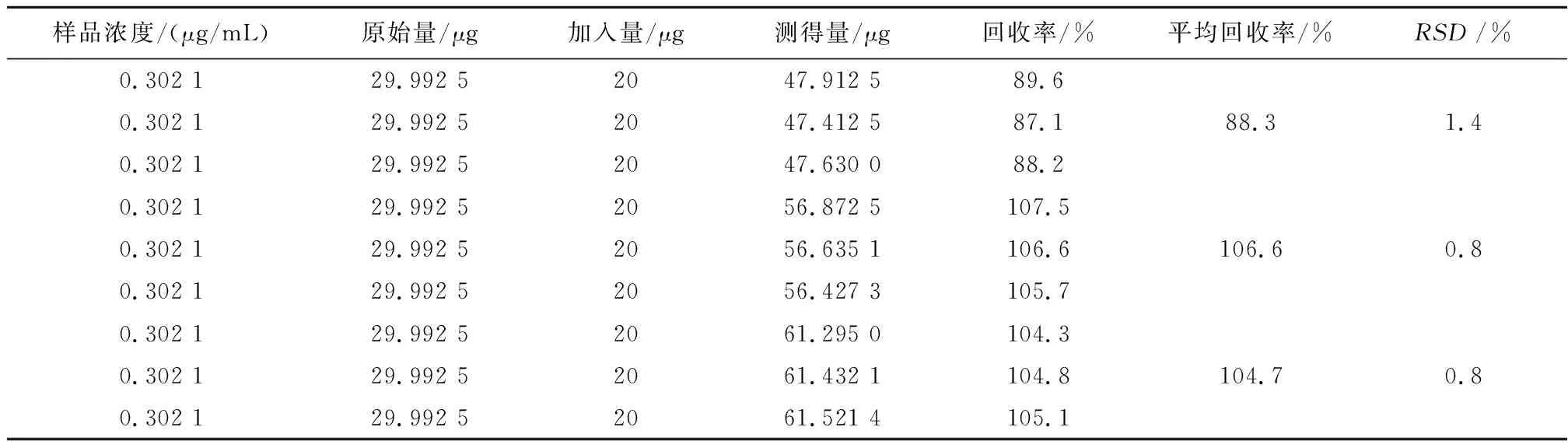
表7 加样回收率实验
2.7 铁离子特征反应结果三氯化铁溶液与硫氰酸钾反应,颜色由黄色变为暗红色;芜菁多糖铁溶液加入硫氰酸钾之后没有颜色变化,说明配合物中游离的Fe3+浓度很低,不能与硫氰酸钾反应生成有颜色的配合物,芜菁多糖与铁络合成稳定的配合物。铁离子特征反应结果见图5。

(A:显色反应前;B:显色反应后)
2.8 BP-Fe(Ⅲ)配合物和芜菁多糖的红外光谱图分析BP-Fe(Ⅲ)配合物主要基团特征吸收峰与芜菁多糖相似,BP-Fe(Ⅲ)配合物在3 400~3 300 cm-1附近的羟基特征吸收峰较芜菁多糖宽,最大吸收峰由3 379 cm-1变为3 387 cm-1。说明芜菁多糖与Fe3+形成稳定配合物后,基本结构无较大变化;在BP-Fe(Ⅲ)配合物合成过程中,反应物芜菁多糖结构中的的羰基和羟基参与配合反应,铁离子具有吸电子作用,可增大羰基极化程度,使羰基振动偶极矩变大,可见1 620 cm-1处羰基伸缩振动强度增加,推断BP-Fe(Ⅲ)中存在与FeOOH相似的结构,见图6。

图6 BP-Fe(Ⅲ)配合物和芜菁多糖的红外光谱图
3 讨论
缺铁性贫血(Iron deficiency anemia,IDA)为营养缺乏性疾病,病因多为患者长期处于铁摄入不足或患者自身铁成分丢失过快,不足以为红细胞提供所需铁成分的状态,进而引起的贫血症状[11]。目前临床上主要应用硫酸亚铁、右旋糖酐铁等口服补铁剂进行治疗,但其稳定性较差、不易吸收,并且容易引起恶心、便秘、胃肠道不适等不良反应[12]。PIC作为新型补铁剂,具有安全性高、不良反应少、铁元素更易于被人体吸收等优势,成为国内外新型补铁剂研究的热点[13-14]。有研究发现制备多糖铁的方法以FeCl3法、硫酸铁铵法及模拟生物矿化法为主,其中FeCl3法工艺相对成熟,制作的周期短、产物的铁含量高,成本低已成为现今制备多糖铁的主要方法[15]。芜菁作为一种药食同源植物,栽培历史悠久,产量较高、品质优良,耐储藏,供应时间长,多糖含量高,以芜菁为原料制备多糖铁配合物具有原料来源广的特点[16]。
本实验用FeCl3法,与芜菁多糖合成BP-Fe(Ⅲ)配合物,通过正交实验优化得到最优合成工艺,为开发新型口服补铁剂提供参考。
