2例斜外侧腰椎椎间融合术并发乳糜漏的临床特征分析
2024-05-06张聃史明张文捷汪丽伟罗满张勇
张聃,史明,张文捷,汪丽伟,罗满,张勇
(广西中医药大学附属国际壮医医院骨关节与脊柱科,广西 南宁 530201)
近年来,斜外侧腰椎椎间融合术(oblique lateral interbody fusion,OLIF)作为一种微创手术方式,广泛应用于治疗腰椎退行性疾病。随着该技术的普及和应用,手术并发症的问题也逐渐凸显,常见的并发症包括神经损伤、血管损伤、椎体终板损伤和融合器沉降等[1-2]。淋巴漏是腹部手术中较为少见的并发症,其中腹部乳糜漏作为淋巴漏的特殊形式,主要由乳糜池周围淋巴管破裂所引发,使得腹腔引流出现乳白色或乳糜样液体[3]。乳糜漏在OLIF手术中较罕见,目前文献中鲜有报道。广西中医药大学附属国际壮医医院出现过2例OLIF术后并发乳糜漏患者,现报告如下。
1 病历资料
1.1 患者1 女性,85岁,2019年11月因“腰背痛3年伴左下肢间歇性跛行1年”入院。既往高血压病史。专科查体:胸腰段脊柱左侧弯畸形,生理前凸消失,L2~5棘突及椎旁叩击痛(+);左下肢跛行步态,膝腱反射、跟腱反射对称性减弱,四肢肌力肌张力均正常,直腿抬高试验(-);左侧股神经牵拉试验(+),左大腿前外侧皮肤感觉稍有迟钝;生理反射存在,病理征(-)。术前X线片示腰椎左侧弯伴旋转,L2~3、L3~4、L4~5椎间隙不对称性狭窄;术前CT示腰椎退变性改变,L2~3、L3~4椎间隙高度丢失,椎间孔狭窄;术前腹主动脉CT血管造影术未见明显走行异常。临床诊断:(1)腰椎退变性侧凸伴腰椎管狭窄症;(2)高血压病。排除手术禁忌证后,行“L2~3、L3~4、L4~5OLIF手术”。术中依次完成L2~5间隙的融合器置入,术中出血约80 mL,术后常规腹膜后放置引流管。术后X线片提示L2~5椎间隙融合器在位良好,椎间隙高度恢复良好,腰椎冠状位畸形矫正满意。
术后1 d引流出血性液体约50 mL,术后2 d约70 mL,术后3 d引流袋内新增出现约200 mL乳白色液体(见图1a)。患者无发热及腹痛腹胀,大小便正常,腹部切口干燥无渗出。送检引流液常规提示李凡他试验(+),生化提示总蛋白 32.8 g/L,13 000转高速离心后呈乳白色与淡血性分层(见图1b),高倍镜下可见脂肪球(见图1c),考虑乳糜液混入。判断为术后乳糜漏。术后予以静滴头孢呋辛48 h,嘱患者严格卧床休息,采取左侧卧位利于引流;低盐低脂高蛋白饮食;术后6 d乳糜液引流量无明显增加;术后7 d实验室检查提示白蛋白30.8 g/L,行腹部CT未见腹腔积液,拔除引流管;嘱患者佩戴支具下地行走,患者腰背部胀痛感以及双下肢肌力恢复良好,于术后10 d出院。
1.2 患者2 男性,52岁,2023年8月因“腰椎术后反复腰腿痛5年”入院。患者于2018年因腰椎管狭窄症在外院行“后路L4~5、L5S1椎间盘切除椎管减压椎弓根螺钉内固定术”,术后反复腰痛伴左大腿前外侧疼痛,活动后加重,休息后缓解。既往双肾结石病史。专科查体:腰椎生理曲度正常,腰后可见一长约15 cm纵行手术瘢痕,L3~S1棘突及椎旁压痛(+),腰部屈伸活动受限;左侧股神经牵拉试验(+),双下肢肌力肌张力均正常,生理反射存在,病理征(-)。术前X线片示腰椎生理曲度存在,L3椎体向后移位(未超过下一位椎体1/4),L4~S1椎体内固定在位;术前MRI示L3~4
椎间盘向后突出、双侧侧隐窝变窄、两侧神经根受压。临床诊断:(1)腰椎滑脱症(L3椎体Ⅰ度后滑脱);(2)腰椎管狭窄症术后邻椎病;(3)双肾结石。排除手术禁忌证后,行“L3~4OLIF术+后路L4~S1内固定装置去除术”。术中完成L3~4间隙的融合器置入及L4~S1内固定装置去除,术中出血约100 mL,术后常规腰部及腹膜后放置引流管。术后CT示L3~4椎间隙融合器在位良好,L4~S1金属内固定已移除。
术后1 d连接腹部引流袋内可见引流液分层:上层约200 mL乳白色液及下层约150 mL血性液体,术后2 d引流出80 mL乳白色浑浊液,术后3 d新增20 mL乳白色液体(见图2a)。患者无发热及腹痛腹胀,大小便正常,腹部切口干燥无渗出。送检引流液常规提示“乳糜试验(+)”,高倍镜下可见脂肪球(见图2b),判断为术后乳糜漏。术后予以静滴头孢唑啉钠48 h,嘱患者严格卧床休息,左侧卧位利于引流;低盐低脂高蛋白饮食;观察术后4~5 d乳糜液引流量无明显增加并拔除引流管;术后7 d实验室检查提示白蛋白31.9 g/L;嘱患者佩戴支具下地行走,患者腰腿痛较入院时明显改善,于术后8 d出院。
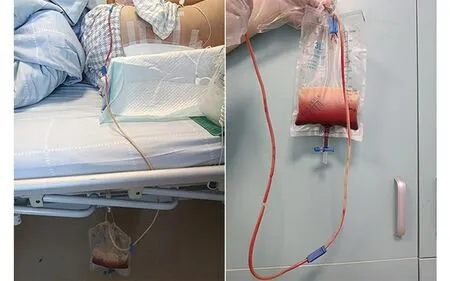
a 术后引流袋内乳白色引流液
2 讨 论
以OLIF为代表的腰椎侧方融合技术,是近几年来发展较快的微创椎间融合术式,患者术中出血少,术后康复时间明显缩短。主要技术优势包括不破坏脊柱后部肌肉及脊柱后韧带的完整性,有效恢复退变性椎间隙高度及增加椎管容积,矫正脊柱冠状面畸形等,目前已逐步替代部分开放性腰椎融合术。随着该技术的迅速普及,与之相关的手术并发症也日益增多[4]。腹膜后乳糜漏是OLIF手术的罕见并发症[5],需要特别关注。乳糜池位于L1或L2前面、由左右腰干和肠干汇合形成的膨大区,主要收集肠干、左右腰干的淋巴,注入至胸导管中。乳糜池作为胸导管的起始部,多位于T12和L2椎体间,紧贴右膈角及腹腔后壁腹主动脉,向上穿行膈肌的主动脉裂口后汇入锁骨下静脉或颈内静脉。因此,腰椎前路手术有损伤乳糜池及周围淋巴系统的可能性。乳糜漏或淋巴漏的发生是由于局部区域的淋巴液循环途径被破坏或中断,淋巴液压力大于组织液压力或体腔内压而引起外漏。本组2例患者均采用Stand-Alone OLIF术式,采取右侧卧位左侧入路,术中按照OLIF手术“斜入路、直操作”的规范,在直视下完成责任椎间隙操作,而且均处理了高位椎间盘。尽管术中未发现明显可视性损伤,但从解剖位置来看,腰椎的高位椎间盘更靠近乳糜池,器械牵拉、椎间隙处理、试模放置及假体植入等操作均可能造成乳糜池周围的淋巴管道损伤并导致阻塞。因此,腰椎高位椎间隙的侧前方手术或可视为并发乳糜漏的一种高危因素。
乳糜流速取决于饮食、肠道蠕动功能、肢体活动、呼吸运动、咳嗽、邻近动脉搏动及腹内压和胸腔压力的变化[6]。当发生乳糜漏时,会看到乳糜样的白色液体,2例患者的腹部引流液外观与此一致。与其他部位淋巴漏的浆液性或淡黄色液体不同,乳糜液内的甘油三酯含量明显更高[7]。发生大量乳糜漏的患者可出现持续性腹痛、腹胀及恶心呕吐等,淋巴液的大量丢失还会伴随甘油三酯、电解质、淋巴细胞、免疫球蛋白等丢失,引起患者脱水、营养缺乏和免疫障碍。2例患者发生乳糜漏后,尽管未出现胃肠道不良反应,实验室检查白细胞、电解质水平正常,但是白蛋白水平均出现明显下降。术后乳糜漏的诊断尚无统一标准,引流液实验室蛋白测定≥32 g/L及甘油三酯≥100 mg/L、淋巴管造影术均是有效的诊断方法[8]。也有观点认为同时满足“术后非血性乳白色引流液;引流液排除出血、胆漏、胰漏、肠漏等并发症;通过乳糜试验定性或甘油三酯测定为淋巴液”即可判定为淋巴漏或乳糜漏[9]。本研究中,患者1引流液蛋白测定≥32 g/L,患者2乳糜试验(+),并同时在高倍显微镜下发现脂肪微粒存在,综合渗出物外观性状,最终判定引流液为乳糜液。
关于术后乳糜漏或淋巴漏的预防及治疗目前暂无统一标准或指南。研究表明术前禁食后淋巴液流量可明显减少,术前纠正贫血及低蛋白血症能减少术后淋巴漏的发生率[3]。通常术后淋巴液引流<500 mL/d时首选保守治疗,常见治疗方案为控制饮食、全胃肠外营养、药物治疗、淋巴管造影术等;饮食上加强摄入中链脂肪酸、高蛋白饮食及多种维生素和微量元素补充,减少长链脂肪酸摄入[10]。淋巴液引流≥500 mL/d,若肠内营养无法减少淋巴液量,可选择至少持续3周的全胃肠外营养支持[3]。生长抑素、胰脂肪酶抑制剂等被证实可减少淋巴液的产生[6,11]。淋巴管造影术作为诊断性方法,也可用于治疗术后淋巴漏,但需注意操作中出现造影剂栓塞和过敏反应的并发症[12]。保守治疗的预后普遍良好,极少需要进行手术干预。选择手术的患者多数为至少连续5 d淋巴液引流≥1 000 mL/d或保守治疗无效的乳糜漏(≥2周),常见手术方式为结扎关闭淋巴管漏口或行腹腔-静脉分流术[13-14]。手术治疗乳糜漏的相关并发症和死亡率较高,需严格评估病情后谨慎施行[9,15]。本研究诊治的2例乳糜漏患者,术后淋巴液引流量均<500 mL/d且逐日减少,配合卧床休息、改变体位、调节饮食收获了良好的预后。至于何时拔除腹膜后引流管,目前暂无定论。过往经验是在腹部切口愈合良好、未发生明显胃肠道不良反应前提下,连续48 h引流袋内新增乳糜液<20 mL可予以拔除。另外,术前行胸部X线或胸部CT评估膈肌的重要性不容忽视,这是因为完整的膈肌能够有效防止拔除引流管后,乳糜液通过主动脉裂孔进入胸腔,从而避免乳糜胸的发生[16];同时,膈肌的封闭作用有利于淋巴管的自愈。经进一步分析,低压淋巴系统、淋巴管之间的多重连接以及与静脉系统的吻合,使得丰富的淋巴管网可以重新构建被破坏的淋巴流,从而自动关闭渗漏口,乳糜漏自然愈合,很少引起明显的临床症状。
OLIF术后乳糜漏是由多种因素导致的局部淋巴循环受损所致,手术操作损伤淋巴管是发生术后乳糜漏的重要原因。完整周密的术前评估是预防乳糜漏的基本措施,细致规范的术中操作是预防乳糜漏的关键环节,密切的术后观察和及时的个体化处理是乳糜漏获得良好预后的重要保障。非手术治疗应当作为首选,保持引流通畅、加强高蛋白饮食是治疗乳糜漏的关键。根据本研究病例经验,结合文献资料,大多数乳糜漏可通过保守治疗而获得良好预后,而保守治疗失败的患者,需评估病情后再谨慎决定是否进行二次手术。
