VSD 联合自体富血小板血浆凝胶在糖尿病慢性难愈合创面植皮治疗中的应用
2024-04-22王鸿彬
王鸿彬 程 杰
(1 内蒙古自治区精神卫生中心内蒙古自治区第三医院心身健康体检保健中心,内蒙古 呼和浩特 010030;2 内蒙古医科大学第二附属医院)
在经济高速发展和老龄化程度加重的环境下,糖尿病有着较高的发病率, 糖尿病在我国成年人的发病率约在11%, 由此推测糖尿病患者约1.14 亿[1],糖尿病足(DFU)的慢性难愈合创面是糖尿病严重的并发症之一, 常规的治疗方案虽然能促进创面的愈合,但治疗周期长、治疗费用较高等问题对患者造成较大的负担[2]。 近年来,使用持续封闭负压引流技术(VSD)治疗糖尿病慢性难愈合创面取得了一些成绩,但此技术是通过VSD 材料维持创面的负压环境来促进创面局部的血运循环, 此类型创面的愈合不但需要改善创面局部的血运循环, 更需要细胞因子等生物活性物质的刺激[3]。 自体富血小板血浆凝胶(APG)具有促进细胞因子活化的作用, 能从多方面改善创面微循环障碍并修复损伤的神经[4-5]。 基于此理论,本研究选取80 例糖尿病慢性难愈合创面患者为对象,分析VSD 联合APG 在糖尿病慢性难愈合创面植皮治疗中的应用。
1 临床资料
1.1 一般资料
选取内蒙古自治区第三医院2021 年2 月—2022 年6 月收治的80 例糖尿病慢性难愈合创面患者为研究对象,随机分为随机分为观察组(n=37)和对照组(n=43)。 对照组年龄34~73 岁,平均年龄(61.37±6.29)岁;病程7~22 年,平均病程(11.47±3.58)年。 观察组年龄34~74 岁,平均年龄(61.38±6.59)岁;病程6~22 年,平均病程(11.49±3.68)年。2组患者一般资料比较,差异无统计学意义(P>0.05),具有可比性。 见表1。
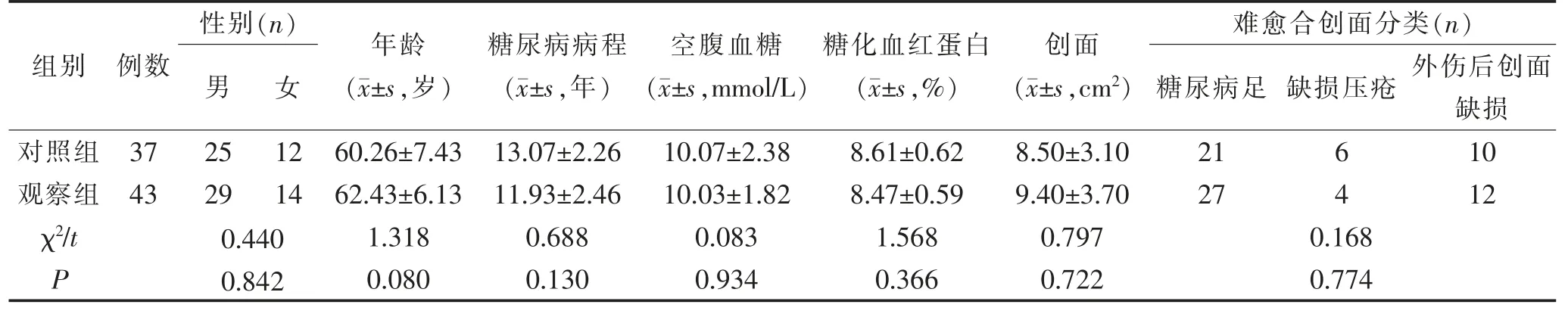
表1 2 组患者的一般资料比较
纳入标准:(1)符合糖尿病诊断标准[6];(2)在糖尿病的基础上合并皮肤难愈合创面且经常规治疗28天后未愈合;(3)患者有较好的依从性,血糖水平比较稳定;(4)神志清楚、精神系统无障碍。 排除标准:(1)非糖尿病合并的创面;(2)合并骨髓炎;(3)下肢动脉闭塞;(4)恶性肿瘤;(5)合并自身免疫性疾病或全身感染性疾病。 所有患者均签署研究知情同意书,本研究经医院医学伦理委员会审核通过。
1.2 方法
2 组患者在入院后根据血糖情况继续口服或皮下注射胰岛素进行降糖治疗, 若存在创面感染行分泌物菌培养和药敏试验, 根据药敏结果选择敏感的广谱抗生素,若存在高血压和高血脂等疾病,给予控制血压和控制血脂等调节内环境治疗,在入院后3~7天进行创面清创, 清创要彻底, 剪去创面坏死的痂皮,将创面内的坏死组织彻底清除、消灭死腔,以创面有少量血液渗出为宜,刮除创面老化的肉芽组织,用过氧化氢、 碘伏水和含庆大霉素的生理盐水反复冲洗。对照组清创术后采用VSD 覆盖创面,观察组清创后将APG 均匀的敷在创面上, 再用VSD 覆盖创面,待2 组创面达到移植皮片的条件时进行植皮术。
对照组清创术后采用VSD 覆盖创面。 修剪VSD材料,使之和创面的形态相匹配,如果存在较大的腔隙, 把VSD 材料带着夹层中的冲洗管一同填到腔隙中,通过VSD 材料吸出腔隙最底的分泌物,用无菌贴膜封闭VSD 边缘外5 厘米处,接床头负压通道,压力设置为-60~-80 mmHg, 治疗7 天后更换1 次VSD,此为一个治疗周期, 持续多个治疗周期直到能够植皮的条件,进行植皮术。
观察组清创后将APG 均匀的敷在创面上, 再用VSD 覆盖创面。先制备自体APG:患者在空腹状态下抽取肘部静脉血, 应根据患者创面大小抽取相应的静脉血,并注入抗凝管中充分摇匀,采用2 次离心法进行制备, 先将标本在离心机中以3 000 转/分钟离心10 分钟,抗凝管中的全血分成了3 层,中间层即为富含血小板和白细胞层, 取出中间层后再进行3 000 转/分钟离心10 分钟, 抗凝管中液体分成了2层,下层为富血小板血浆,得到血小板计数为(1 500~71 800)×109/L 的自体血清干细胞(PRP)。 PRP 激活剂由凝血酶和葡萄糖酸钙混合后制成, 将PRP 与PRP 激活剂混合(PRP : PRP 激活剂=10 : 1)摇匀后静止就可以制成APG,将制成的APG 尽快均匀的敷在创面上,厚度约2 毫米,在其上覆盖VSD 封闭负压吸引, 治疗7 天后拆除VSD,APG 联合VSD 覆盖创面7 天为一个治疗周期, 持续多个治疗周期直到能移植皮片的条件,给予植皮术。
植皮的方式采取的是全厚皮片拉网植皮, 植皮后继续VSD 负压吸引覆盖创面,7 天后拆除VSD,观察植皮的效果。
1.3 评价指标
(1)植皮前指标:创面细菌清除度、肉芽组织增长率及肉芽组织生长厚度。 在行植皮术前观察治疗后2 组创面细菌的数量、 肉芽组织的面积及肉芽组织的厚度。
(2)创面愈合率:测量移植皮片稳定后的创面面积,与第1 次清创后的创面进行比较计算创面愈合率,并记录创面愈合时间, 即从清创到植皮术后移植皮片稳定的时间。 创面愈合率=(原始创面的面积-未愈合创面的面积)/原始创面的面积×100%
(3)创面愈合速率:创面愈合率与创面愈合时间的比值。
(4)疗效指标:显效为溃疡创面愈合面积≥70%,创面无明显渗出,局部有新鲜肉芽组织;有效为溃疡创面愈合面积≥30%,创面可见少量渗出,创面周围出现新鲜肉芽组织; 无效为溃疡创面愈合面积≤30%,创面无显著改善,总有效率=(显效+有效)/总例数×100%[7]。
1.4 统计学分析
应用SPSS 18.0 统计学软件进行分析,符合正态分布的计量数据以均数±标准差(±s)表示,采用独立样本t检验比较组间差异;计数资料以率(n,%)表示,采用χ2检验。 以P<0.05 为差异有统计学意义。
2 结果
2.1 2 组植皮前指标比较
观察组创面细菌清除度、 肉芽组织增长率及肉芽组织生长厚度均优于对照组, 组间差异有统计学意义(P<0.05)。 见表2。
表2 2 组植皮前指标比较(±s)
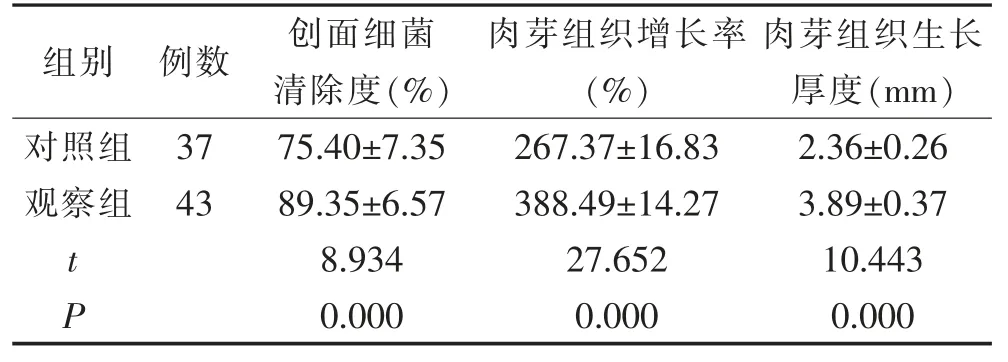
表2 2 组植皮前指标比较(±s)
?
2.2 2 组创面愈合率及速率比较
观察组创面愈合时间短于对照组,创面愈合率及速率均优于对照组,组间差异有统计学意义(P<0.05)。见表3。
表3 2 组创面愈合率及速率比较(±s)
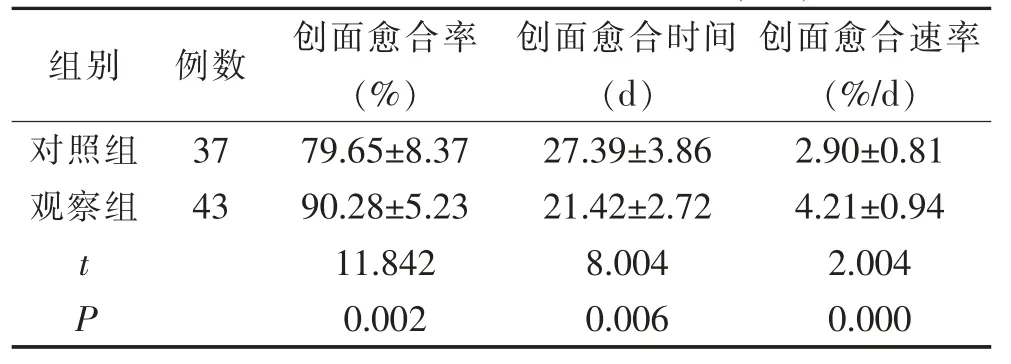
表3 2 组创面愈合率及速率比较(±s)
?
2.3 2 组治疗效果比较
观察组治疗总有效率高于对照组, 差异有统计学意义(P<0.05)。 见表4。
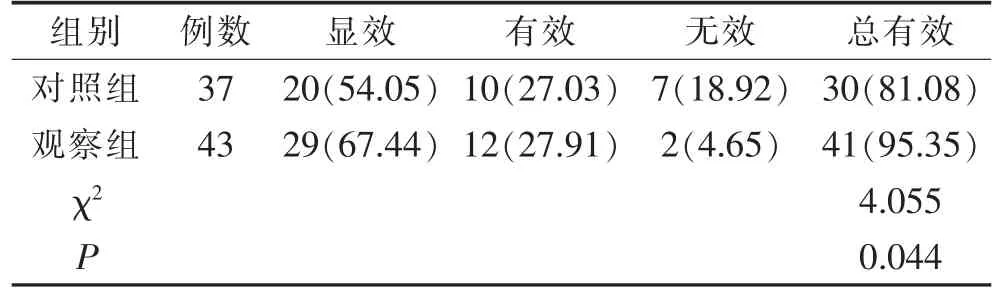
表4 2 组治疗效果比较(n,%)
3 讨论
随着经济的发展和医疗水平的进步, 使得人民生活水平有了显著提升, 生存寿命有了明显增加,伴随而来的如糖尿病等慢性疾病发病率逐年升高,糖尿病是临床最常见的慢性疾病, 长时间的高血糖状态使得使得脂质代谢紊乱, 导致了血管管壁内细胞增殖而使得管壁增厚,影响了微循环的血运,微循环的血运障碍不但使糖尿病溃疡创面愈合困难, 也使得末梢神经的营养发生障碍。 末梢神经的损伤不仅因血运障碍引起, 还因为高血糖对神经的直接毒性作用、氧化应激产生炎性因子的损伤、脂质代谢的异常对神经的损伤等。
糖尿病慢性难愈合创面就是较严重的并发症之一, 糖尿病患者慢性皮肤创面是指皮肤创面超过2周以上未愈合,若时间超过4 周且无愈合倾向,就会成为慢性难愈合创面[8]。 它的形成原因主要是微循环障碍、周围神经病变和创面感染等因素,创面不愈合就使得营养物质通过创面渗出, 使患者的营养状况和抵抗力逐渐下除,严重影响患者康复和生存质量[9]。糖尿病慢性难愈合创面的常规治疗是换药, 会损伤新生的肉芽组织,延长创面的愈合时间。 在换药过程中对于高于创面和老化的肉芽组织, 需要人为的刮除, 创面漫长的愈合过程增加患者的心理负担和经济负担。 为了防止在换药过程中出现创面干燥,影响肉芽组织的生长, 有研究指出在创面涂抹湿润烧伤膏,不但能增加创面的湿润度,也能加快创面进入炎症反应期,从而加快创面的愈合[10]。 但创面涂抹湿润烧伤膏还是需要经常换药, 在换药过程中需要把和脓性分泌物混合的药膏拭去, 虽然此方法可以相对的增加创面愈合速度, 但换药过程中会对患者造成明显的疼痛。
近年来, 一些新的治疗理念和方法应用于糖尿病足的治疗, 最具有代表性的就是负压伤口疗法(NPWT), 将海绵状的泡沫材料填充或覆盖在创面上, 用特殊的无菌半渗透薄膜覆盖NPWT 和其附近的皮肤,通过引流管将NPWT 和负压装置相连,使渗出液及时排出,VSD 是NPWT 中一种最常使用的技术。 海峡两岸医药卫生交流协会烧创伤暨组织修复专委会对NPWT 在糖尿病足创面治疗中制定应用共识,NPWT 有持续、间歇和可变负压三种使用模式,目前临床上最常用的是持续负压模式, 对于血管性溃疡的负压值建议为-60~-8mmHg,对于老年糖尿病足患者因对疼痛敏感性差、皮肤弹性差,若按常规负压值吸引可使得NPWT 周围出现水疱, 可适当降低负压值[11-12]。在使用NPWT 过程时要仔细观察引流管的通畅度,引流液的量、颜色,在使用1 或2 次后要对使用效果进行评估, 若无效建议停止使用NPWT,评估失效的原因,原因多为创面血运障碍或感染所致,待患肢血运和感染控制后再评估是否继续使用。 对于NPWT 使用的时间应根据创面的评估情况来确定,一般3~5 天更换NPWT 材料,不建议超过7 天,对于创面分泌物较多、 术前发现创面血运差的患者应适当减少每次使用NPWT 材料治疗的时间, 对于渗出液中有较明显的血性液体的患者应随时停止使用NPWT 治疗,查看创面有否有活动性出血。
对于糖尿病慢性溃疡创面愈合的重要措施是改善创面周围的血液循环,VSD 可以封闭创面减少与外界的相通、使创面的分泌物及时吸走、使创面处于负压状态, 使得VSD 具有控制感染、 扩张局部微血管, 促进肉芽组织生长等作用, 从而促进创面的愈合,虽然VSD 能有效控制感染,但它不能取代彻底的清创, 对于合并创面明显感染的患者在感染没有控制前,不建议使用VSD 进行常规的治疗,应在感染控制后再使用VSD 治疗, 创面感染明显的患者常伴有较多的渗出物, 导致引流管部分或全部堵塞使创面引流不畅, 使得创面的感染逐渐加重并使感染向深部发展,有形成蜂窝组织炎或坏死性筋膜炎的可能。本研究中2 组患者创面在使用VSD 前, 将创面进行彻底的清创并根据菌培养结果使用抗炎治疗,因此,所有患者未出现感染扩散和加重的情况出现, 对照组的患者在每次拆除VSD 见创面的渗出和分泌物逐渐减少、创面的肉芽组织逐次增多,较观察组的效果较好。
糖尿病慢性难愈创面因感染、 血液循环障碍等原因导致多种营养因子缺乏, 在创面的修复过程中需要多种细胞因子, 如血管内皮细胞因子(VEGF)、成纤维细胞生长因子 (EGF)、 胰岛素样生长因子(IGF)、白细胞介素-1(IL-1),可以促进细胞增殖和修复炎性细胞。 PRP 凝胶中的血小板激活后能释放多种细胞因子,如VEGF、EGF、IGF、IL-1、血小板衍生生长因子(PDGF)、转化生长因子-β(TGF-β)等,并且其浓度是体内浓度的3~8 倍, 这些因子通过自身作用和因子间的协同作用, 促进细胞的增殖分化和迁移,促进肉芽和纤维组织的形成,形成的纤维网状支架能为细胞的修复提供的良好的支架结构, 促进创面的修复[13]。 冯光等[14]通过研究指出,PRP 有单次提取量大、使用方式灵活、手术安全性高的特点,PRP凝胶能用于修复各类慢性伤口, 可有效促进慢性难愈性创面的愈合。
本研究中的PRP 是用自体新鲜血液制备的,避免了使用同种异体PRP 治疗出现排异反应等风险[15],制备的方式采用的是二次离心法, 此方法对设备要求比较低,操作简单,现用现制备,但在制备过程中有受到外界污染的可能, 而且如果需要制备PRP 量较大的时候,会损失一部分全血。 莫骁群等[16]研究用全自动血细胞分离机一次性制备PRP 并给予冻存,使用时解冻,此方法可有效避免二次离心法的缺点,但对设备和技术操作的要求比较高。
糖尿病慢性难愈创面的覆盖如果选择刃厚皮片植皮,因刃厚皮片较薄,愈合后的皮片耐磨性差,即便轻微摩擦也会导致皮片破溃出血或形成水疱,对于糖尿病足创面的患者尤为明显, 创面给予全厚皮片覆盖, 可以明显增加皮片的耐磨性和患者的舒适性。 而创面较深的患者以前常规的治疗方法是皮瓣移植填充缺损, 此方法需要增加另一处创面对患者的创伤较大,通过使用VSD 治疗后,可以使创面肉芽组织生长较好, 大大减少用皮瓣移植填充缺损的可能。本研究中所有的创面经VSD 治疗后,均可通过全厚皮片移植覆盖创面, 也进一步验证了VSD 对糖尿病难愈创面肉芽组织生长明显的促进作用。
本研究发现VSD 联合PRP 凝胶组的患者在提高创面愈合质量和缩短创面愈合的时间方面明显高于对照组,这与PRP 具有促进细胞增殖、重建微循环和抗感染等作用有关, 观察组中有1 例患者植皮术后的效果为无效,因为此患者的年龄偏大(79 岁),糖尿病的病史较长(20 年),因饮食较随意导致血糖水平不平稳,同时创面的分泌物培养,提示有多重耐药菌感染,多种原因导致的感染控制不理想、植皮后创面愈合差。 观察组中其余患者创面愈合趋势和治疗效果非常好。 本研究结果与王爱等[17]研究结果类似,通过自体PRP 凝胶联合VSD 技术修复烧伤创面,可提高创面愈合率,缩短创面愈合时间,减轻疼痛和瘢痕增生程度。
综上所述, 糖尿病难愈创面的治疗需要多学科多维度的治疗,在对老年或病程较长的患者,应密切观察病情, 合理调节负压值, 避免创面并发症的发生,VSD 联合PRP 凝胶具有协同作用,其效果比单独使用VSD 有更好的提高创面愈合质量和缩短创面愈合的时间,适宜于临床应用。近年来制备PRP 的技术较前有了很大的改进,但制备的方法缺乏标准化、临床的应用缺乏个性化,对此需要进一步深入研究。
