基于标准的高三化学整合教学研究
——由一道江苏高考真题引发的思考
2024-04-18周萍
周 萍
(1.江苏省常州市武进区学校和教师发展中心;2.江苏省前黄高级中学)
1.现状分析——区域调研,发现问题
在区域调研过程中,我们通过深入学校、深入课堂,进行听课交流、走访座谈,发现在高三化学教学中部分教师过于依赖教辅资料,缺乏自己的思考和提炼,也缺乏对课标提出的“增进学科理解”的进一步认识。对于很多老师来说,高三教学主要还是做题、讲题,认为只要研究高考题就足够了。因此呈现出的课堂多数是就题论题,有知识罗列但不成体系,有思路点拨但思维引领不够,有方法归纳但刻板生硬,学生不会迁移应用,也缺乏学习的主动性和积极性,课堂氛围沉闷枯燥。如何构建系统、高效的高三课堂,让学生在深度理解中发展学科思维,在素养提升中实现高三学习再成长,这是我们亟待解决的问题。
2.基于标准的高中化学整合教学
基于标准的高中化学整合教学是指以现行的《普通高中化学课程标准》(2017年版2020年修订)为贯通高中化学教学三级属性(“教什么” “怎么教” “何以教” “谁教” “教谁”)的根本依据,在其现有教学条件下所开展的具有整合性教学品质和特定系统性教学行为特征的高中化学教学。但也有老师认为基于标准的教学更多体现在高一高二的新授课教学,高三只要用好教辅资料就行了,所以也就存在调研过程中出现的情况。而笔者认为高三化学教学更要在“标准”的指导下进行整合教学,只有贯通三级属性才能立体而形象地呈现教学,追根溯源,反观教学本身,方能发现本质,增进学科理解(增进学科理解的主体既是教师也是学生)。
3.基于一道高考题的剖析与思考
3.1 学生的困惑,教学的起点
【例】(2022年江苏卷,17题节选)氢气是一种清洁能源,绿色环保制氢技术研究具有重要意义。

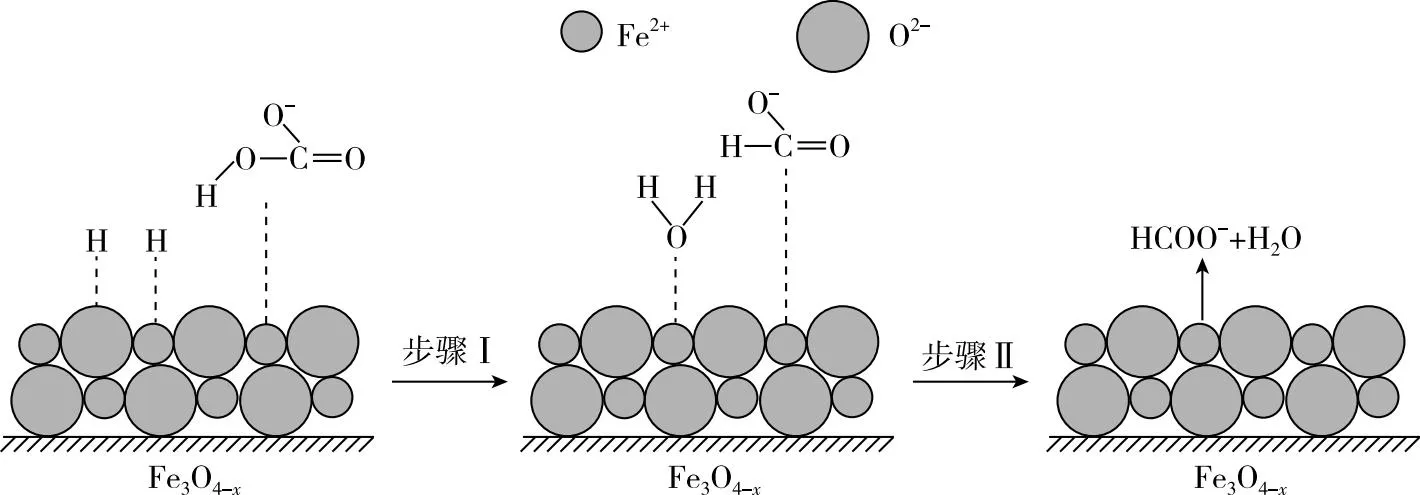
这是一道化学反应机理解析题,不同于以往氧化还原反应机理的考查,而是考查了有机反应中化学键的断裂和形成。学生在之前的训练中已习惯于氧化还原反应机理类型(2021届高考真题)的考查,拿到此题顿觉束手无策,固有的解题模型显然不适用于此,答题过程中慌乱无措。甚至也有老师在问,2021年明明考查的是氧化还原反应机理,我们一直训练了很久,学生对此类题型也已了然于心,怎么2022年考查的却是有机反应类型的,难道方向又变了?殊不知,“变”已成为新高考的一大特点,近年来新高考试题的灵活性与变化性日益明显,光用单一的、机械的方式去搞“对点训练”,去总结所谓的“答题规律”,然后再让学生记忆性地去“套用方法”,已经不适应新的高考政策,更不符合国家对优秀人才、创新人才的选拔要求。
3.2 基于标准,反思教学
思考1:真的束手无策吗?

思考2:真的很陌生吗?
找标准:首先还是找到教学的依据,也是考查的依据——课程标准。《普通高中化学课程标准》(2017年版2020年修订)在选择性必修课程模块1化学反应原理中就明确要求学生“知道化学反应是有历程的”,增加对化学反应历程的认识,有利于学生从微观层面深入理解化学反应的过程和本质,从而深刻揭示化学反应的规律,有针对性地对化学反应进行调控。在选择性必修课程模块3有机化学基础中,也明确要求“引导学生建立‘组成、结构决定性质’的基本观念,形成基于官能团、化学键与反应类型认识有机化合物的一般思路”,并且在内容要求和学业要求上作了进一步细化(如表1)。这为我们的教学指明了方向,也提出了要求。
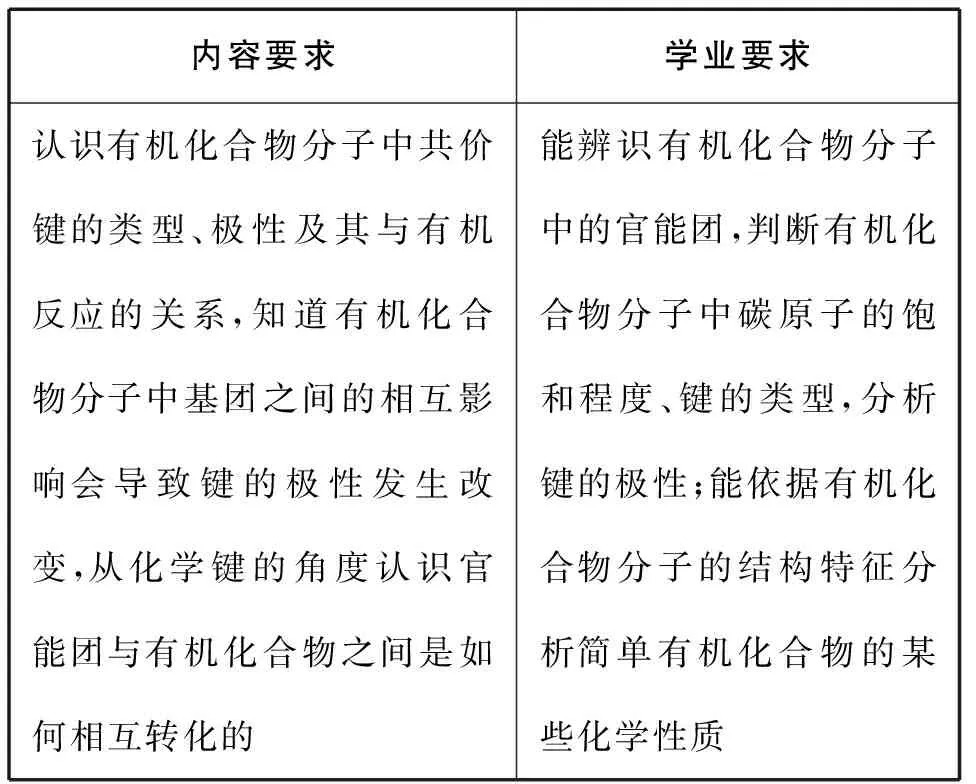
表1
找关联:对有机化学中化学键的断裂和形成机理有了涉及,那么以往教学中是否也有类似情形,而我们的教学又是否到位,是否能让学生产生知识关联,发散思维视角,从而建构对这类问题的整体认识,这就需要我们在高三复习中进行整合教学,这是建立在高一高二教学基础上的再整合。
教学片段一——苏教版必修第一册“电解质溶液”(氯化钠在水溶液中电离生成水合离子的过程)(P19)、苏教版选择性必修1《化学反应原理》“强电解质和弱电解质”(P80)。
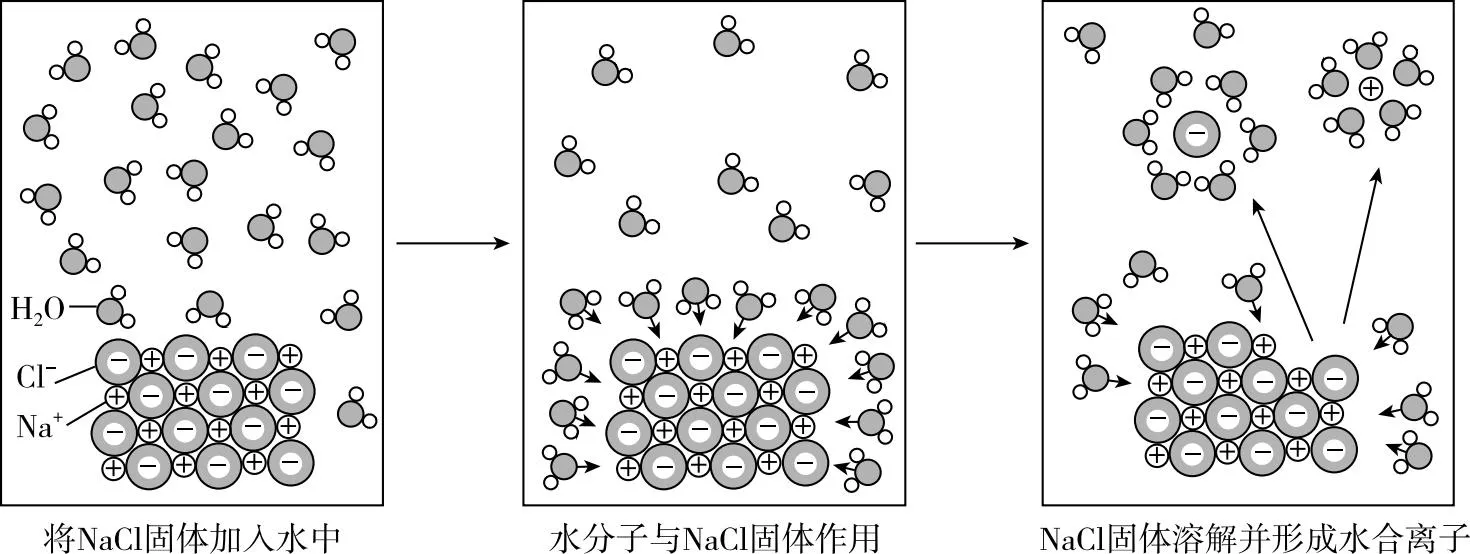
(图片摘自人教版化学必修第一册第二节离子反应“电解质的电离”第14页)
NaCl固体加入到水中后,在水分子作用下,Na+和Cl-脱离NaCl固体表面,由于电负性O>H,水分子中氧原子略带负电,主要进攻Na+,因此形成的水合钠离子氧原子向内,氢原子朝外,而水分子中氢原子略带正电,主要进攻Cl-,因此形成的水合氯离子氢原子向内,氧原子朝外。高三复习时,我们可以引导学生回归教材,从电负性视角再观氯化钠溶于水时微观世界的变化,体会水分子的真正作用,从而加深对电解质、非电解质、强电解质、弱电解质这一组核心概念的理解和应用。
教学片段二——苏教版必修第一册“分子间作用力”(P131)、选择性必修2《物质结构与性质》“氢键”(P79)。
水蒸发是什么变化?蒸发时水分子既然没有断裂化学键,那为什么需要吸收能量?呈电中性的水中到底存在着怎样的作用力?相比于同主族氢化物、分子量更大的H2S,这种作用力有何不同,它是如何形成的?会引起物质性质的哪些变化,能否解释水结成冰体积膨胀、水与酒精任意比互溶这些现象?相比于同周期的氢化物HF,哪个氢键更强,如何解释液体氟化氢的蒸发热比水的蒸发热低这一现象?一连串的追问,不仅能突出对“分子间作用力”这一核心概念的复习教学,还能促进学生对“氢键”的深层思考,思考其形成过程、形成条件,学会从电负性、原子半径、静电作用等视角分析思考、拓展应用,真正理解“氢键”不是化学键,也不同于普通的分子间作用力,充分体现结构对性质的决定作用。
教学片段三——苏教版选择性必修2《物质结构与性质》“元素电负性的周期性变化”P40—42。
新教材(苏教版)在“元素电负性的周期性变化”教学中设置了“批判性思维”这一栏目,促进学生对“电负性”的本质理解,发展学生的高阶思维能力,教师在平时的教学中要充分利用好这些资源,领悟其背后承载的教育价值。


教学片段四——苏教版选择性必修2《物质结构与性质》“配合物的形成和应用”P107—113。

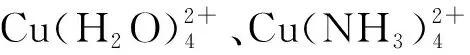
教学片段五——问题解决[2022年江苏卷,15题节选“设计合成路线”、人教版选择性必修3《有机化学基础》第三节“醛 酮”中的“乙醛”(P67)]。
15.(15分)化合物G可用于药用多肽的结构修饰,其人工合成路线如下:
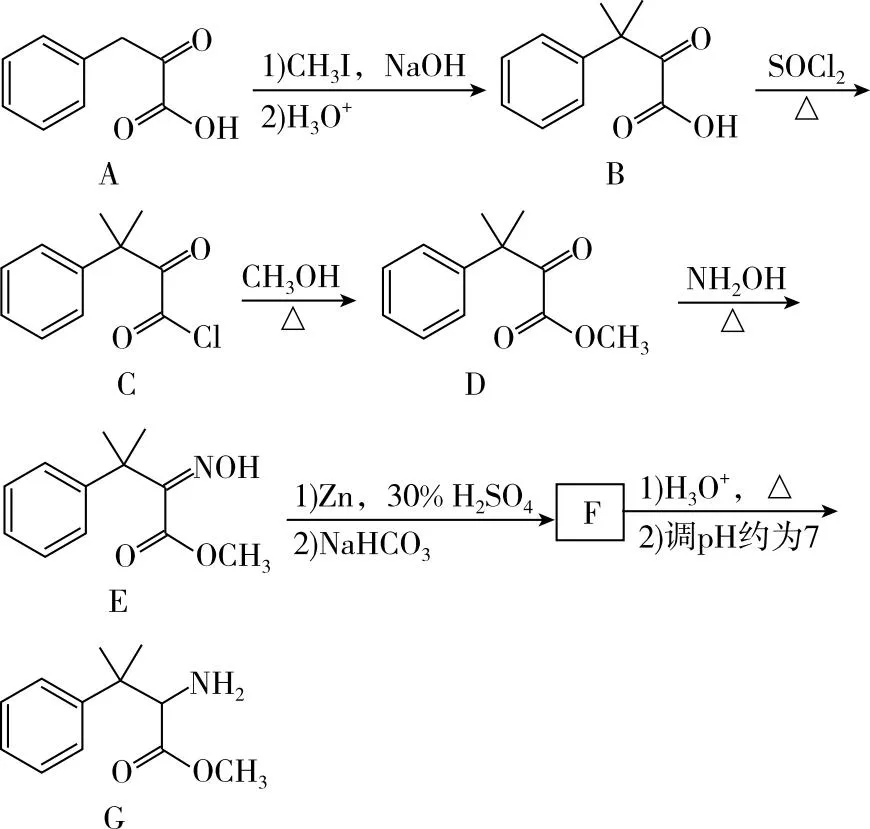
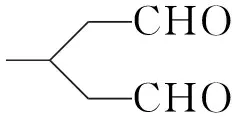
解题的关键是要看懂信息中第二个反应的反应机理,即“羰基与α-H加成问题”。在人教版选择性必修3《有机化学基础》第三节“醛 酮”中就出现过乙醛与HCN加成反应的机理。在上述的合成路线设计中,丙酮的碳氧双键同样存在类似情况,明白这一点,学生就能切入要点进行快速解题。丙酮中氧原子电负性较大带部分负电荷,碳原子带部分正电荷,当与另一个丙酮分子α-H发生加成反应时,带正电的α-H就连接在氧原子上,余下的带负电的原子团就连接在碳原子上,然后发生消去反应。实际在信息的第一个反应中也存在着因电负性差异对化学键极性产生的影响,CH3MgBr中C—Mg键断裂,带正电的MgBr和氧原子结合,带负电的CH3和醛基上的碳原子结合,然后O—MgBr键断裂,带负电的氧原子和H+结合形成羟基。
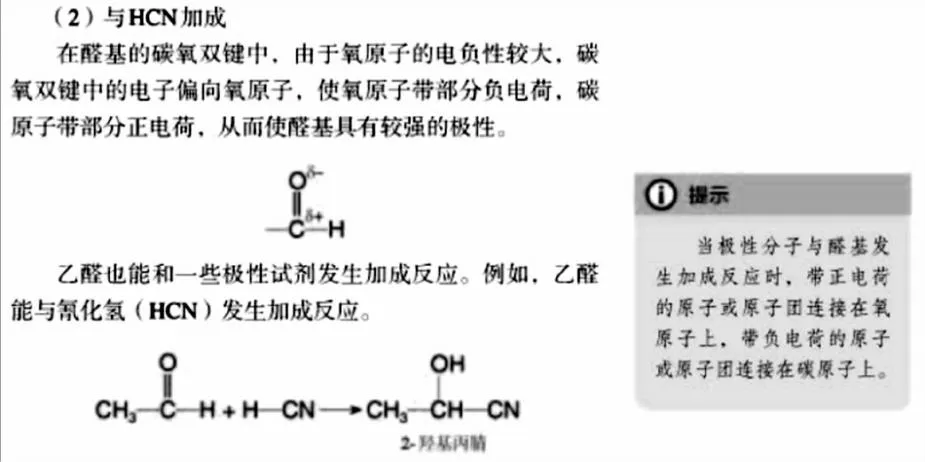
(图片来自人教版选择性必修3《有机化学基础》第三节“醛 酮”第67页)
4.高三化学教学建议
通过对必修和选择性必修教材相关内容的整合教学,不仅让学生更深刻地理解核心概念,更能帮助学生打开视角,学会融会贯通、迁移应用。
课标指出,开展基于学生学科核心素养发展的课堂教学,要求教师进一步增进学科理解。化学学科理解是对学科知识及其思维方式和方法的一种本原性、结构化的认识,它不仅仅是对化学知识的理解,还包括对具有化学学科特质的思维方式和方法的理解。学科理解的直接目的是提升教师的专业素养,终极目标却是发展学生的学科核心素养,因此增进学科理解的主体既是教师也是学生。唯有理解本质,掌握方法,发展学科思维,形成学科观念,才能在变化莫测的高考中有所突破,助力学生的可持续发展。
4.1 重视试题的深度剖析与纵向挖掘,由单一问题向整体建构转化
高考试题对一线教学有引领作用,研究真题是每一位老师的必修课。很多高考试题为我们提供了研究问题的新角度与新思路,揭示了物质变化中更本质和更微观的含义,有的和国家优秀的传统文化相关,有的和先进的工艺生产相关,有的体现了药物研究的最新成果,有的凸显了科技前沿的新发现和新成果,彰显了育人理念和学科价值,具有很好的示范意义。总结试题的基本模型与设问角度,厘清试题问什么?为什么这样问?试题的核心指向是什么?问题的内在关联在哪里?对复习教学的启示是什么?有哪些认识视角?如何利用好正逆向思维、对比思维等方法策略指导学生作答?才能建构对试题的整体认识,提升反思意识,激活复习思路。
4.2 合理设计组织结构化教学内容,由学科知识向学科理解转化
不局限于题目本身,而是将知识点的理解和关键能力的培养渗透于高一必修、高二选择性必修以及高三的复习教学中,注重知识关联,强化学科理解,提升核心素养。尤其在高三复习教学中,不能只是对原有知识的简单再现,应更加注重知识点或核心概念的整合教学,由点及面,贯穿一条主线(主题式教学),进行情境创设、任务布置、问题解决的整体设计。以思维发展为导向,开展分类与概括、证据与推理、模型与解释、符号与表征等具有学科特质的高阶思维学习活动,深化认识视角,构建结构化认识思路,引领学生思维能力的整体发展。
江苏省教育科学“十四五”规划课题“基于标准的高中化学整合教学研究”(课题编号:D/2021/02/171)的研究成果之一。
