提高硝酸胍得率的工艺研究
2024-04-10余晓红
*余晓红
(浙江正鑫新材料有限公司 浙江 321004)
引言
硝酸胍化学名:二氨基硝酸胍,英文:Guanidine nitrate。分子式CH6N4O3或CH5N3·HNO3,分子量:122.08。品种有:硝酸胍、精制硝酸胍、专用超细硝酸胍、试剂型等。硝酸胍不仅在化工工业中应用广泛,在医学、农业及一些高科技产业也有重要作用。如硝酸胍是一种良好的产气剂,而且是一些化合物的重要中间体,是良好的硝化剂、添加剂、沉淀剂,也可作为汽车安全气囊新材料[1],医学上可用于合成盐酸洛氟普啶[2]等药物,火箭推进剂、油漆工业、照相材料、消毒剂等领域。硝酸胍也可作为一种多用途化工原料产品,是生产磺胺脒、磺胺嘧啶等药物的重要中间体,硝酸胍在农药上不仅是杀虫剂吡虫啉[3]的原料,用于合成下一步中间体硝基胍,还可用作多种磺酰脲类除草剂的中间体以及用于制造混合炸药,如浇铸、螺装、塑料粘结炸药[4]等;可作为染料敏化太阳能电池电解液的有效添加剂[5];可作仲钨酸B-胍盐沉淀法分离钨钼的良好沉淀剂[6];可以合成一种新型的胍基比色荧光双希夫碱化学传感器L。随着医药和农药工业的迅速发展,目前国内对硝酸胍的需求越来越大,它不仅用于国内工业的生产,还可用于出口,因此发展前景良好。
硝酸胍为白色结晶粉末或颗粒,是一种有机强碱,属强氧化剂,具有中等毒性,熔点217℃;能溶于甲醇、乙醇和水,不溶于丙酮、苯、乙醚;pH呈中性;因为它是强氧化剂,在受热、接触明火或者受到摩擦、震动、撞击后可能发生爆炸;与硝基化合物和氯酸盐组成的混合物对震动及摩擦敏感,也会发生爆炸[7];并且在高热分解后会产生有毒的燃烧产物—氮氧化物[8]。
针对硝酸胍的生产,各国的生产方法不尽相同,美国和日本多采用双氰胺法,德国采用直接法由氨基氰作为原料直接制得,其中双氰胺法为传统工艺合成路线的主要方法,产率高;尿素法是在双氰胺法的基础上发展起来的,使用尿素代替双氰胺制备,较双氰胺法原料易得、成本低,但是存在不良反应影响硝酸胍的制备。另外,还有可在微通道中连续流合成硝基胍的方法,氰胺钙法等。目前国内较为成熟的几种硝酸胍生产工艺路线有双氰胺法、尿素法、BAF法等[9],对比上列三种工艺路线,双氰胺法反应条件最易达成,且无副产物,后处理最为简便,相较于尿素法及BAF法,成本较低,故本文选择工艺较为稳定的双氰胺法作为研究方案。
1.试验部分
所用原材料:双氰胺(工业级)、硝酸铵(工业级)、氢氧化钠(工业级)、苦味酸(工业级)、甲醛(工业级)、液氨(工业级)等。
2.实验内容
(1)合成工艺。双氰胺法合成硝酸胍的工艺路线,反应分两步进行,反应式为:
在第一个反应器中加入一定比例的双氰胺与硝酸铵,加热至一定温度,至熔融状态,保温反应一段时间,然后导入第二个反应器,继续加等量的硝酸铵,加热至一定温度,中间产生的氨气由排气阀输送至回收瓶中回收,反应一定时间后,可倒入冷凝烧杯(宽且浅的烧杯,加快冷却效率,必要时可用风扇降温),降温至25℃左右冷却凝结,即可获得产品硝酸胍。
(2)产品指标及检测。硝酸胍产品质量按HG/T 3269—2022要求应符合表1要求。

表1 硝酸胍产品质量指标
检测方法:
①含量的测定方法是在碱性条件下,硝酸胍与苦味酸生成苦味酸胍沉淀,称重即可计算硝酸胍的含量。
②加热减量的测定方法是取一定量的硝酸胍称重后置于105~110℃烘箱中烘2.5h,然后冷却称重,干燥前后的质量之差为加热减量。
③水不溶物。水不溶物是硝酸胍测定的一项重要的质量指标,采用溶解、过滤、烘干等方式检测。
④游离硝酸的测定方法是取一定量的硝酸胍,加入蒸馏水后加热溶解,冷却至室温,用氢氧化钠标准溶液滴定测量。
⑤游离硝酸铵的测定是依据硝酸铵与甲醛生成六次甲基四胺,过程中反应生成硝酸,再用氢氧化钠滴定即可测量。
3.结果与讨论
(1)原料配比对得率影响。在硝酸胍粗品的生产过程中,双氰胺与硝酸铵两者之间比例的不同,会影响到最后硝酸胍的得率有所不同。在设定其他三种反应条件都为最优情况,只改变原料的配比,测定在不同配比的情况下,得到不同得率硝酸胍,如表2所示。
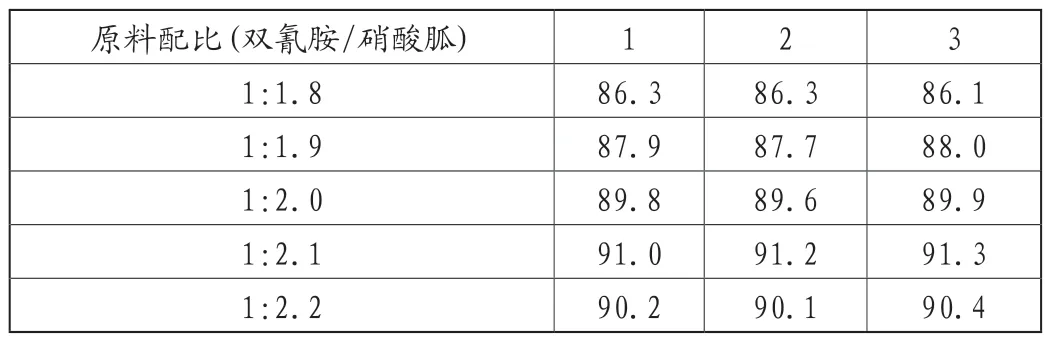
表2 原料配比不同对硝酸胍得率的影响(单位:%)
由表2可知,原料配比的不同会对硝酸胍最后的得率带来影响,且出于经济效益的考虑,在原料配比为1:2.1时,硝酸胍的得率最高,即硝酸铵稍微过量,有利于提高硝酸胍的得率。因此,经过实验优选,双氰胺与硝酸铵之间的配比以1:2.1较合理。
(2)升温方式对得率影响。用双氰胺法制硝酸胍时,升温方式的不同也有可能会影响到最后产品得率。因此,先设定其他条件都为最优时,然后分别以分段升温和一步升温的方法进行试验,其中分段升温分为两步,第一步为升温至100~105℃,并保温半小时,使双氰胺与硝酸铵混合物全部熔融,第二步再升温至200~210℃,使之反应;一步升温法为直接升温至200~210℃进行反应,然后探究这两种升温方式对硝酸胍最终得率的影响,如表3所示。

表3 升温方式对硝酸胍得率的影响(单位:%)
由表3可知,在设定其他反应条件不变时,分段升温法具有较高的得率。
(3)反应温度对得率影响。因已确定采用分段升温法,因此讨论反应温度只需改变第二步反应温度即可,设定其他条件不变时,探究反应温度对硝酸胍的率的影响,如表4所示。
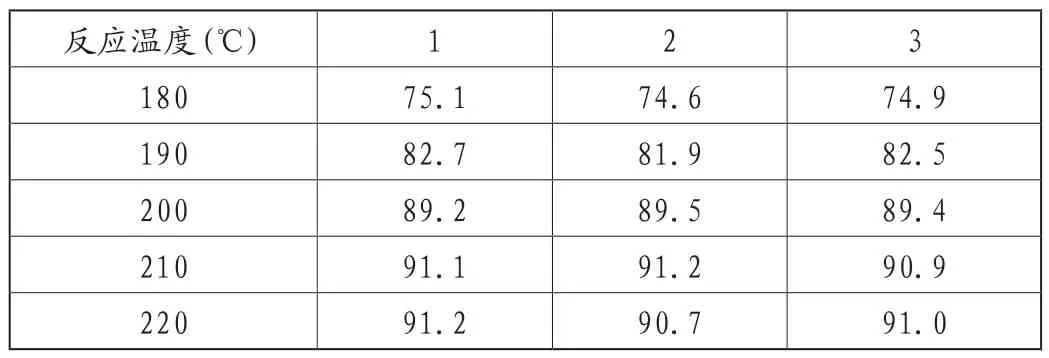
表4 反应温度对硝酸胍得率的影响(单位:%)
由表4可知,在反应温度为180~200℃之间,硝酸胍的得率有较为显著的提升;在210~220℃时,硝酸胍的得率没有明显的变化,因此,出于经济效益的考虑,反应温度优选在200~210℃之间。
(4)反应时间对得率影响。因为采用的是分步升温法,因此要分开讨论第一步升温的反应时间及第二步升温的反应时间,并且设定其他反应条件不变情况下,探究反应时间对最终硝酸胍得率的影响,第一步反应时间的影响如表5所示。
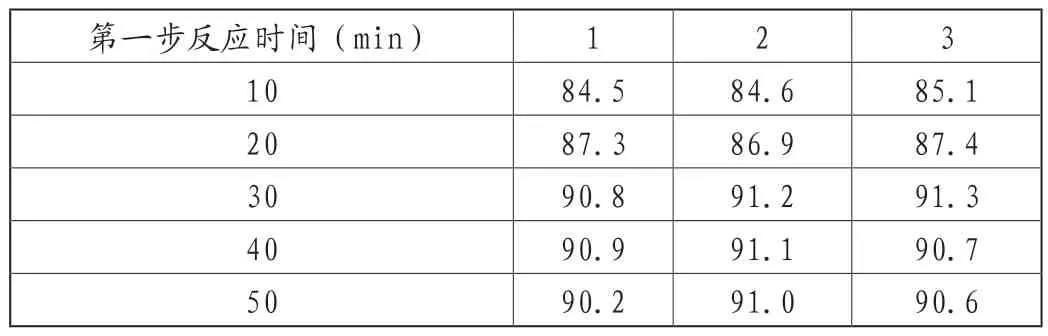
表5 第一步反应时间对硝酸胍得率的影响(单位:%)
由表5可知,第一步反应时,反应时间在10~30min时,最终硝酸胍的得率有明显的提升;在30~50min时,硝酸胍的得率不再有较大的变化,因此,第一步反应时间优选为30min左右。
第二步反应时间对硝酸胍得率的影响如表6所示。

表6 第二步反应时间对硝酸胍得率的影响(单位:%)
由表6可知,在第二步反应时,反应时间在20~60min之间时,硝酸胍的得率有较大的提升;在60~90min时,硝酸胍的得率较为稳定,无明显变化。因此,第二步反应时,反应时间优选为60~70min之间。
(5)外加氨气对得率影响。在确定上述合成方式后,本研究又采用外加氨气和不外加氨气对得率是否影响进行实验;外加氨气来源是用液氨气化后从低部通入反应瓶中,采用开始反应就连续通入,后期通入、不通入氨气对得率情况进行比较实验;实验设定其他条件不变时,探究氨气通入是否能提高硝酸胍得率进行实验,结果如表7所示。
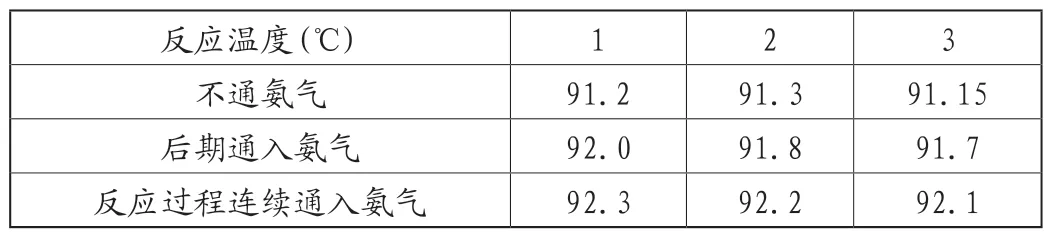
表7 氨气通入对硝酸胍得率的影响(单位:%)
由表7可知,反应过程连续通入氨气,硝酸胍的得率有较为显著的提升,可以达到92.3%,因此,为了获得较高的硝酸胍得率采用反应过程连续通入氨气的方式来得到。
(6)验证实验。在确定上述合成方式后,本研究又对上述确定的实验条件进行重复验证实验,验证实验条件如下:原料双氰胺与硝酸铵之间的配比为1:2.1~2.2,以分段升温法进行反应,第一步反应温度为100~105℃,反应时间为30~40min左右,第二步反应温度为200~210℃,反应时间为60~70min,采用开始反应就连续通入氨气对得率情况进行验证实验,结果如表8所示。

表8 验证实验硝酸胍得率(单位:%)
由表8可知,实验得到的硝酸胍得率全部大于92%,最高能达到92.3%,满足实验的要求,也证明所得的反应条件满足硝酸胍得率的要求。
4.结论
本文以双氰胺和硝酸铵作为原材料来合成硝酸胍,从原料配比、升温方式、反应温度及反应时间四种反应条件作为研究对象,通过试验看出:原料双氰胺与硝酸铵之间的配比为1:2.1~2.2,以分段升温法进行反应,第一步反应温度为100~105℃,反应时间为30~40min左右,第二步反应温度为200~210℃,反应时间为60~70min,可得硝酸胍最终的得率为91.3%,采用开始反应就连续通入氨气工艺,结果表明是合成硝酸胍得率较高的一条工艺路线。
