多囊卵巢综合征患者程序性细胞死亡因子4表达及睾酮与胚胎质量相关性研究*
2024-03-29仇雪梅赵明蕊解晓丽赵淑芹
仇雪梅,赵明蕊,解晓丽,赵淑芹
(枣庄市妇幼保健院生殖遗传中心,枣庄 277100)
多囊卵巢综合征(polycystic ovary syndrome,PCOS)为一高度复杂的内分泌和生殖功能障碍性疾病,其发病率为育龄妇女的5%~10%,是导致无排卵性不育的主要原因。目前PCOS的确切发病机制尚不明确,过多的雄激素可能是引发此病的核心要素之一[1-3]。研究表明,卵巢颗粒细胞凋亡增加与PCOS患者卵泡发育异常密切相关[4-6]。Ding等[7]研究显示,PCOS患者外周血单个核细胞中凋亡相关基因程序性细胞死亡因子4(programmed cell death 4,PDCD4)表达显著增加,PDCD4高表达与颗粒细胞凋亡相关,并可作为PCOS发生的独立危险因素。Lu等[8]认为,PDCD4是治疗代谢性疾病的新靶点。本课题组前期研究显示,高浓度睾酮诱导PDCD4表达上调和卵巢颗粒细胞凋亡[9]。提示PDCD4在颗粒细胞凋亡及PCOS发病风险中的重要性。本研究在外周血细胞和体外研究基础上,探讨控制性超促排卵(controlled ovarian hyperstimulation,COH)中PCOS患者卵巢颗粒细胞中PDCD4表达及其与胚胎质量的相关性,分析血清睾酮(Testosterone,T)水平与胚胎质量的相关性,以期进一步探讨PDCD4及睾酮的临床意义,从而为提高PCOS患者的临床结局提供依据。
1 资料与方法
1.1 研究对象 选取2020年10月至2021年11月在枣庄市妇幼保健院生殖中心行体外受精-胚胎移植(in vitro fertilization-embryo transfer,IVF-ET)助孕的超促排卵周期PCOS患者(28例)和非PCOS患者(40例)。本研究经医院医学伦理委员会批准。依据2003年鹿特丹标准,PCOS的诊断标准为满足以下3个条件中的2个:(1)排卵少或不排卵;(2)有高雄激素血症的临床和生化特征;(3)超声检查见多囊性卵巢。同时排除其他可能导致高雄激素的疾病,如先天性肾上腺皮质增生、分泌雄性激素的肿瘤、Cushing综合征等。非PCOS患者(对照组)纳入标准:月经规律,基础体温测试结果表明有正常排卵,超声检查证实卵巢形态正常,输卵管和(或)男方因素导致的不孕。排除标准:合并卵巢功能早衰、内异症、高泌乳素血症、甲状腺功能异常等;曾行卵巢手术或放化疗;近3个月内接受过促排卵治疗或服用性激素者。
1.2 方法
1.2.1 COH方案 综合评估患者情况,选择适合的常规促排卵方案,包括患者年龄、体质量指数(body mass index,BMI)、窦卵泡数、基础性激素水平及血清抗苗勒管激素(anti-Mullerian hormone,AMH)水平。促性腺激素(gonadotropin,Gn)(果纳芬,75IU/支,默克雪兰诺公司)起始剂量150~225IU/d,并同时监测血清黄体生成素(luteinizing hormone,LH)、雌二醇(Estradiol,E2)和孕酮水平,以调整Gn剂量。B超监测到至少1个卵泡直径≥18mm时,当天肌肉注射人绒毛膜促性腺激素(human chorionic gonadotropin,HCG)(珠海丽珠公司)5000~10000IU,36h后在阴道超声引导下穿刺取卵。
1.2.2 优质胚胎判定 取卵后进行常规授精,根据Veeck胚胎分级标准对胚胎进行分级,第2天细胞数为2~4细胞,第3天细胞数为6~8细胞,Ⅱ级以上(卵裂球大小均等或基本均等,碎片<20%)的胚胎为优质胚胎。
1.2.3 颗粒细胞收集与处理 穿刺卵泡抽取的卵泡液立即于显微镜下观察,拾取卵母细胞-卵冠丘复合物后,将剩余的卵泡液收集于离心管,1500r/min离心10min。弃上清,用PBS清洗1次,用2mL PBS悬起细胞沉淀,用吸管将其加入具有等体积的淋巴细胞分离液中,2500r/min离心20min。小心吸取悬浮子两层淋巴细胞液间的颗粒细胞层,收集于新的离心管内,加5mL PBS溶液清洗,1500r/min离心5min。PBS清洗3次,-80℃冰箱冻存备用,用于相关指标检测。
1.2.4 逆转录与实时定量PCR 颗粒细胞总RNA使用Trizol(Invitrogen Corporation,美国)进行提取。按逆转录试剂盒(PrimeScriptTMRT-PCR Kit,TakaRa,中国)说明书进行cDNA合成。实时荧光定量PCR(Real-time Quantitative PCR,qPCR)法应用SYBR Premix Ex TaqTM试剂盒(TakaRa,中国)对PDCD4 mRNA表达进行定量分析。3-磷酸甘油醛脱氢酶(glyceraldehyde-3-phosphate dehydrogenase,GAPDH)为内参,各组mRNA相对表达量应用2-△△Ct方法计算。基因扩增引物序列:PDCD4正向引物5'-TGGATGAAAGGGCATTTGAGA-3',反向引物5'-AGCCTTCCCCTCCAATGCTA-3',目标扩增片段大小为164bp;GAPDH正向引物5'-GCACCGTCAAGGCTGAGAAC-3,反向引物5'-TGGTGAAGACGCCAGTGGA-3',目标扩增片段大小为138bp。所有引物均由南京金思特公司合成。
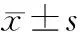
2 结 果
2.1 患者一般情况及实验室结局 PCOS组和对照组的年龄、不孕年限、BMI、基础促卵泡激素(follicle stimulating hormone,FSH)、雌二醇(Estradiol,E2)、泌乳素(Prolactin,PRL)和睾酮比较,差异无统计学意义(P>0.05)。PCOS患者的AMH和基础LH水平均高于对照组,差异有统计学意义(P<0.05)(表1)。两组的Gn用量、Gn时间和HCG注射日子宫内膜厚度比较,差异均无统计学意义(P>0.05)。PCOS组的HCG注射日E2值高于对照组,差异均有统计学意义(P<0.05)。两组的正常受精率、卵裂率、优胚率、可用胚率和卵母细胞利用率比较,差异均无统计学意义(P>0.05)。见表2。

表1 PCOS组和对照组基本临床资料比较

表2 PCOS组和对照组IVF-ET治疗结局比较
2.2 PCOS患者卵巢颗粒细胞PDCD4表达 实时定量PCR法检测结果显示,PCOS组的PDCD4表达略高于对照组,差异无统计学意义(P=0.804)。见图1。对照组与PCOS组的平均获卵数分别为(15.3±3.3)和(19.6±2.1)。对照组以组内获卵数均值(15.3)为分界,分为获卵数≤15组和获卵数>15组。PCOS组获卵数组内差异较小,未进行亚组分析。结果显示,获卵数较多的对照组(获卵数>15组)及PCOS组的PDCD4相对表达量高于获卵数少的对照组(获卵数≤15组),但差异无统计学意义(图2)。
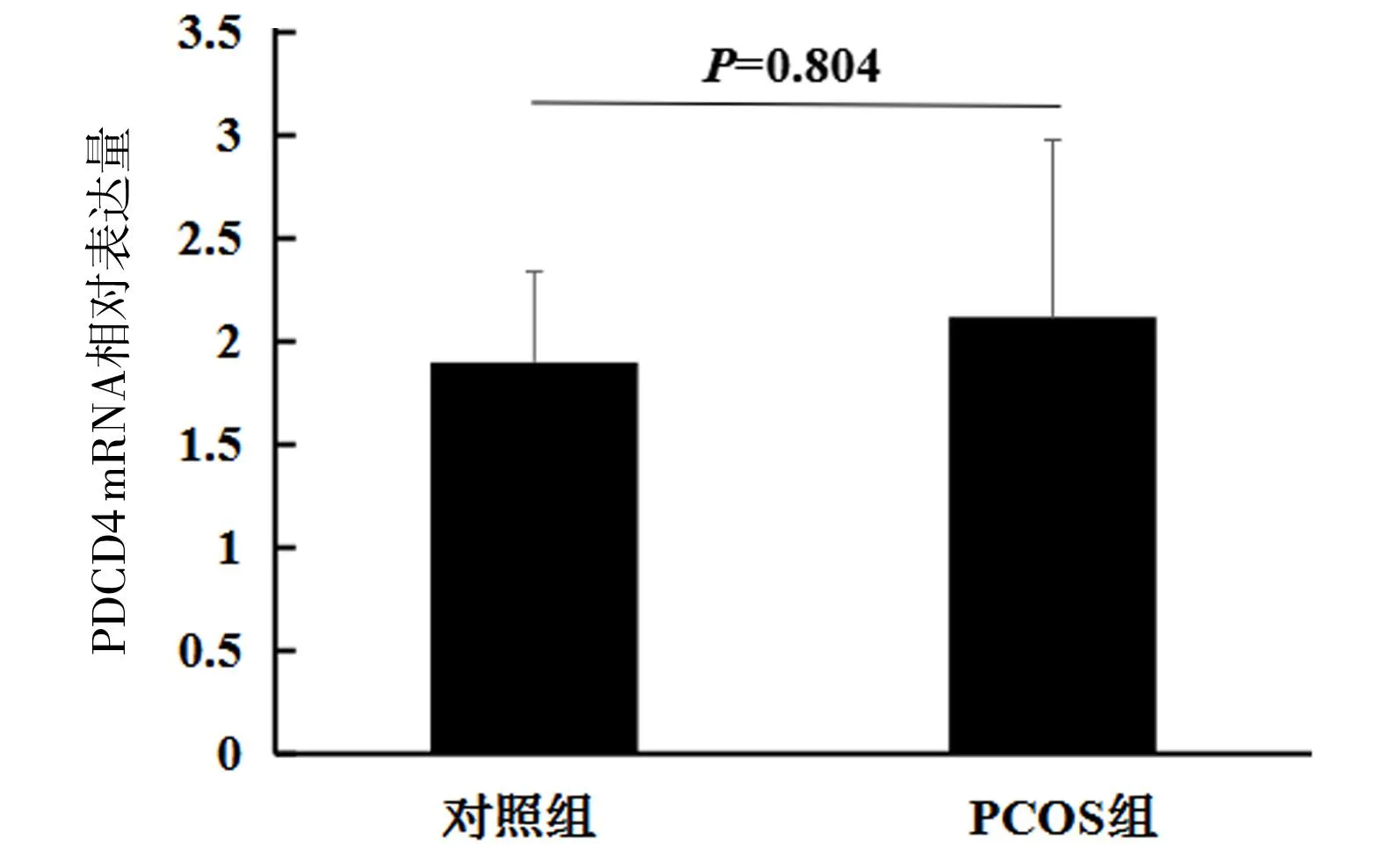
图1 qPCR检测PCOS组和对照组PDCD4 mRNA表达水平
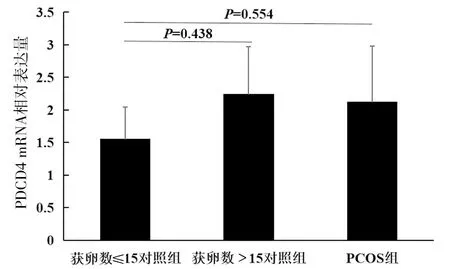
图2 qPCR检测不同获卵数各组PDCD4 mRNA表达
2.3 PDCD4表达与胚胎质量相关性分析 根据患者可用胚率分为低可用胚组(可用胚率低于30%)和正常可用胚组。结果显示,低可用胚组的PDCD4表达高于正常可用胚组,差异有统计学意义(P=0.044)。见图3。

图3 qPCR检测PDCD4 mRNA表达
2.4 睾酮水平与胚胎质量相关性分析 PCOS患者根据血清睾酮水平分为T<0.7ng/mL组(22例)和T≥0.7ng/mL组(6例)。结果显示,高睾酮水平组的正常受精率和卵母细胞利用率低于低睾酮水平组,差异有统计学意义(P<0.05)。见表3。
3 讨 论
PCOS是一种病因复杂的疾病,一般认为其病因与下丘脑-垂体-卵巢轴调节紊乱有关。下丘脑以脉冲的方式分泌促性腺激素释放激素,脉冲的幅度增大导致患者血液中黄体生成素异常增高,从而促进雄激素的合成和分泌[10]。而FSH分泌被抑制,导致雄激素无法充分转化为雌激素,雄激素的进一步升高阻碍卵泡发育、封闭卵泡,堆积的发育不全的小卵泡导致卵巢形成多囊样改变,无法正常排卵。AMH是一种由卵泡颗粒细胞分泌的激素,其在调节卵泡发育过程中起着重要作用,与卵巢储备功能密切相关。PCOS患者中AMH表达明显升高,可用于PCOS的诊断及疗效评估[11-12]。本研究中PCOS组与对照组的年龄、不孕年限、BMI、基础FSH、E2、PRL和睾酮比较,差异均无统计学意义,PCOS患者的AMH和基础LH均高于对照组,这与以往关于PCOS的研究相符。
Eini等[13]研究表明,高雄激素血症可能通过影响芳烃受体途径损害卵母细胞的发育能力。PCOS患者通过辅助生殖技术可产生形态正常的MⅡ卵母细胞,但卵母细胞发育能力和胚胎发育潜力受到损害[14]。辅助生殖技术中PCOS患者能否获得与健康人相当的妊娠结局,目前研究结果并不一致,有不少研究报道了COH中PCOS与非PCOS患者临床结局的差异。吴晓燕等[15]研究表明,PCOS组的胚胎种植率、临床妊娠率低于对照组;赵考考等[16]研究显示,PCOS患者的获卵数、正常受精数高于对照组,组间优质胚胎数、着床率、临床妊振率差异无统计学意义;黄剑磊等[17]研究表明,PCOS组的卵母细胞成熟率、正常受精率、可用胚胎数、可用胚胎率、囊胚形成率均低于对照组。本研究结果显示,PCOS组与对照组的正常受精率、卵裂率、优胚率、可用胚率和卵母细胞利用率均未见明显差异;根据睾酮水平进行亚组分析发现,高睾酮水平组的正常受精率和卵母细胞利用率低于低睾酮水平组,表明睾酮水平对卵子及胚胎质量影响的重要性。以往研究结果不一致可能与睾酮水平不同有关。
颗粒细胞环绕于卵母细胞周围,向卵母细胞供应必要的营养物质和生长因子,对于卵母细胞的生长发育至关重要,与PCOS卵泡发育异常及该疾病的多种表征有着紧密联系。虽然结论尚未得到证实,但多项研究显示,PCOS患者卵泡发育障碍可能与卵巢颗粒细胞凋亡增加有关。PDCD4基因是在细胞凋亡中因一种表达特异的蛋白质而鉴别出来的凋亡促进基因。PDCD4在其确切的细胞作用方面存在一些差异,但其通常被表征为一种抑制细胞周期进展和增殖并促进细胞凋亡的蛋白质。最近研究表明,PDCD4是PCOS发病机制的新参与者[18],其作为miR-16[19]、miR-155[20]及miR-323-3p[21]的靶基因可抑制卵巢颗粒细胞增殖并促进细胞凋亡。推测PDCD4可能通过影响卵巢颗粒细胞的增殖及凋亡在PCOS的发病机制中发挥作用。但是,卵巢颗粒细胞中PDCD4的表达情况尚不清楚。通过对PCOS患者和健康人的外周血单核细胞进行研究,Ding等[7]发现PCOS患者中凋亡相关基因PDCD4表达显著上升。廉红梅等[22]研究显示,PCOS患者血清PDCD4表达高于对照组。本课题组前期研究结果表明,高浓度睾酮导致PDCD4表达增加[23]。本研究结果显示,PCOS组与对照组的PDCD4表达无明显差异,可能与两组睾酮水平相当及样本量太小有关。PCOS患者颗粒细胞中PDCD4表达情况尚需进一步增加样本量进行研究证实。本研究结果显示,低可用胚组的PDCD4表达高于正常可用胚组,差异有统计学意义,表明颗粒细胞PDCD4表达对胚胎质量有一定的影响。
综上所述,COH中卵巢颗粒细胞PDCD4高表达与低可用胚率相关,睾酮水平与受精率和卵母细胞利用率密切相关,睾酮水平升高,受精率和卵母细胞利用率降低。这一结论对于如何改善PCOS患者助孕结局提供了线索。
