接受母婴阻断治疗的慢性HBV感染孕妇产后肝炎发作的风险预测模型构建*
2024-03-29刘耀丹
刘耀丹,刘 敏
(上海市公共卫生临床中心妇产科,上海 201508)
乙肝母婴传播(mother-to-child transmission,MTCT)占乙型肝炎病毒(hepatitis B virus,HBV)新发感染的40%~50%,是HBV感染的主要原因[1]。目前通过乙型肝炎疫苗与乙型肝炎免疫球蛋白联合作为预防策略的总体有效率可达到90%~95%,然而,感染HBV孕妇所生婴儿中仍有10%出现乙肝病毒感染[2]。对于乙型肝炎e抗原(hepatitis B e antigen,HBeAg)阳性和高病毒载量的孕妇,妊娠中、晚期使用核苷类似物(nucleostide analogues,NAs)抗病毒治疗可进一步减少MTCT[3],但产后可能出现肝功能异常[4-5],且产后发作率高于妊娠期[6]。对于以母婴阻断为目的进行抗病毒的孕产妇,产后肝炎发作风险目前尚无明确的预测方法。本研究旨在检测慢性HBV感染孕产妇在不同时期肝功能、乙肝表面抗原(hepatitis B surface antigen,HBsAg)、乙肝e抗原(HBeAg)、乙肝病毒脱氧核糖核酸(hepatitis B virus deoxyribonucleic acid,HBV DNA)、血清乙型肝炎病毒核心相关抗原(hepatitis B core-related antigen,HBcrAg)等相关指标,探讨慢性HBV感染孕产妇在乙肝抗病毒治疗产后肝炎发作风险的危险因素,并构建风险预测模型,为临床实践中以孕期母婴阻断目的抗病毒用药者产后的随诊和抗病毒方案提供参考。
1 资料与方法
1.1 研究对象 选取2020年1月至2022年10月在上海市公共卫生临床中心产检及分娩的223例慢性乙肝感染孕产妇,定期随访至产后48周。本研究纳入标准基于《慢性乙型肝炎防治指南(2019版)》[7]和《乙型肝炎病毒母婴传播预防临床指南(2020版)》[8],结合指南中孕产妇MTCT抗病毒标准:(1)HBV DNA定量水平>2×105IU/mL,血清HBsAg水平>1×104IU/mL,HBeAg阳性,血清丙氨酸氨基转移酶(alanine aminotransferase,ALT)和血清天冬氨酸氨基转移酶(aspartate transaminase,AST)持续正常,肝纤维化超声无异常;(2)孕期行抗病毒治疗预防MTCT。排除标准:(1)接受慢乙肝活动性肝炎抗病毒治疗的患者;(2)合并其他嗜肝病毒感染、HIV病毒感染、肝硬化和其他妊娠相关肝病(如妊娠期肝内胆汁淤积)的患者。本研究方案获上海市公共卫生临床中心伦理委员会批准(批准号:2020-S224-02号)。
1.2 研究方法
1.2.1 观察指标 本研究为前瞻性观察性研究,将符合纳入标准的以母婴阻断为目的的慢性HBV感染的孕妇纳入观察组,通常为产后6周停药(其中19例患者于产后当天停药)。根据患者产后48周随访结果分为停药后肝炎发作组和未发作组(对照组)。于妊娠早中期、妊娠晚期、产后(6±1)周、(12±2)周、(24±2)周、(36±2)周及(48±2)周随访检测肝功能、HBV DNA、乙肝五项情况,以及抗病毒当日的血清HBcrAg定量水平。产后6周随访时,如发现ALT≥2×正常值上限(upper limit of normal,ULN)或HBV DNA较基线下降≥3 lgIU/mL和/(或)HBeAg较基线下降≥50%的患者则建议继续抗病毒治疗,定期随访至产后48周。不符合上述条件者则于产后6周停药,停药随访过程中出现ALT≥2×ULN且HBV DNA≥2×104的患者也建议抗病毒治疗,并继续随访至产后48周。
1.2.2 结局评价标准 将产后肝炎发作定义为在妊娠期及产后48周内ALT≥2×ULN,且排除药物性肝损伤、非酒精性脂肪肝病等。
1.2.3 实验室检测方法 收集患者在抗病毒当日空腹静脉血样本3mL于黄头促凝管内,6h内1000g/min离心15min获取血清,-80℃保存。采用ELISA酶联免疫分析试剂盒(上海赛培森生物科技公司)和Multiskan FC酶标仪检测HBcrAg水平。采用Roche Light Cycler 480 qPCR系统检测HBV DNA水平,检测范围(50~2)×109IU/mL。采用Abbott Architect C16000全自动生化分析系统检测肝功能指标,将ALT的ULN定义为40U/L。采用微粒子酶免疫法和Abbott Architect I2000全自动生化分析系统检测HBsAg、HBeAg,其中HBsAg检测范围0.05~250IU/mL,HBeAg检测下限为1.0SCO。

2 结 果
2.1 入组队列随访及产后肝炎发作情况 223例慢性HBV感染孕妇纳入原始队列,其中198例孕妇同意在孕28周使用NAs抗病毒进行母婴阻断入组(替诺福韦酯151例,替比夫定47例)。19例患者因口服替比夫定且要求母乳喂养,于产后当天停药。随访过程中有80例(40.40%)患者失访,余118例均规范随访至产后48周。
产后48周内患者ALT异常率30.81%(61/198),其中肝炎发作比例为20.20%(40/198),ALT≥10×ULN者5例(2.53%)。在产后(6±1)周、(12±2)周、(24±2)周、(36±2)周及(48±2)周肝炎发作比例分别为14.65%(29/198)、4.08%(6/147)、2.61%(3/115)、2.02%(2/99)、0%(0/87)。产后(6±1)周肝炎发作比例与其它4个随访节点相比,差异均有统计学意义(P=0.0034、0.0014、0.0016、<0.0001)。5例ALT≥10×ULN患者中均发生在产后6周。见图1。
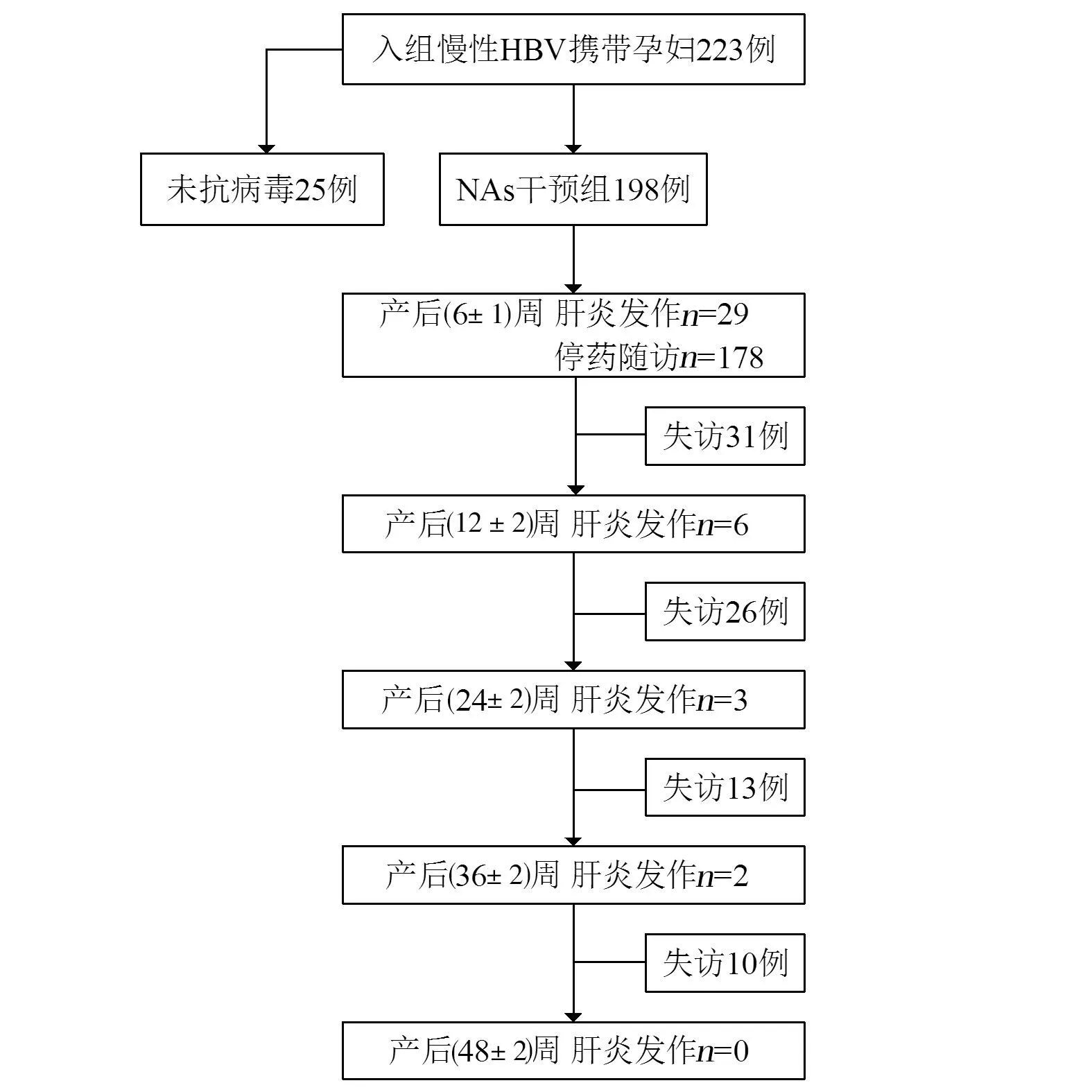
图1 慢性HBV感染孕产妇随访情况
2.2 产后不同停药时间患者产后肝炎发作情况 产后立即停药组和产后6周停药组在抗病毒时和产后各随访时间点的ALT水平比较,差异均无统计学意义(P>0.05),见表1。
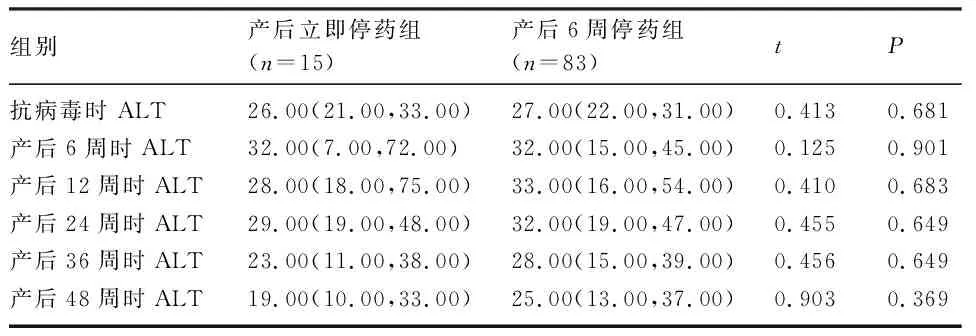
表1 产后不同停药时间患者各时间点ALT水平比较(U/L)[M(P25,P75)])
2.3 患者产后肝炎发作的危险因素分析 单因素分析结果显示,患者开始抗病毒时的血清基线ALT、HBcrAg、HBsAg、HBeAg及HBV DNA为影响慢性HBV感染孕妇产后肝炎发作的相关因素(P<0.05),见表2。将单因素分析中具有统计学差异的因子纳入多因素logistic回归分析,结果显示,患者开始抗病毒时的血清基线HBcrAg、HBsAg、HBeAg及HBV DNA为影响慢性HBV感染孕妇产后肝炎发作的独立危险因素(P<0.05),见表3。
表2 198例慢性HBV感染孕妇产后肝炎发作危险因素的单因素分析

表3 影响慢性HBV感染孕妇产后肝炎发作危险因素的多因素分析
2.4 血清标志物对慢性HBV感染孕妇产后肝炎发作的预测能力 根据孕妇开始抗病毒时血清HBcrAg、HBsAg、HBeAg和HBV DNA这四个独立危险因素对应的偏回归系数β,构建慢性HBV感染孕妇产后48周内肝炎发作风险的回归预测模型为logit(p)=-65.372+1.655*HBcrAg+1.713*HBsAg+2.445*HBeAg+0.702*HBV DNA,其中p为慢性HBV感染孕妇产后48周内肝炎发作的概率。Hosmer-Lemeshow模型χ2=3.088,P=0.929,提示模型的拟合度较好。
绘制血清HBcrAg、HBsAg、HBeAg和HBV DNA预测慢性HBV感染孕妇产后48周内肝炎发作的ROC曲线,其AUC依次为0.713、0.627、0.813、0.896,提示以上指标对慢性HBV感染孕妇产后肝炎发作风险有较好的预测价值,且四者联合诊断预测价值更高(AUC=0.953),预测灵敏度为90.00%,特异度为90.50%,见图2。
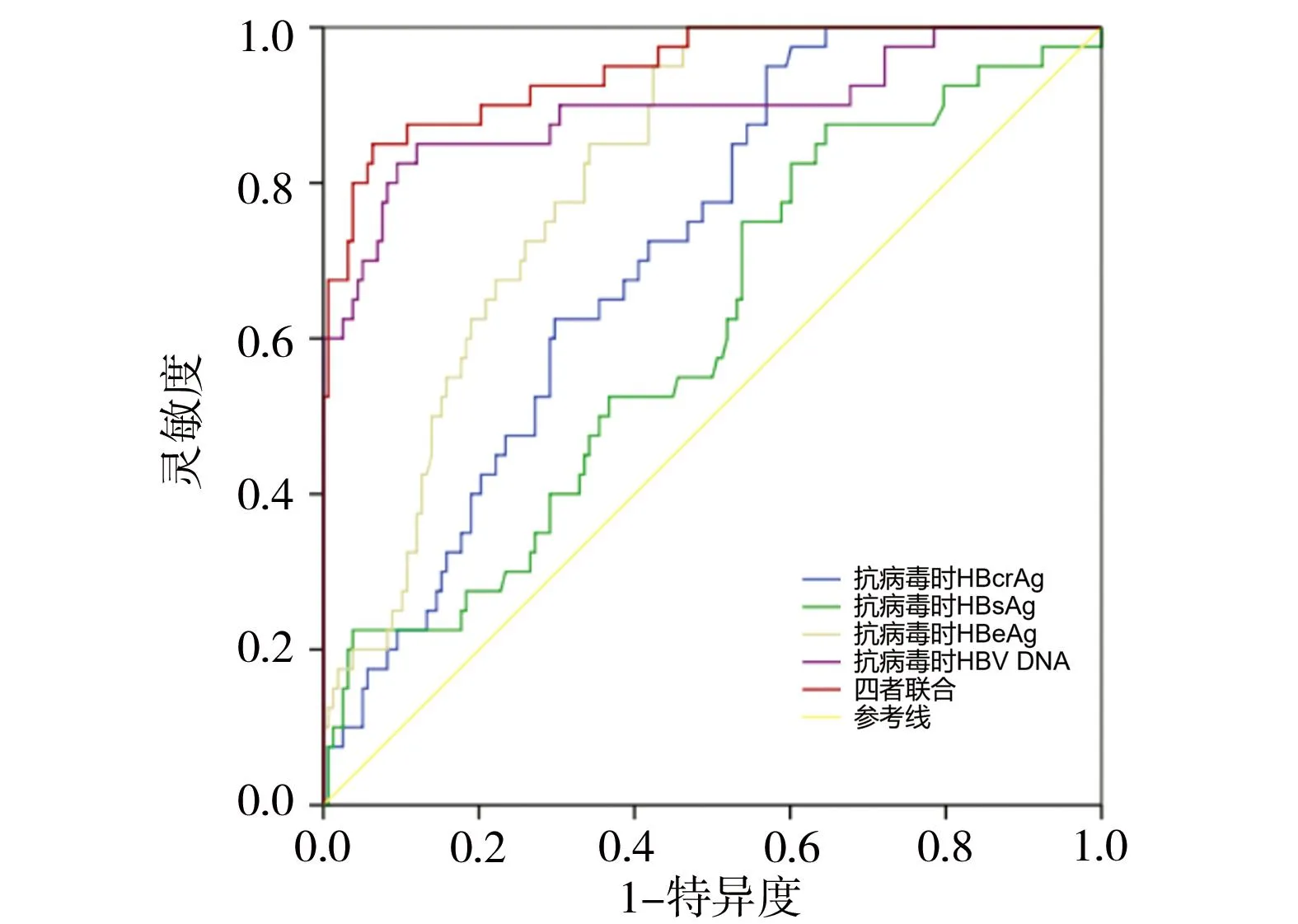
图2 慢性HBV感染孕妇ROC曲线
3 讨 论
多数乙肝孕产妇处于免疫耐受期(慢性HBV携带状态),处于乙肝病毒与人体免疫功能之间的平衡状态。根据当前指南[3],临床上这一时期的患者对抗病毒药物应答反应不佳,停药后往往出现病毒反弹,且很少发生HBeAg血清学转换或HBsAg清除,此时即使继续抗病毒也无法进一步消除病毒[9]。因此对于该类患者可考虑产后即刻停药或产后继续抗病毒1~3个月后停药[6,8]。但分娩后的激素变化和免疫功能变化使此类患者的免疫平衡被打破时就可能发生产后肝炎活动,产后子宫炎症、高HBV DNA载量刺激、机体免疫力改变、产后皮质醇水平快速下降从而减少对肝脏炎症的抑制等种种原因都可能加重肝脏炎症反应[10]。
《预防乙型肝炎病毒母婴传播管理流程(2022)》[11]中,“约28%的HBV感染孕妇在产后24周内出现肝功能异常,同时孕妇HBV DNA负荷过高是肝功能异常的危险因素”。本研究显示,慢性HBV携带孕产妇以母婴阻断为目的抗病毒治疗停药后在产后48周内肝炎发作比例为20.20%,主要发生在产后(6±1)周,与目前报道数据相符。本研究比较产后立即停药和产后6周停药的ALT异常概率无显著差异,提示分娩时停药与产后6周停药对产后肝功能无明显影响。本研究中有10.1%(20例)的患者发生了明显血清学转换倾向及ALT异常升高遂继续抗病毒治疗,针对这一类患者应充分沟通继续服药的利弊及停药风险并加强随访频率。一项针对中国人群的前瞻性研究报道,对于免疫耐受期的孕妇无论是否采用NAs干预,妊娠期和产后都可能发生肝炎发作,产后发生率高于妊娠期,其肝炎活动的峰值为产后6周[12],但大部分患者的肝炎活动是自限性的,鲜有肝炎失代偿发生[13],这可能与妊娠相关的免疫激活强度较低有关。但仍有自行停药后引发乙肝相关肝衰竭的报道[14],提示预测乙肝孕产妇产后肝炎活动发生风险至关重要[15]。
关于孕期应用NAs抗病毒治疗产后预测肝炎活动的研究较少,且结果不一。先前研究表明,高乙肝病毒载量和停止抗病毒治疗是产后肝炎发作的潜在危险因素[16-17]。Liu等[18]发现,开始抗病毒时的基线HBV DNA水平是患者产后肝炎发作的独立预测指标。郭辉杰等[19]认为,妊娠期基线ALT水平是影响产后肝功能异常的独立因素。Lu等[20]报道,接受母婴阻断抗病毒的免疫耐受期患者产后肝炎发作的危险因素包括年龄较小、产前ALT较高、产后较高的干扰素-γ(interferon gamma,INF-γ)水平和产后较低的HBeAg水平。但很难根据单一的血清学指标和单一的时间节点对患者进行风险分层,精准预测出每个以母婴阻断为目的抗病毒的不同个体产后肝炎的发作情况。
新型生物学标志物可更好地反映患者HBV共价闭合环状DNA(cova-lently closed circular DNA,cccDNA)的表达及转录水平[21]。HBcrAg包括血清HBcAg、HBeAg与p22cr这三种蛋白质抗原。由于它们具有相同的149个氨基酸序列,因此可用同种单克隆抗体进行检测[21]。一项针对白种人群的研究发现,慢性乙肝患者抗病毒治疗后血清HBsAg、HBcrAg和HBV RNA与停药后较高的肝炎发作风险相关[22]。对于亚洲人群,在抗病毒停药后,约51%处于较低HBcrAg水平的患者出现高病毒学反应性(virologic response,VR)[23]。但目前研究多聚焦于慢性乙肝患者中血清HBcrAg的预测效能,关于血清HBcrAg对母婴阻断为目的抗病毒的孕产妇患者产后肝炎发作的预测研究不多,仅一项研究报道了对于慢性HBV感染免疫耐受期孕妇短程抗病毒治疗后慢性乙型肝炎急性发作者,分娩后停药时的HBcrAg和HBsAg可作为其发病的预测指标[5]。
本研究通过检测慢性HBV携带孕产妇在孕期开始抗病毒治疗时血清HBcrAg水平结合肝功能、乙肝五项、HBV DNA水平,确定了开始抗病毒时血清HBcrAg、HBsAg、HBeAg和HBV DNA水平可有效预测这类人群经短期抗病毒治疗后的产后肝炎发作,四项指标的高水平与肝炎活动率呈正相关。本研究进一步应用ROC曲线分析显示,联合检测患者开始抗病毒当日血清HBcrAg、HBsAg、HBeAg和HBV DNA水平的AUC(0.953)明显大于单独检测各项预测因子的AUC,表明孕妇开始抗病毒时联合检测各项预测因子可有效提高对产后肝炎活动的预测效能。
本研究的局限性:(1)研究开展时间贯穿于新型冠状病毒疫情时期,而本中心为新冠孕产妇定点救治医院,导致乙肝孕产妇的收治人数显著少于设计预期,且很难收集各个时间点完整的血样,尤其是抗病毒停药时的血清HBcrAg等各项指标,可能导致选择偏倚。(2)新型冠状病毒感染或新冠疫苗接种可能与肝炎活动及肝功能异常有关[24],本研究并未统计患者是否曾感染新型冠状病毒及疫苗接种情况,可能导致一定混杂偏倚。(3)选择产后48周作为肝炎活动的结局终点,患者在产后48周后的情况并未随访,缺乏长期的临床结果,需在后续更大样本量研究中进一步研究,观察NAs干预的长期影响。
综上所述,在慢性HBV感染孕产妇以母婴阻断为目的抗病毒时,联合检测患者开始抗病毒时的血清HBcrAg、HBsAg、HBeAg和HBV DNA水平可有效预测患者产后48周内肝炎活动的风险,对预测慢性HBV感染孕产妇患者产后肝炎发作具有一定的临床价值。
