体外膜肺氧合并发血栓发生率的meta分析
2024-03-26彭伊梦李思雨孙亚楠王胜昱
彭伊梦, 姚 杨,李思雨,丁 格,孙亚楠,王胜昱
(西安医学院第一附属医院 呼吸与危重症医学科,陕西 西安 710077)
体外膜肺氧合技术(extracorporeal membrane oxygenation,ECMO)是一种机械循环支持装置,主要用于治疗危及生命的心脏和肺功能衰竭[1],它包括两种方式:静脉-静脉(venovenous,VV)ECMO(在呼吸衰竭中提供支持和氧合)和静脉-动脉(venoarterial,VA)ECMO(同时提供呼吸和心脏支持)。虽然ECMO已显示出明显的优势,但文献报道ECMO支持后患者的住院生存率为30%~55%[2]。同时用于ECMO支持的血管通路套管和离心泵通常可产生高剪切应力和湍流造成血流动力学变化,导致循环血细胞和止血蛋白的损伤,减少血管性血肿因子与胶原和血小板的结合,导致血栓形成、纤维蛋白溶解和血小板功能受损的状态[3],从而造成ECMO治疗后患者发生血栓相关并发症的风险显著增高[4],需要常规抗凝来防止血栓性并发症[5],降低死亡率。研究表明,ECMO支持治疗后血栓并发症发生率为3.9%~71.4%[6-7],不同研究结果存在差异。本研究通过研究ECMO治疗患者血栓并发症的发生率,以指导临床,降低血栓相关并发症的发生风险,从而降低患者病死亡率。
1 资料与方法
1.1文献检索 计算机检索 PubMed、 EMBASE、万方和中国知网数据库等相关数据库,查找关于ECMO治疗患者发生血栓相关并发症的研究文献,检索时限为建库至2022年12月 31 日,检索关键词为“Extracorporeal Membrane Oxygenation或ECMO” 、“thrombus或 complication”等。
1.2纳入与排除标准 纳入标准:①纳入研究的所有患者均接受ECMO治疗;②所纳入研究详细描述了ECMO治疗期间、治疗后发生血栓并发症及其发生率。排除标准:①患者年龄<18岁;②需纳入数据不完整、数据重复等;③文章未明确指出血栓并发症及发生率;④既往存在血栓栓塞性疾病,如急性肺栓塞或慢性血栓栓塞性肺动脉高压等疾病的研究。
1.3数据提取和质量评价 由2名评价者按照纳入标准与排除标准独立筛选文献,如遇到有争议的则讨论解决。提取资料的内容包括:文献的第一作者、发表年份、国家、样本量、参与者年龄、研究方法、体质指数(body mass index,BMI)、ECMO持续时间、发生血栓例数、抗凝监测方式、研究结局等临床基本资料。采用AHRQ量表(Agency for Healthcare Research and Quality)对纳入文章进行质量评价,分别从研究人群选择、组间可比性及暴露因素(结果测量)3个方面对每一项研究进行评分。
1.4统计学方法 采用StataSE 16.0软件对所纳入文章进行质量评价,采用RevMan5.4软件进行统计学分析及敏感性分析。首先对各研究进行异质性分析,统计学结果认为P≤0.1,I2>50%时具有异质性,选用随机效应模型进行meta分析,反之,则用固定效应模型。当具有异质性时,进行亚组分析研究导致异质性的原因,如设计方案、年龄、性别、BMI、ECMO持续时间、抗凝监测方式等是否一致。
2 结 果
2.1文献检索结果 按照纳入、排除标准,由2名研究人员进行独立评价。初步检索到 547篇文章,其中153篇无法获取全文,去除重复文章、排除综述、meta分析、会议论文、病例报道、动物研究或专家共识等313篇,通过阅读全文筛选,排除40篇文章,最终共纳入16篇文章,共计1 136例患者,其中发生血栓并发症者345例,文献主要发表年份为2012-2022年,文献具体筛选流程见图1。

图1 纳入文献筛选流程
2.2纳入文献基本特征 所纳入文献基本特征见表1,根据NOS评分标准对纳入的每一项研究进行质量评价,评分越高,文章风险偏倚越低,质量评价结果见表2。
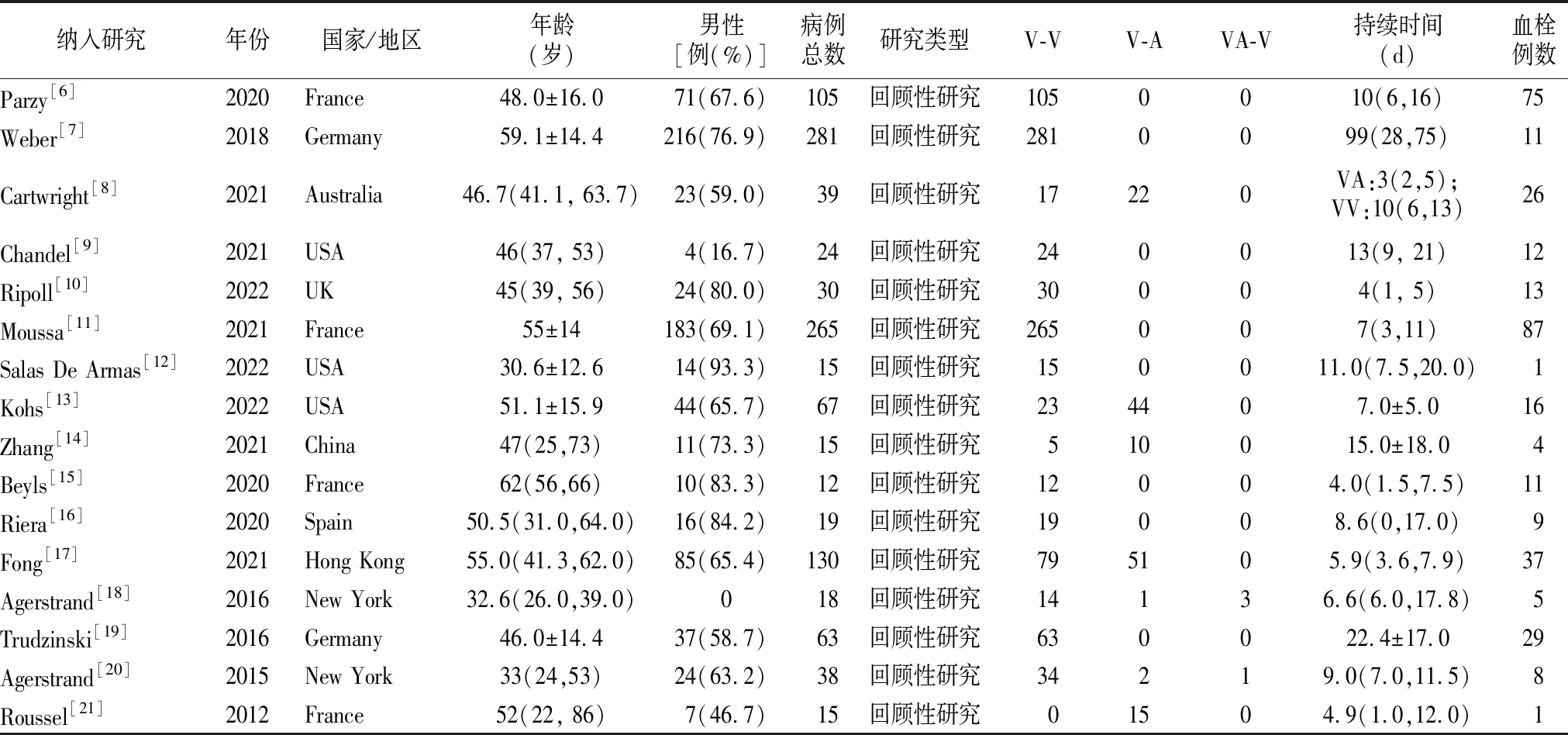
表1 纳入文献的基本特征
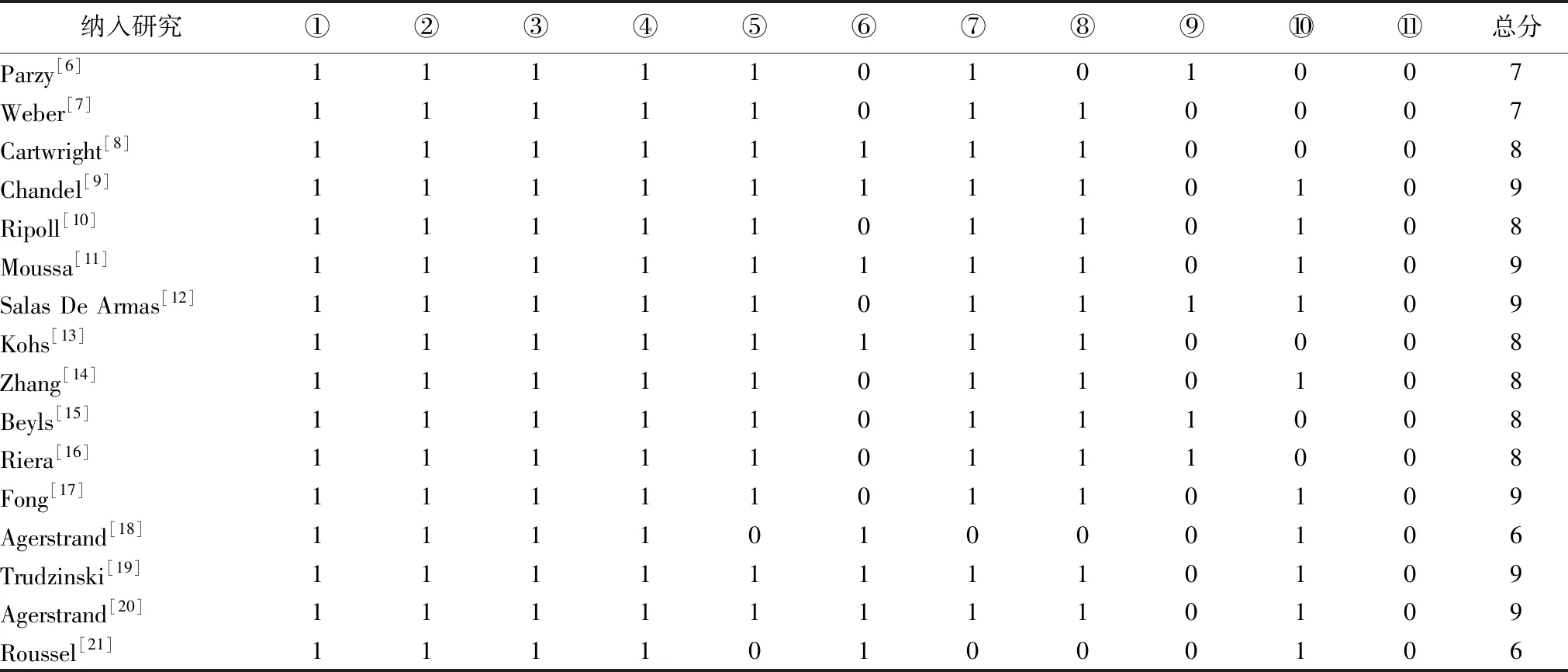
表2 纳入文献的质量评价
2.3Meta分析结果
2.3.1ECMO并发血栓的发生率 纳入分析的16篇文献均准确提供了血栓发生率,异质性分析提示P<0.01,I2=91%,各研究间存在异质性,故采用随机效应模型对效应量进行合并,结果显示总的血栓发生率为52.0%(95%CI:0.30~0.88)。漏斗图结果显示基本对称,可认为无明显发表偏倚,但有部分研究散落在置信区间外,提示存在异质性,见图2~3。
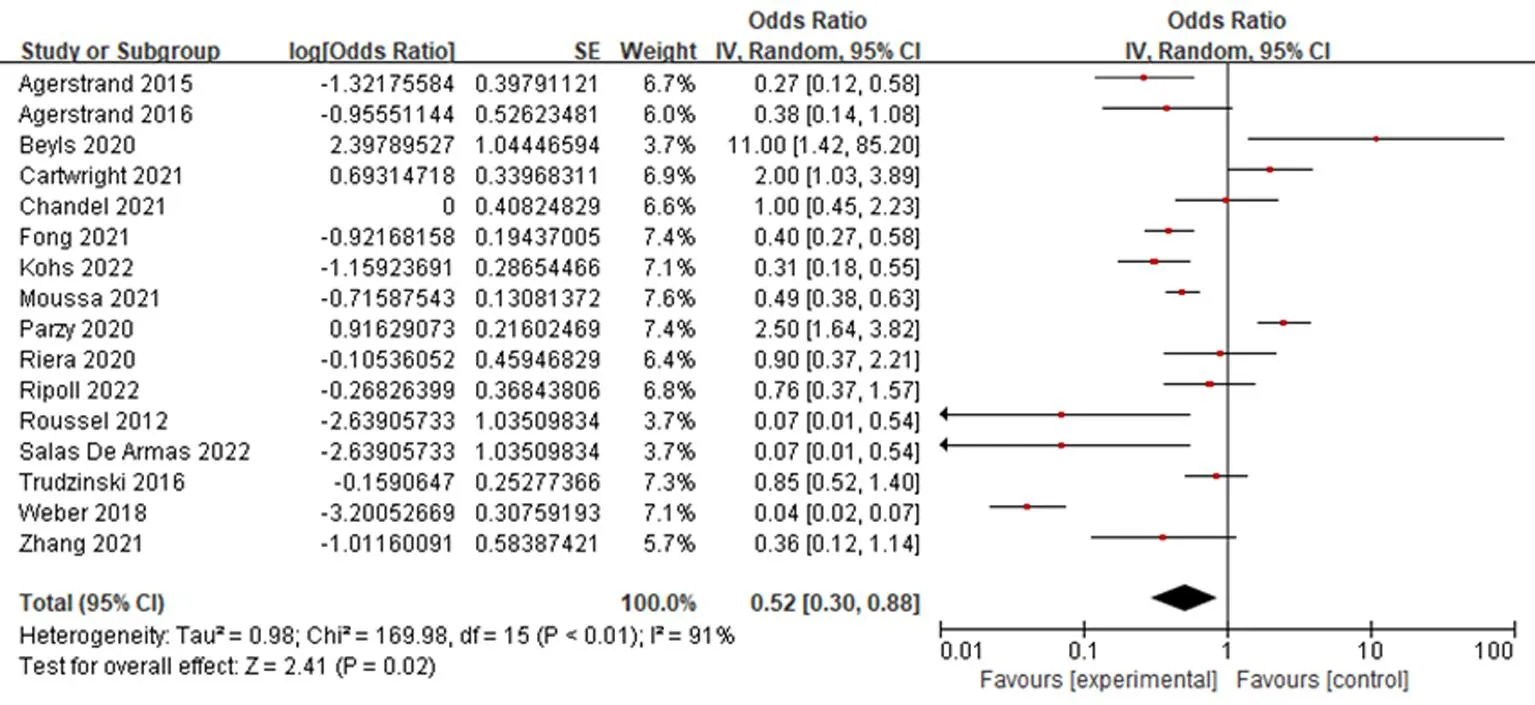
图2 ECMO患者血栓发生率的森林图
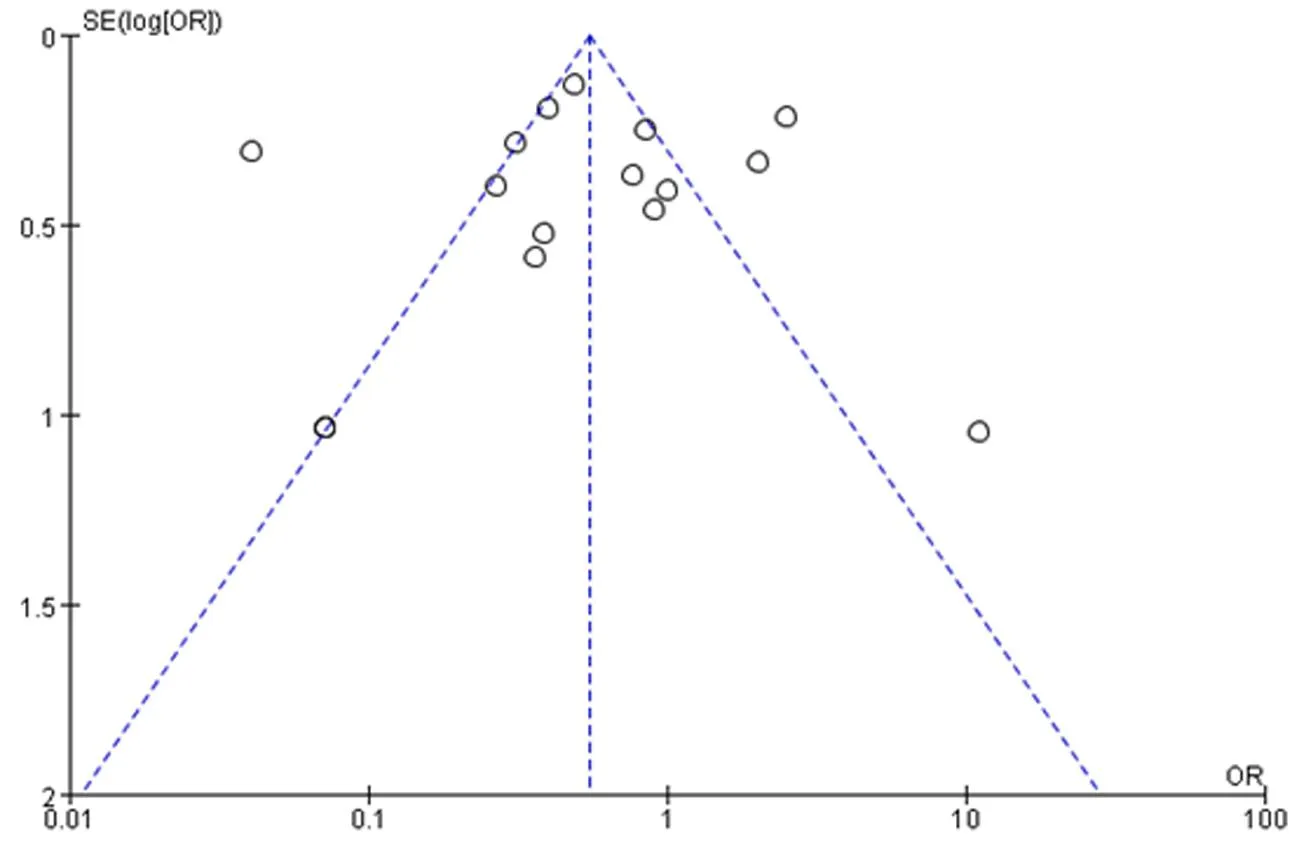
图3 ECMO患者血栓发生率的漏斗图
2.3.2亚组分析 根据患者年龄、ECMO持续时间、BMI及抗凝监测方式等因素进行亚组分析,结果显示:①依据联合国确定的新的年龄分段,将年龄分为<45岁、45~59岁、≥60岁3个阶段,因≥60岁年龄段仅纳入一篇文献研究,未纳入亚组分析,其中<45岁、45~59岁ECMO并发血栓的发生率分别为27.0%、53.0%,年龄越大,血栓发生率越高。②通过计算平均ECMO持续时间中位数,将ECMO平均持续时间分为≤10天、>10天两组,血栓发生率分别为50.0%、39.0%,ECMO持续时间越短,血栓发生率越高。③依据BMI分级标准,将BMI分为24~27.9 kg/m2、≥28 kg/m2两组,其血栓发生率分别为27.0%、66.0%,BMI值越高,血栓发生率越高。④ 依据活化部分凝血活酶时间(APTT)、激活全血凝固时间(ACT)、抗fxa 3种不同的抗凝监测方式进行亚组分析,结果显示, APTT组血栓发生率最高(57.0%),其次为抗fxa组(45.0%),ACT组血栓发生率最低(13.0%),见表3。
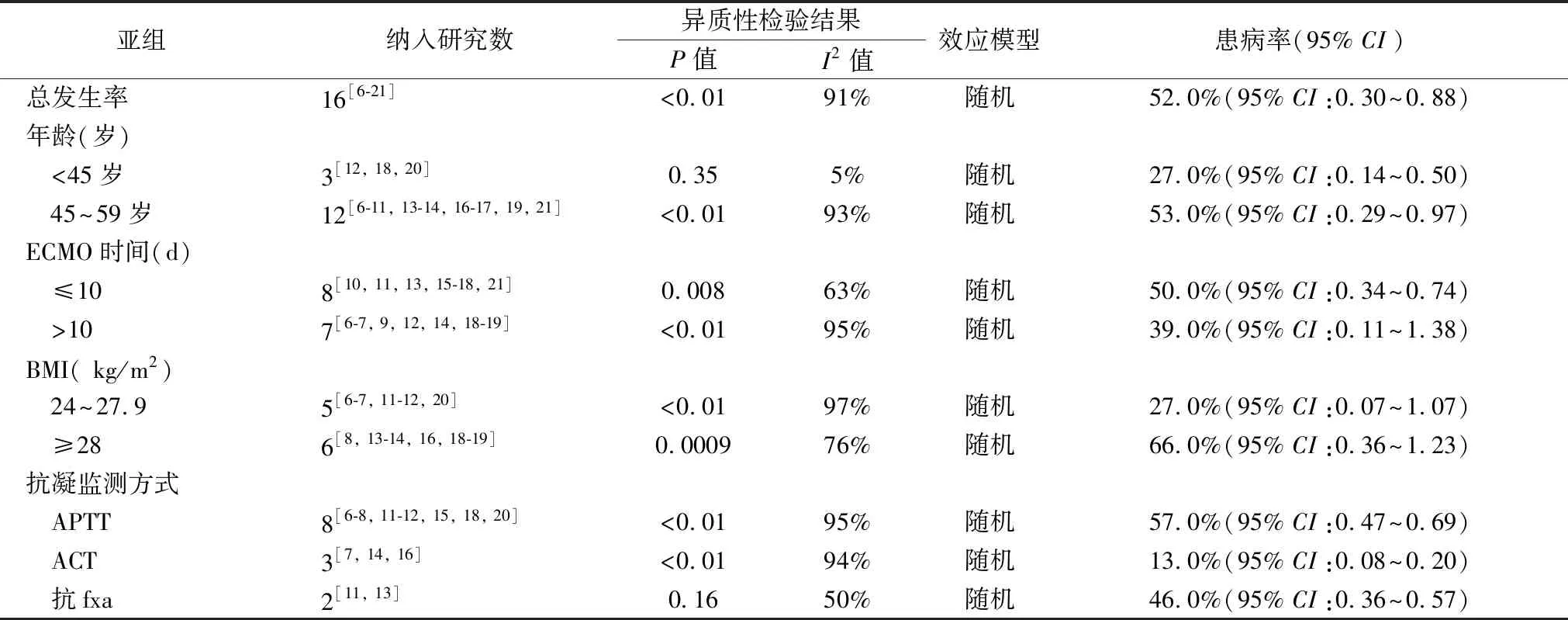
表3 Meta分析结果汇总表
2.3.3敏感性分析 共纳入16篇文献,采用逐一排除法排除单个研究进行敏感性分析,基于随机效应模型合并后的结果与血栓总发生率的结果相似,提示此次meta分析结果稳定,见表4。
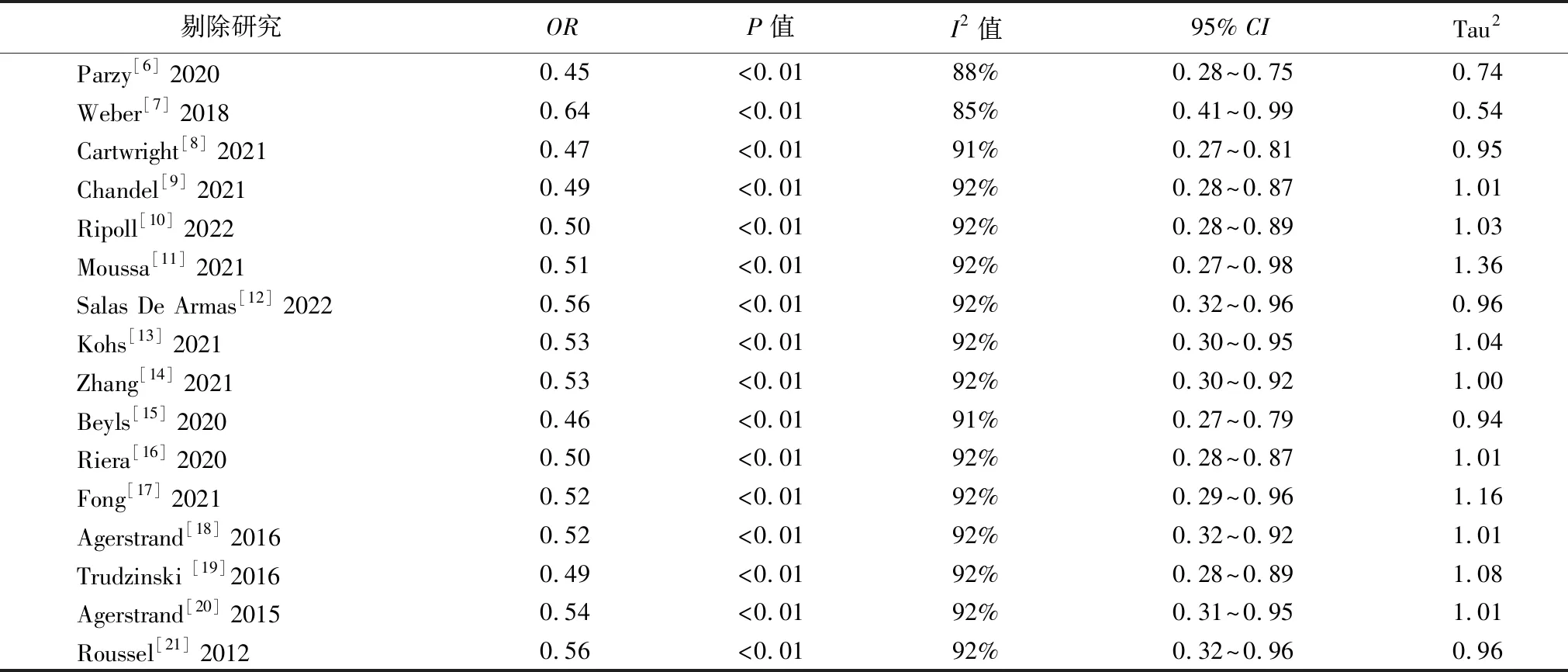
表4 ECMO患者血栓发生率的敏感性分析
3 讨 论
ECMO是一种便携式改良的体外循环装置,能够支持危重患者数天至数周[22],VA ECMO的适应证主要包括心源性休克、感染性休克伴相关心肌病、心脏骤停、栓塞症、难治性室性心律失常和有创手术并发症等,VV ECMO用于急性呼吸窘迫综合征、吸入性损伤、哮喘持续状态、胸部创伤和急性呼吸道阻塞等。接受ECMO治疗的患者病情危重,常有凝血功能障碍和高炎症状态,由于所需的人工材料及其对循环、内皮、血液、炎症和免疫系统的影响,潜在的并发症问题一直备受关注,如血栓、出血、感染、全身炎症反应综合征、肾功能衰竭等。在ECMO启动时,患者的血液与外来ECMO回路的接触会引发大量的炎症反应,导致促凝剂和抗凝因子的激活,促进了止血系统的上调,导致过度的血栓形成和纤溶,以及血小板和凝血因子的消耗[23],患者容易发生不适当的出血和凝血。此外,ECMO患者还存在血小板功能缺陷[24],影响其活化、黏附和聚集,导致血小板留在循环中的效果可能较差,从而增加出血、血栓并发症[25],这是其最常见的不良反应[26]。研究发现,ECMO支持治疗的新型冠状病毒肺炎患者尽管进行了血栓预防,但是发生血栓并发症的风险仍超过了30%[27]。然而,Agerstrand等[20]的一项回顾性研究发现,ECMO支持期间使用低靶点的APTT进行抗凝时,回路及氧合物血栓形成较为罕见,不同研究血栓发生率差异明显。本系统研究的目的是评价ECMO治疗患者血栓发生率,并分析血栓发生的风险因素。
本研究结果表明,ECMO治疗患者血栓并发症的发生率为52.0%(95%CI:0.30~0.88),异质性分析提示P<0.01,I2=91%, 具有较高的异质性,异质性的原因多考虑与所纳入研究的临床资料有关。进一步亚组分析结果提示,年龄越大、ECMO时间越短、BMI值越高、采用APTT监测抗凝者血栓发生率均较高。在对年龄进行亚组分析时,因年龄≥60岁这一年龄段仅纳入了一项研究,并未纳入分析;BMI及抗凝监测方式在进行亚组分析时因部分纳入文献未明确提及相关指标,部分研究也被排除在外,造成结果具有片面性。通过meta分析尽管能预测ECMO治疗患者血栓并发症的发生率,但仍存在一定的局限性,分析其原因可能为:①筛选纳入的文献存在一定的异质性,可能是由于年龄、样本量大小、人群、不同研究方式、性别、地域、ECMO持续时间及方式等因素影响所致,虽进一步进行了亚组分析寻找异质性来源,但对年龄进行分析时,年龄≥60岁这一年龄段仅纳入了一项研究,不够全面。此外,研究发现,ECMO插管类型并不影响住院死亡率和长期生存率[28],加之所纳入文献并未明确提及不同类型插管方式血栓发生情况,因此并未对ECMO方式进行亚组分析,造成结果存在一定偏差,需大规模开展相关临床研究。②本系统研究在测量结果筛选时,除排除了在ECMO治疗前已有血栓发生患者的文献,仅关注了每一项研究血栓的发生率,并未考虑患者ECMO治疗前基础疾病、免疫状态、凝血功能、高炎症反应等情况,因此在结果预测上具有一定偏倚。③ECMO支持治疗常规使用低分子肝素、普通肝素抗凝,预防出现血栓及出血并发症,但所纳入的大部分文献并未明确指出抗凝监测方式及凝血指标变化,因此在进行meta分析、亚组分析时未考虑抗凝因素影响,使结果有一定偏差。④临床试验研究中,发表的结果多为阳性结果,发表偏倚也应该加以考虑。⑤本系统研究仅使用英文检索文献,可能会因语种导致偏倚。
综上,ECMO治疗患者血栓并发症的发生率较高,对患者的预后、生存率有一定的影响。但受到所纳入文献质量、文献数量的影响,需进一步大规模、高质量的临床试验研究来证实ECMO治疗患者血栓并发症的发生率。
