薰衣草精油缓释固体分散体的制备及其体外释药性能研究
2024-03-19王园园顾志荣毛小文
王园园,顾志荣,郭 燕,毛小文,葛 斌
(1.甘肃中医药大学 药学院,甘肃 兰州 730000;2.甘肃省人民医院 药剂科,甘肃 兰州 730000)
薰衣草精油(Lavender essential oil,LEO)是薰衣草(Lavandula angustifoliaMill.)的主要有效成分,是由多种小分子化合物组成的具有挥发性的复杂混合物[1]。薰衣草及LEO 目前尚未被2020 年版《中国药典》收载,但薰衣草收载于《中华本草》《中华人民共和国卫生部药品标准-维吾尔药分册》及《维吾尔药材标准》,具有消散寒气,益胃健脑,燥湿止痛之功效,同时也收载于《欧洲药典》及《美国药典》中[2-5]。LEO 的化学成分主要为芳樟醇、乙酸芳樟酯、1,8-桉叶素、萜品烯-4-醇、罗勒烯、乙酸香叶酯等,其中以芳樟醇与乙酸芳樟酯含量最高[6]。目前对于LEO的研究热点主要集中在其神经系统药理作用与治疗价值方面,如改善睡眠障碍、抗焦虑、抗抑郁、抗狂躁、影响内分泌、治疗偏头痛及神经性疼痛等[7-8]。此外,LEO 还具有抗氧化、解痉、镇痛、抗菌、抗肿瘤、抗突变等作用[5]。国内外对LEO 主要采用吸入疗法与透皮吸收疗法,用于改善睡眠,缓解焦虑、抑郁及头痛,其中采用吸入疗法治疗睡眠障碍使用尤多,多做成含有薰衣草的枕头、香包、粉剂等,但存在疗效不确切,难以量化控制,作用机制不明,携带不便等问题[9]。因此,开发一种安全有效、稳定可控、适于口服、作用持久的治疗失眠的现代LEO新制剂,对于解决上述问题具有实际意义。本研究首次尝试以硬脂酸、PEG 6000和单硬脂酸甘油酯为辅料制备LEO固体分散体,并考察其体外释药性能,以提高LEO溶出,达到缓释效果,长效改善睡眠。
1 仪器与材料
1.1 试验仪器
890B GC-5977A MSD 型GC-MS 联用仪,配备氢火焰离子化检测器(FID),DB-5MS 毛细管柱(30 m × 0.25 mm,0.25 μm),Chemstation 化学工作站(美国Agilent公司);AL204 型万分之一电子天平(瑞士Mettler Toledo 公司);DZF-6090 型真空干燥箱(上海一恒科学仪器有限公司);RCZ-8M 溶出试验仪(天津天大天发科技有限公司);pHS-3C 型酸度计(上海越平科学仪器有限公司);SB25-12DTD型超声波清洗机(宁波新芝生物科技股份有限公司)。
1.2 材料
LEO,购自广州科然精油原料有限公司(精油浓度 ≥ 98%,阴凉遮光保存);对照品芳樟醇(CHB210217)、乙酸芳樟酯(CHB210623),纯度均 ≥ 98%,均购于成都克洛玛生物科技有限公司;药用级辅料单硬脂酸甘油酯、聚乙二醇6000、硬脂酸,均符合2020年版《中国药典》标准;丙酮、环己酮,均为色谱纯,均购于天津大茂化学试剂厂;实验用水均为蒸馏水。
2 方法
2.1 LEO 及固体分散体中芳樟醇和乙酸芳樟酯含量测定
2.1.1 GC-MS分析条件
色谱柱为DB-5MS 毛细管柱(30 m × 0.25 mm,0.25 μm),程序升温(起始温度50℃,保持5 min,以2℃/min 升高至100℃,再以3℃/min 升高至150℃,再以8℃/min升高至250℃),载气为氦气(99.99%),流速为1 mL/min,进样量为0.4 μL,分流比为60 ∶ 1,进样口温度为250℃。采用电子轰击离子源(EI),电子能量为70 eV,离子源温度为230℃,接口温度为250℃,扫描方式为全扫描,扫描范围30 ~ 500m/z。
2.1.2 标准储备液配制
分别取芳樟醇和乙酸芳樟酯96.4 mg、52.3 mg,置于10 mL容量瓶中,以丙酮溶解并定容至刻度,配制成浓度分别为9.64 mg/mL、5.23 mg/mL 的混合标准储备液。
2.1.3 供试品溶液制备
精密称取样品15 mg,置于10 mL 容量瓶中,加入环己酮1 mL,以丙酮定容至刻度,即得供试品溶液。
2.1.4 线性关系考察
依次取上述标准贮备液0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8 mL,分别加入10 μL 环己酮作为内标,再以丙酮定容至1 mL容量瓶中,采用“2.1.1”项下条件测定,记录峰面积。
2.1.5 精密度试验
取同一批样品,按“2.1.3”项下方法制成供试品溶液,采用“2.1.1”项下条件连续进样6 次,记录峰面积。
2.1.6 重复性试验
取同一批样品6 份,按“2.1.3”项下方法制成供试品溶液,采用“2.1.1”项下条件进样测定,记录峰面积。
2.1.7 稳定性试验
取同一批样品,按“2.1.3”项下方法制成供试品溶液,分别于0、2、6、8、12 h 按“2.1.1”项下条件进样测定,记录峰面积。
2.1.8 加样回收率试验
精密称取已知芳樟醇和乙酸芳樟酯含量的样品,分别加入芳樟醇和乙酸芳樟酯对照品适量,按“2.1.3”项下方法制成供试品溶液,按“2.1.1”项下条件进样测定,计算回收率。
2.1.9 溶出度测定
精密称取LEO 原料与缓释固体分散体分别装于胶囊中,置于900 mL磷酸盐缓冲液(pH = 7.2)中,采用2020 年版《中国药典》四部规定的“第二法(桨法)”[10]测定,转速50 r/min,水浴温度(37 ± 0.5)℃,分别在0.5、2、4、6、8、12 h 各取样2 mL,同时补充等体积、同温新鲜介质,所取样品经0.45 μm 微孔滤膜过滤,自取样至滤过在30 s内完成,取续滤液,蒸干,按“2.1.4”项下方法制备供试品溶液,按“2.1.1”项下条件进行测定,计算累积溶出度。
2.2 正交试验优化LEO 缓释固体分散体的处方配比
2.2.1 单因素考察
以硬脂酸 ∶ PEG 6000 ∶ 单硬脂酸甘油酯 ∶LEO = 3 ∶ 4 ∶ 1 ∶ 1 为基准,使其中1 个因素水平变化,其他2个因素水平固定,进行单因素考察。选择硬脂酸/LEO 用量比值(A)、PEG 6000/LEO 用量比值(B)、单硬脂酸甘油酯/LEO 用量比值(C)作为影响因素,以芳樟醇和乙酸芳樟酯总量的累积溶出度(P)为综合评价指标,累积溶出度设3 个考察点P2、P6、P12,分别指2、6、12 h 的累积溶出度,P2、P6、P12分别以30%、65%、90%为标准,则P= 100 - |P2- 30%|- |P6- 65%| - |P12- 90%|,P值越高,表明与所定的标准趋势越接近[11]。
2.2.2 正交试验设计优化处方配比
根据单因素考察结果,A、B、C 等3 个因素各选定3 个水平,按照L9(34)正交表设计试验,因素水平见表1。

表1 正交试验设计因素水平表Tab. 1 Table of design factors for orthogonal test
2.2.3 工艺验证
采用优化出的最佳处方配比制备3批LEO固体分散体,按照“2.1.9”项下方法测定各时间点的P。
2.3 LEO缓释固体分散体的体外释药模型拟合
分别采用零级方程、一级方程、Higuchi 方程、Ritger-Peppas 模型等4 种模型,对12 h 内累积溶出度(P)与释药时间(t)进行曲线拟合,采用拟合系数r判断其拟合程度,r越接近于1拟合越优[12]。
3 结果与分析
3.1 方法学考察
3.1.1 线性关系考察
以进样量为横坐标(X),芳樟醇、乙酸芳樟酯与内标物的峰面积比值为纵坐标(Y),绘制工作曲线,计算回归方程及相关系数r,见表2,总离子流图(Total ion chromatogram, TIC)见图1。
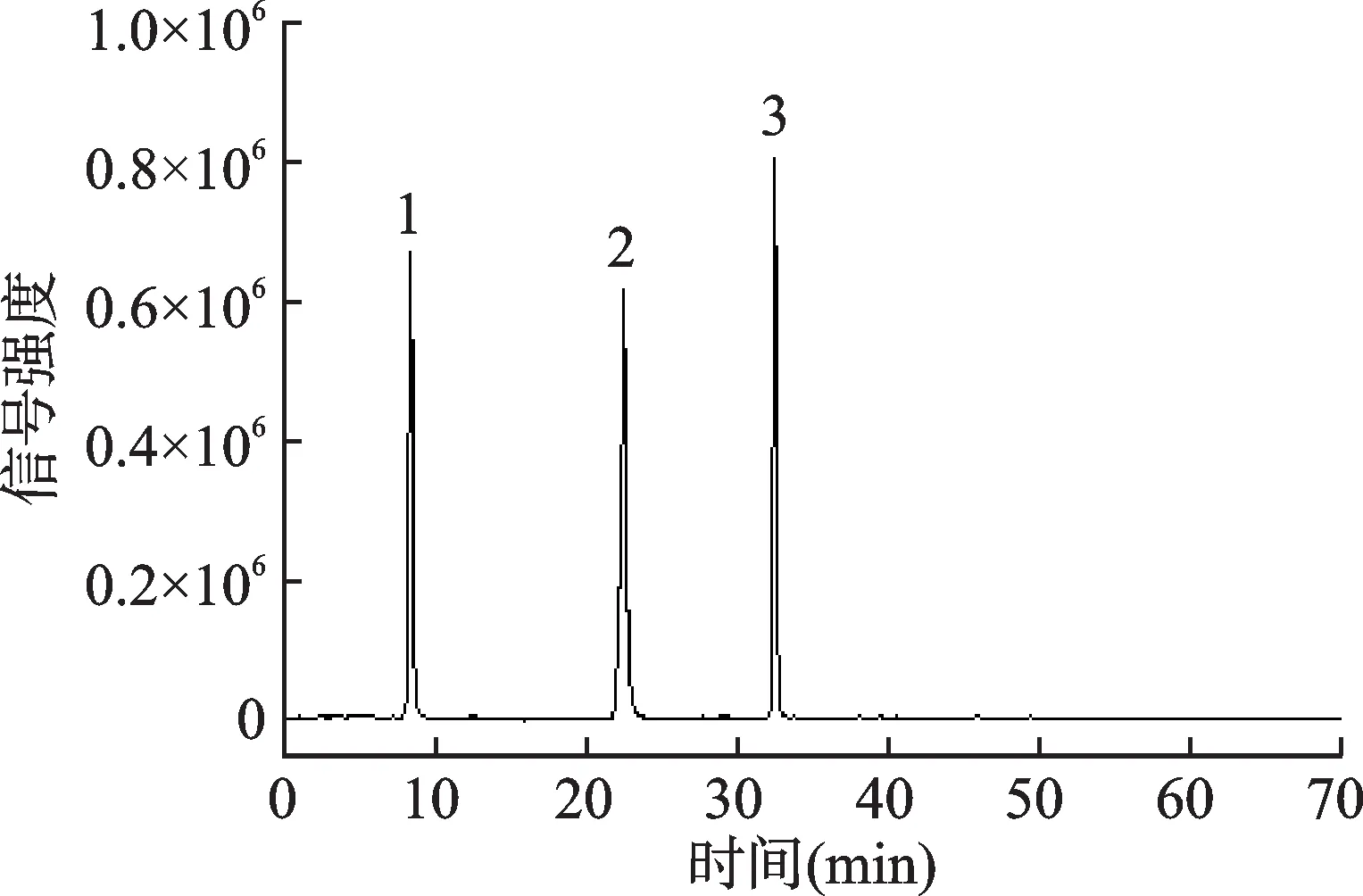
图1 芳樟醇、乙酸芳樟酯和环己酮TIC图Fig.1 TIC diagram of linalool, linalyl acetate and cyclohexanone
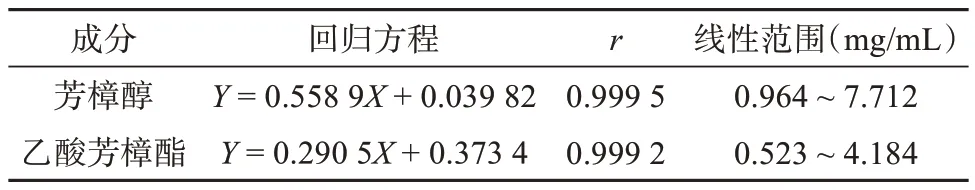
表2 芳樟醇和乙酸芳樟酯的回归方程Tab. 2 Regression equation of linalool and linalyl acetate
3.1.2 精密度试验
芳樟醇、乙酸芳樟酯与内标物峰面积比值的RSD分别为1.63%、1.37%,表明仪器精密度良好。
3.1.3 重复性试验
芳樟醇、乙酸芳樟酯与内标物峰面积比值的RSD分别为2.34%、2.65%,表明该方法重复性良好。
3.1.4 稳定性试验
芳樟醇、乙酸芳樟酯与内标物峰面积比值的RSD 分别为2.82%、2.26%,表明供试品溶液在12 h内稳定。
3.1.5 加样回收率试验
芳樟醇和乙酸芳樟酯的平均加样回收率分别为96.86%和103.41%,RSD分别为2.41%和2.27%。
3.2 单因素试验
当硬脂酸/LEO 用量比值、PEG 6000/LEO 用量比值、单硬脂酸甘油酯/LEO 用量比值分别为3 ∶ 1、5 ∶ 1、1 ∶ 1 时P最大,结果见图2 ~ 4,故依此设计正交试验的因素水平。
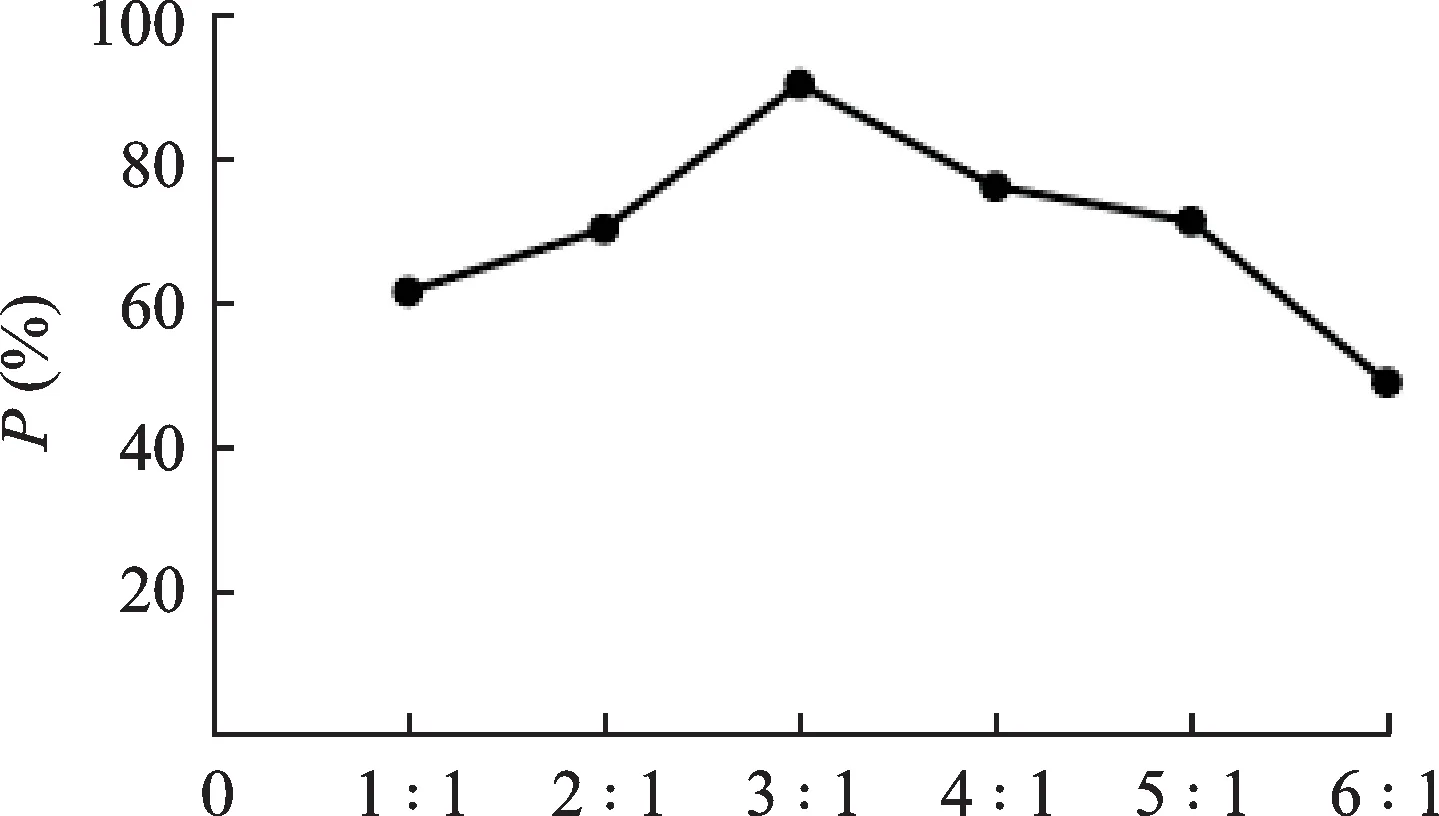
图2 因素A对P的影响Fig.2 The influence of factor A on P
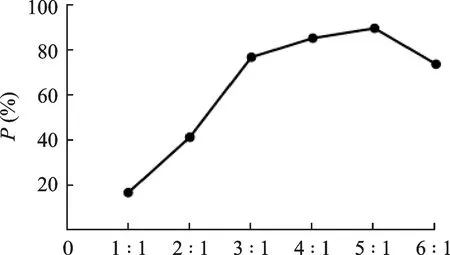
图3 因素B对P的影响Fig.3 The influence of factor B on P
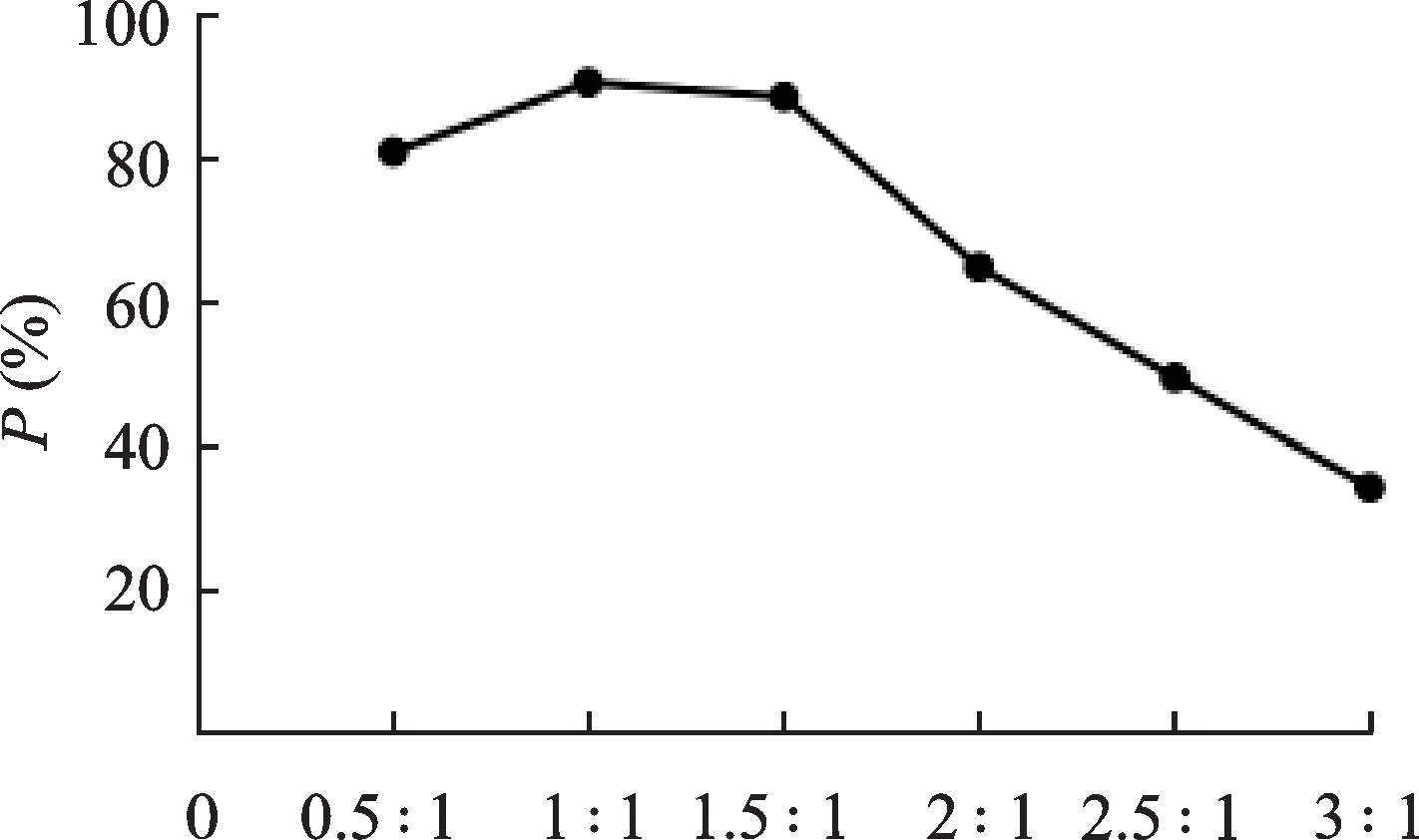
图4 因素C对P的影响Fig.4 The influence of factor C on P
3.3 正交试验
正交试验结果见表3,方差分析结果见表4。结果表明,各因素对LEO 缓释固体分散体P影响大小顺序为B > C > A,最佳处方工艺为A2B2C2,即硬脂酸 ∶ PEG 6000 ∶ 单硬脂酸甘油酯 : LEO = 3 ∶ 5 ∶1 ∶ 1。
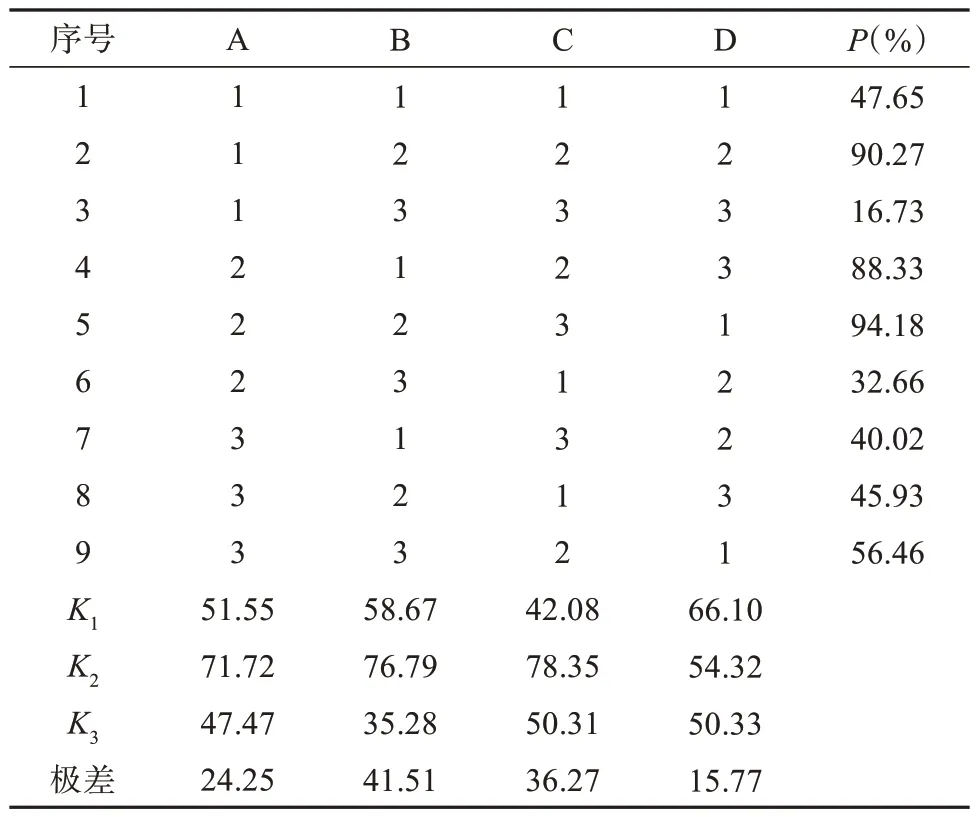
表3 正交试验结果Tab. 3 Results of orthogonal test

表4 方差分析结果Tab. 4 Resultsof variance analysis
3.4 工艺验证
由图5 可知,各时间点P值的RSD 均 < 3%,表明所优选的处方配比工艺稳定、可靠,所制得的缓固体分散体释放速度适宜,在体外能够持续释药12 h,达到了良好的缓释效果,其2 h 的平均释放度为33.43%,6 h 的平均释放度为68.87%,12 h 的平均释放度为92.91%。

图5 3批LEO固体分散体的体外释药曲线Fig.5 Releasecurves of three batches of LEO solid dispersions in vitro
3.5 LEO缓释固体分散体制备工艺
采用熔融法制备,将硬脂酸、PEG 6000、单硬脂酸甘油酯按照3 ∶ 5 ∶ 1 的配比置于70℃烘箱中,待完全熔融后滴加与单硬脂酸甘油酯同比例的LEO,充分搅拌以混合均匀,然后迅速倾倒于冰浴不锈钢板上,涂成薄层,置冰箱中于-20℃冷却6 h,用药勺刮掉凝结的固体分散体,置真空干燥器中充分干燥,待脆化后研细,过80 目筛,即得[13-14]。
3.6 LEO缓释固体分散体的体外释药模型拟合
如表5 所示,一级模型拟合系数r最接近于1,表明一级释药模型拟合度最高。

表5 LEO固体分散体的体外释药模型拟合Tab.5 Release model fitting of LEO solid dispersions in vitro
4 讨论
4.1 LEO治疗失眠的作用机制
薰衣草是蒙医及中医的常用药材,其有效成分是LEO,目前主要采用芳香吸入法治疗睡眠障碍,在民间尤其流行。LEO 能够使实验动物自主活动受到抑制,睡眠时长延长,睡眠潜伏期缩短,但治疗睡眠障碍的分子机制至今尚未完全阐释清楚[15],其机制可能是通过干扰5-HT 信号通路和GABA 能信号通路来发挥治疗失眠的作用[16]。5-羟色胺(5-HT)是一种作用于睡眠-觉醒周期的重要单胺类物质,是一种能促进睡眠的神经递质[17]。有研究表明[18-19],薰衣草精油组与模型组相比,薰衣草精油组小鼠脑内5-HT 含量均显著增加,存在极显著差异,而DA、NE 含量均显著减少,存在极显著差异。因此是通过增加脑内5-HT、减少NE 和DA 来达到治疗失眠的目的。GABA是中枢神经中最重要的抑制性神经递质,能够调节正常状态下的睡眠-觉醒周期,通过神经冲动传递至下丘脑和脑干中,抑制该部位控制觉醒的基因的表达,从而改善失眠[20]。有实验结果显示,薰衣草精油组、轻组分组、芳樟醇组均可使大鼠脑内GABA 水平增加,从而增加抑制作用,改善失眠作用[21]。
4.2 体外释放考察的评价指标选取
目前研究认为,LEO 中最主要的活性成分为芳樟醇、乙酸芳樟酯、1,8-桉叶素等,其中又以芳樟醇、乙酸芳樟酯含量最高,该2 种成分含量越高则LEO 的品质越好。因此,本研究建立GC-MS 法测定芳樟醇、乙酸芳樟酯含量的方法,作为体外释放考察的评价指标。
4.3 辅料的选取
本研究在文献调研的基础上,选择硬脂酸、PEG 6000 及单硬脂酸甘油酯作为LEO 缓释固体分散体的制剂辅料。硬脂酸与PEG 6000成形性较好,对油脂类药物的吸收较好,价廉易得,但也存在水溶性较强,溶蚀性能欠佳,药物释放速度难以调节的问题,不利于形成固体分散体的缓释性能。因此选择一种不溶于水的W/O 型辅助乳化剂——单硬脂酸甘油酯配合使用,不仅能够增加基质的整体稳定性,增加硬脂酸与PEG 6000 在水中的溶蚀能力,而且能够调节药物释放的速度,且密度较大可使制备更加容易。
5 结论
本研究先采用单因素考察,在此基础上采用L9(34)正交试验设计优化处方配比,所得最佳配比为硬脂酸 ∶ PEG 6000 ∶ 单硬脂酸甘油酯 ∶ LEO = 3 ∶5 ∶ 1 ∶ 1,三者按照该比例配合使用,是制备LEO 缓释固体分散体的理想选择,所制得的缓固体分散体释放速度适宜,在体外能够持续释药12 h,达到了良好的缓释效果。并通过零级方程、一级方程、Higuchi 方程、Ritger-Peppas 等4 种模型对体外释药进行拟合,其溶出动力学符合一级动力学模型。该实验所优选的处方配比工艺稳定可靠,所得缓释固体分散体能显著改善药物溶出,为其工业化生产奠定了基础。
