临床研究风险与受益的评估框架构建研究*
2024-03-15余中光盛艾娟
余中光,陈 虎,盛艾娟
(1. 中日友好医院呼吸中心,北京 100029;2. 沧州市中心医院科研处,河北 沧州 061001;3. 首都医科大学附属北京佑安医院伦理委员会,北京 100069)
0 研究背景
为最大程度地保护研究参与者的权益与安全,世界医学协会《赫尔辛基宣言》(2013 版)、国际医学科学组织理事会《涉及人的健康相关研究国际伦理准则》(2016 版)等指南规范均强调研究风险与预期受益必须是可接受的原则。但是,如何解释或指导应用上述伦理原则的文献却很少[1],因为这些指南规范并没有描述风险与受益的定义与内涵。因此,医疗机构伦理审查委员会(institutional review board,IRB)在伦理审查过程中,只能依靠IRB 委员的经验来判断研究风险与受益,这会影响研究风险与受益比的准确判断,甚至会增加错误的概率[2]。事实证明,如果没有清晰的定义,IRB 在评估研究风险和潜在受益方面会存在显著差异[3-4]。例如:有的伦理委员会低估了研究风险,高估了研究受益,对研究参与者保护不充分;有的伦理委员会高估了研究风险,低估了研究受益,影响了一些有价值的研究。一些多中心临床研究,因不同医疗机构伦理委员会的风险与受益判断结果不一致,导致重复审查和资源浪费[5-6]。美国国立卫生研究院一项针对伦理委员会关于“磁共振(不使用镇静剂)”是否为低风险的调查研究发现:在188 人的调查对象中,48% 的受访者认为属于最小风险,35% 的受访者认为不高于最小风险,9% 的人认为高于最小风险,说明不同人对研究干预手段风险大小的认知也存在显著差异[7]。为减少上述认知偏差,阐明临床研究风险与受益内涵已成为紧迫的研究任务。
当前生物伦理学者在澄清与风险、受益相关的一些关键概念方面取得了一定的进展。根据研究参与者参与研究而发生伤害的可能性及严重程度,有学者[8-9]根据一定特征将研究风险按照生理、心理、经济、社会或法律等方面进行划分;有学者[10]将研究风险划分为:药物风险、额外的生理风险及负担、社会风险、心理风险及负担,但均未对每个类别的风险进行系统的内涵阐述。在研究参与者研究方面,有学者[10]提出直接受益、群体受益与科学受益的概念,亦有学者[11]认为研究受益可分为研究参与者受益与社会受益。然而,相比于风险研究,学术界对受益的研究更为缺乏,这种不对称反映在具体的伦理审查实践中。例如,在研究知情同意书上通常会详细列出可能造成的伤害或不适,但很少关注受益或是对受益的描述过于简单。近年来,我国在临床研究领域取得了较为长足的发展,研究伦理体系建设发展迅速,但“本土化”的临床研究风险与受益评价标准和理论依旧缺乏[12]。因此,基于中国国情,本文采用扎根理论方法尝试构建适用于中国的临床研究风险与受益框架,以期拓展现有风险与受益评估理论,为我国研究人员、IRB 评估临床研究的风险和潜在受益提供切实、可行的指导原则。
1 研究方法与设计
1.1 研究对象
为保证研究资料的全面性,本文研究对象来自北京、上海、河北、山东、福建、浙江、江苏、辽宁等8 个省市的机构伦理委员会委员、资深伦理秘书和伦理研究者。
1.2 研究设计
由于缺乏适用于中国国情的临床研究的风险与受益理论,本研究采用扎根理论法[13-14]分析临床研究风险与受益,并深入了解风险与受益的构成要素及其内涵,探究这些要素之间的模式和关系。
1.3 数据收集
采用半结构化访谈法收集数据。访谈以中文交流,并根据每个受访者的背景和经验灵活进行,并在获得受访者允许的情况下进行录音。在讨论过程中进行记录,以跟踪新出现的想法。在访谈时还收集了受访者的人口统计学特征。访谈问题如下:①研究参与者参加临床研究会存在哪些风险,这些风险会给研究参与者带来哪些伤害或损失?②研究受益应当包括哪些方面,能否具体阐述?
1.4 数据分析
本研究成立了编码小组,由2 位熟悉该领域的成员组成。通过小组研讨的方式,共同进行原始资料的概念化、范畴化及后续的编码工作。NVivo11软件用于文本资料的存储、整理、编码和分析。
1.5 研究步骤
本研究严格遵循扎根理论的模型建立准则和步骤,将文本资料概括化及范畴化,同时结合专家意见修订存在争议的范畴概念,避免编码者主观意向对编码效果的影响,以保证研究的信度和效度。具体步骤如下:
第一步:开放式编码,对文本资料的整理得到的原始资料,经过多次、反复提炼初始概念,最终抽象出新的范畴。第二步:主轴式编码,在开放式编码的基础上挖掘不同范畴间的逻辑关联,不断分析各范畴之间显性和隐性的逻辑关系,并基于范畴间的联结关系归纳提炼主范畴。第三步:选择式编码,对相应的范畴关系进行不断分析和比较,着重探讨核心范畴与其他范畴间的联系,以“故事线”的方式来描述行为现象和脉络条件,发展新的理论框架。第四步:理论饱和度检验,本文将3 份访谈资料用于理论饱和度检验,与已得出的概念、范畴及范畴间关联进行复查,经检验未得出新范畴与关系,也未发现存在实质分歧,因此通过理论饱和度检验。
2 研究结果
2.1 人口统计学信息
本研究共纳入29 名访谈者,分析统计了他们的性别、年龄、学历、职业、工作年限及单位属性。其中,性别方面:男性占比27.59%,女性占比72.41%;年龄方面:31~35 岁占比13.79%,36~40岁占比24.14%,41~45 岁占比37.93%,≥46 岁占比24.14%;学历方面:博士占比34.48%,硕士占比55.17%,本科占比10.35%;职业方面:伦理委员占比75.86%,资深伦理秘书占比24.14%;工作年限:5~10 年占比65.52%,11~15 年占比20.69%,≥16年占比13.79%;单位属性方面:医院占比72.41%,大学占比20.69%,社区占比3.45%,第三方组织占比3.45%。具体详见表1。
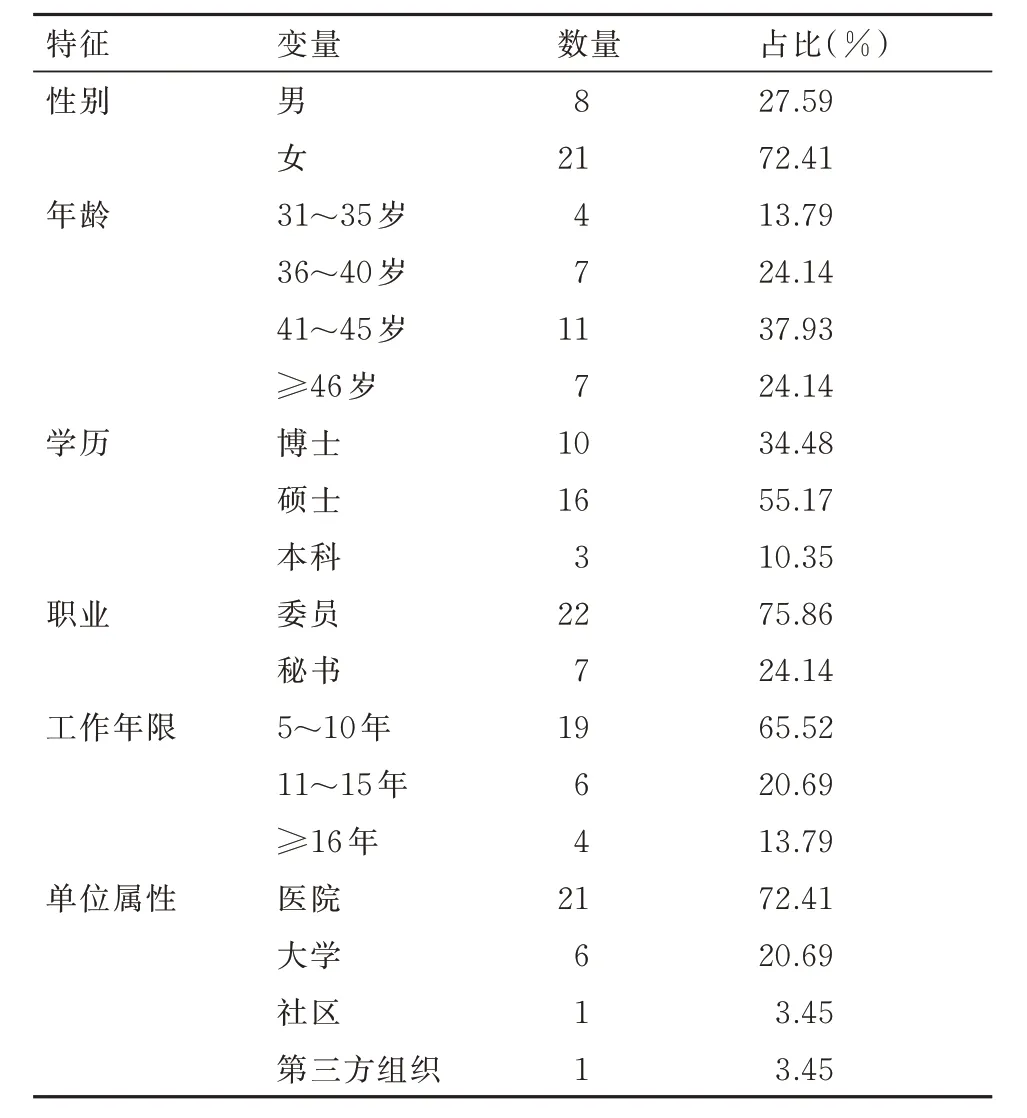
表1 访谈者个人信息
2.2 研究风险与受益
构建适合中国国情的临床研究风险与受益评估体系,需要考虑中国特有的文化环境、社会环境、经济发展水平、居民素质、疾病谱等因素,上述因素的差异性会对个人、群体、社会产生不同的影响,从而形成特殊的背景环境。因此,本文基于中国国情提出了临床研究风险与受益框架。其中,临床研究风险由生理风险、心理风险、经济风险和社会风险四个维度构成;研究受益由研究参与者受益和社会受益两个维度构成。详见表2。

表2 我国临床研究风险与受益框架
2.2.1 研究风险
第一,生理风险。研究参与者参与研究而发生身体伤害的可能性和严重程度,包括轻微或严重的伤害、暂时或永久的伤害、立即或延迟的伤害[8-9]。可分为身体不适、人体损伤两个方面。
①身体不适:研究干预措施(药物、器械、新疗法、新技术等)或研究设计(随机双盲、对照、安慰剂等)导致研究参与者身体损害,绝大多数是暂时性、可逆的、一过性。如轻度的药物不良反应;常见的静脉抽血造成短暂的头晕或是静脉穿刺、侵入性检查有关的疼痛等轻微不适。
②人体损伤:干预措施(药物、器械、新疗法、新技术等)或是研究设计(随机双盲、对照、安慰剂等)引起的研究参与者身体损伤,有可逆的、隐性的损伤,亦有严重的、不可逆、永久性的损伤,甚至灾难性的伤害(致残致畸或死亡)。如肉眼观察不到的隐性伤害风险(X 射线、DNA 断裂等);试验药物的副作用和不良事件对人体系统(肝脏、肾脏、心血管、神经系统等)造成伤害[10]。
第二,心理风险。研究参与者参与研究可能会影响其自我感知,导致其情绪、情感痛苦(如紧张、内疚、尴尬、焦虑或羞耻),或可能引起其思想或行为上的偏差(缺乏自信、自责、易怒等),甚至引发相关并发症[8-9]。从风险类别看,可分为心理不适和心理创伤两个方面。
①心理不适:其严重程度稍轻,一般是短暂的、一次性的。有以下几方面的可能:因研究周期长,过多的关注、随访和信息采集,使得研究参与者产生心理压力和不适;研究不确定性导致研究参与者心理不安,如对药物副作用或不良反应担忧、失去常规治疗机会的担忧;问及研究参与者隐私或是触碰既往不好回忆引起的心理不适;潜意识中感觉被胁迫参加研究引起的心理不适,如来自治疗医生、家人等;研究封闭环境引起的研究参与者心理焦虑,如I 期临床试验、重大传染病研究等;研究者不恰当的言语引起研究参与者的心理不适;阴性结果对高预期研究参与者产生心理不适;信息泄露引起的心理不适等。
②心理创伤:其严重级别高于心理不适,对研究参与者身心影响广泛,症状更为复杂多样。可能是由于研究导致的长期心理不适,最后演变成了心理创伤,如研究参与者对疾病的焦虑、不安得不到有效缓解,从而慢慢演变成心理创伤;或是研究过程中产生的应急伤害、严重伤害事件所引起的心理创伤,如研究参与者术后产生的创伤后应激障碍(创伤性再体验症状、噩梦、失眠等),甚至产生抑郁、焦虑和行为障碍等并发症[15]。
第三,经济风险。因研究方案或程序设计不合理,导致研究参与者产生额外的经济损失和负担[8-9],或是造成研究参与者时间成本的浪费。
①经济损失:研究参与者直接或间接地支出额外费用或是增加个人经济负担,甚至失业。例如:因研究设计的缺陷导致研究参与者承担额外的花费,如来往交通费、额外的医疗康复费用等;因参与研究导致工作单位误工造成的个人经济损失;因参与某疾病研究被医保信息记录,导致无法购买相关商业保险[8];因参与研究导致人体伤残而造成个人失业等经济损失。
②时间成本:因研究程序设计的缺陷,要求研究参与者参加不必要的研究访视,会浪费研究参与者个人时间;或是无效的研究设计可能会浪费研究参与者投入时间。如一项没有科学意义的研究,其研究结果无太多科学价值,IRB 在批准此项研究中应当考虑研究参与者参加研究的时间成本。
第四,社会风险。指个体与群体可能发生的损失[9]。从个体层面讲,研究参与者因参与研究可能面临一些污名化或社会歧视,影响其个人生活和工作,甚至影响其家庭和社会关系[8,10];从群体层面讲,比如基因编辑、器官移植、人工智能等新技术在造福人类的同时,也会给社会群体带来诸多伦理风险。
①社会歧视。个人隐私与信息泄露(如传染性疾病、同性恋、敏感基因、特殊疾病、生理缺陷等)可造成研究参与者被“贴上标签”,导致个人名誉受损或污名化,受亲友、同事、工作单位等群体和组织的歧视与偏见,影响个人就业、教育、婚姻及家庭等社会活动。
②法律纠纷:研究存在侵犯研究参与者权益或是有潜在赔偿纠纷等情形。
③群体风险:研究所涉及的种族/人群遗传资源和信息泄露,会使国家/人群面临生物安全风险;研究采集的大数据(隐私)泄露会影响社会公共和信息安全;基因编辑或新发突发传染病研究可能会引起潜在的社会风险。
2.2.2 研究受益
第一,研究参与者受益。研究参与者通过参加研究疾病的预防、诊断、治疗、康复、预后及健康维护等活动,可能在改善其生理健康、获得心理安慰或是增加对疾病的认识等有潜在的获益[10,16-17]。
①生理受益:主要体现在研究参与者疾病预防、诊断、治疗与康复等方面的潜在受益。比如,研究参与者参加研究可能治愈疾病,缓解疾病症状;或是在医疗团队的指导下,研究参与者能够改进个人生活质量,预防疾病的发生,延长生存周期。
②心理受益:研究参与者参加研究获得的潜在心理受益。例如,可能会获得来自医护人员或病友的心理安慰和支持;或是参加研究对所患病症获得更深刻的认识,心理更加成熟,这对疾病治疗有潜在获益。
第二,社会受益。主要体现在科学价值、社会价值及利益相关者受益[10,16-17]。
①科学价值:医学研究的科学价值在于发现疾病的发生、发展和防治规律,从研究中我们能够获取医学新知识,开发临床治疗新手段和新方法,推动医学科技进步发展。
②社会价值:研究所获取的信息可能有助于解决医学难题,这对改善同类患病人群和社会公众健康有重要作用。比如:研究参与者参与研究对其个人可能没有直接受益前景,但增加了对同类患病人群或是对疾病的认识而使整个社会受益,有助于促进人类健康,延长人类寿命。
③利益相关者受益:利益相关者包括研究者、研究机构和研究资助方,他们在临床研究中扮演着重要角色[18]。例如,利益相关方为临床研究开展投入诸多经费、场地和管理等,理应获得相应的受益。但与上述科学价值和社会价值相比,利益相关者受益在伦理决策过程中并非最重要的。
首先,研究者受益是指研究者对临床研究的科学性、伦理合规性负责。研究者通过开展临床研究可获得新知识、新技术,促使研究成果改善临床实践;亦可通过研究实施锻炼个人和团队的研究能力。其次,研究机构受益是指研究机构主要负责项目的立项、过程和质量管理,通过批准临床研究在本单位的实施,可从研究项目中获得相应的经济利益(如科研经费),亦可通过研究获得新知识产权等成果。最后,研究资助方受益是指研究资助方是临床研究的发起者、组织者或是申办者,在临床研究过程中,研究资助方可获得更多的直接或者潜在的经济利益;亦可通过研究获得新的知识产权等成果。
3 讨论
3.1 系统阐述临床研究风险维度及其内涵
在国际同行研究基础上,本文将临床研究风险维度划分为生理、心理、经济、社会四个层面,并基于中国国情系统阐明和解释每条风险维度的内涵,在理论研究方面具有一定创新性。①在生理风险方面:从研究干预措施、研究程序对研究参与者可能造成的生理伤害进行归类,并将其划分为身体不适、人体损伤两个方面,其归类原则按照伤害的严重程度、发生概率、时效性等方面予以划分。②在心理风险方面:按照风险严重程度划分为心理不适与心理创伤,在专家访谈过程中考虑了研究实施过程中各种可能引起研究参与者心理不适或伤害的因素,提出要重视研究实施对研究参与者的心理影响。③在经济风险方面:当前伦理审查实践过程中更多关注的是经济赔偿问题,关于研究参与者额外的经济损失和时间成本浪费关注较少,为此本文将经济负担与风险单独列为一项重要内容予以考虑。④在社会风险方面:主要表现为个体与群体可能发生的损失,探讨了个人参与研究可能对其社会活动的影响,以及新技术、新方法、人工智能临床研究也会给社会群体带来诸多伦理风险;在今后的伦理审查过程中,IRB 应当给予更多的社会风险关注,尤其是将研究造成群体性风险列入重要的评估范畴。
3.2 率先阐明临床研究受益维度及其内涵
当前学术界的研究重点聚焦在研究风险,对研究受益缺乏内涵阐释。本文深入探讨临床研究受益维度及内涵,将受益分为两大类:研究参与者受益和社会受益。①在研究参与者受益方面:主要强调研究参与者生理与心理的受益,生理受益强调研究参与者参加研究从而可能治愈疾病或缓解症状;心理受益强调研究参与者参加研究可能会获得来自医护人员和病友的安慰和支持,或是对疾病认识加深而缓解心理压力。本研究在访谈过程中发现一个有趣的问题,“研究参与者因参与研究而享受到更便捷的医疗照护”,这是不是受益?很多人会质疑,认为这对普通患者不公平,不符合伦理原则。例如,有的研究机构为尽快招募到研究参与者,会给患者就诊提供便利;美国国立卫生研究院下属国家心脏、肺和血液研究所在其官网阐述临床试验的“可能受益”时也提到:“您将从医生和其他医疗保健人员那获得定期和仔细的医疗照护”[19]。上述便捷性行为虽与伦理原则初衷不符,但属不属于研究受益值得学术界深入思考与研究。②在社会受益方面:主要体现在科学价值、社会价值、利益相关者受益等方面。首先,临床研究必须具有科学价值,它的价值在于解决重要的科学或临床问题,推动医学科技进步,没有科学价值的研究是没意义的;社会价值是为了使患病人群和社会公众获益,我们在伦理审查过程中要综合考虑科学价值和社会价值;然而,对人类研究参与者健康的考虑应优先于科学和社会的受益[17]。其次,突破传统的社会受益认知,本文将机构、研究者和申办方等利益相关者受益纳入社会受益范畴,展现出了一个“大受益”的概念,这是一项重要的创新。IRB 委员在审查临床研究项目时,不能忽略机构、研究者和申办方的受益因素,这些最直接的受益往往是影响研究风险的重要因素。
3.3 为构建适用于中国国情的临床研究风险-受益评估表提供思路
当前医疗机构伦理委员会成员往往依靠经验来判断临床研究项目的风险与受益,伦理决策过程与结果往往存在一定的偏倚性,而开展风险与受益评估是解决伦理决策中直觉判断与认知偏倚的关键手段。但是,国内外关于临床研究风险与受益评估框架的研究仍然缺乏,Rid[1]提出了一个“风险获益评估的七步框架”,但并未涉及具体、细化的评估指标。为了解决上述问题,本研究从伦理审查工作者视角深度阐述了风险与受益维度与内涵,并基于中国国情提出了临床研究风险与受益评估框架,为风险与受益评估提供新的思考范式。后续研究可在已开发的风险与受益评估框架基础上,细化研究风险与受益评估指标,建立基于主观评价与客观资料、数据相结合的一种新的风险与受益评估方法,即探索构建相对客观且量化的风险与受益评估表[20],为伦理决策者确定合理的风险受益比提供证据支持,可以最大限度地减少伦理审查评估中的人为主观因素,使伦理审查更加客观、标准、公正。此外,围绕临床研究风险与受益评估表,可建立新型的伦理审查路径和标准,指导伦理委员会规范化建设,同质化提升不同医疗机构伦理审查质量与水平,助推全国多中心伦理审查政策落地。
4 小结
本研究为质性研究,本文提出的临床研究风险与受益框架是基于探索性研究得出的,其信度、推广度还未经过大样本统计检验。今后尚需对框架中涉及的变量范畴进行概念化并开发出测量量表,采用大规模问卷调查以检验框架中变量之间的关系。
