微生态制剂联合肠内营养治疗2型糖尿病并发肺结核的效果分析
2024-03-14张继萍申晓晓李霞黄秀香叶迎宾郑艳丽李燕
张继萍 申晓晓 李霞 黄秀香 叶迎宾 郑艳丽 李燕
糖尿病(diabetes mellitus,DM)患者感染结核病(tuberculosis,TB)的风险是非糖尿病患者的3倍[1]。全球糖尿病患者感染结核病发病率为13.73%[2]。糖尿病合并结核病(T2DMTB)患者的治疗效果较差,治疗不理想或复发风险极高[3],因此引入有效的预防和治疗方法迫在眉睫。T2DMTB患者往往表现出营养不良,在抗结核治疗过程中可通过肠内营养剂增加营养物质的摄入。同时需要增加营养物质的吸收,这就依赖于微生态制剂,调节肠道菌群,更好地利用营养物质[4]。本研究通过分析T2DMTB患者治疗后的痰涂片转阴情况、免疫指标及离子指标变化情况等,旨在探讨微生态制剂联合肠内营养辅助治疗T2DMTB患者的临床疗效。
1 资料与方法
1.1 一般资料 按随机数字表法将2019年1月1日至2020年12月31日在邯郸市传染病医院收治的T2DMT13患者纳入正常饮食组(A组)、微生态制剂组(B组)、肠内营养组(C组)和微生态制剂+肠内营养组(D组),共纳入77例患者,其中A组19例,B组19例,C组19例,D组20例患者。
1.2 纳入与排除标准
1.2.1 纳入标准:邯郸市汉族人群;T2DMTB组符合2型糖尿病的诊断同时符合肺结核的诊断,初治继发性;患者痰结核分枝杆菌检查阳性,即痰涂片抗酸杆菌萋-尼染色镜检(简称“痰涂片”)阳性。诊断标准见文献[5]。
1.2.2 排除标准:非邯郸市人群,非汉族人群,艾滋病、病毒性肝炎(乙、丙型)、梅毒患者,并发各种肿瘤、结缔组织疾病、其他内分泌疾病患者,围手术期患者,肾功能不全患者及肠结核患者。
1.3 方法 4组纳入患者给予抗结核药品治疗及降糖药品等常规治疗并进行糖尿病饮食宣教。A组在常规治疗基础上,给予常规饮食;B组患者在常规治疗和常规饮食基础上,加用六联益生菌粉(浙江禾健生营养科技有限公司生产,2 g/包),主要包括双歧杆菌、干酪乳杆菌、植物乳杆菌、嗜酸乳杆菌、嗜热链球菌、鼠李糖乳杆菌等,用温水冲服,4 g/d;C组患者在常规治疗和常规饮食基础上,加用复合营养粉(杭州贝聪美健康科技有限公司,25 g/包),150 mL温水搅拌均匀后服用,50 g/d;D组患者在常规治疗和常规饮食基础上,给予六联益生菌粉(方法同B组)及肠内营养(方法同C组)。

2 结果
2.1 4组患者治疗效果比较 4组患者痰涂片转阴率差异有统计学意义(χ2=19.204,P=0.0038),其中A组转阴率52.63%(10/19),B组转阴率36.84%(7/19),C组转阴率57.89%(11/19),D组治疗效果最好,转阴率95.00%(19/20)。见表1。

表1 4组患者治疗效果比较 例(%)

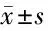
表2 4组治疗前后免疫细胞水平比较
2.3 4组患者治疗前后离子水平比较 与治疗前比较,治疗后A组、B组和C组Na+水平升高,差异有统计学意义(t=-2.373087,P=0.0290;t=-2.2978,P=0.0345;t=-3.16969,P=0.0068),治疗后D组Na+水平有升高趋势,但差异无统计学意义(t=-0.60403,P=0.5534)。与治疗前比较,治疗后A组、B组、C组和D组Pi水平升高,差异有统计学意义(t=-3.638877,P=0.001;t=-4.02907,P=0.0009;t=-3.74725,P=0.0022;t=-4.70007,P=0.0002)。与治疗前比较,C组和D组Fe2+水平升高,差异有统计学意义(t=-2.5827,P=0.0217;t=-2.15895,P=0.0446)。与治疗前比较,B组和C组Mg2+水平升高,差异有统计学意义(t=-3.11784,P=0.0063;t=-2.78951,P=0.0164)。见表3。
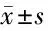
表3 4组治疗前后离子水平比较 mmol/L,
3 讨论
糖尿病是一种慢性代谢性疾病,越来越多的证据表明其与肠道微生物群组成的改变有关。肠道微生物是栖息在胃肠道中的各种微生物群,与身体存在共生关系,具有显著的代谢和调节功能。微生物群被认为是一种特殊的“器官”[6],对代谢紊乱的发展有显著影响[7]。肠道微生物群通常是稳定的[8],但随着年龄的增长,由于免疫系统减弱,消化道功能障碍或营养不良导致肠道微生物稳态发生变化[9]。研究发现,微生态制剂可以通过调节肠道菌群改变糖脂代谢,改善轻度炎症,增强免疫反应[10]。本研究结果显示,单独使用微生态制剂对于T2DMTB患者症状并没有明显的改善。可能是由于微生态制剂调整肠道菌群稳定需要长时间的摄取,短时间内效果并不明显。微生态制剂可改善患者血糖控制水平,为抗结核治疗打下基础。
结核病是一种消耗性疾病,营养不良和结核病往往相互作用。一方面,结核病导致营养不良恶化,蛋白质-能量供应不足,微量营养素缺乏,机体处于分解代谢状态,体重或体质指数(BMI)降低[11]。另一方面,营养不良被认为会使糖尿病患者更容易感染结核病,并通过损害细胞介导的对结核分枝杆菌的免疫力延迟转归。同时,之前研究指出,营养支持与改善血糖控制有关,可减少血糖控制不佳对结核病的影响[12]。因此,可通过应用肠内营养剂改善患者的营养状况,从而提高免疫力。本研究结果显示,单独应用肠内营养剂可促进痰涂片转阴,有效的改善结核病患者的感染状况。
在抗结核治疗过程中注意营养物质的摄入,同时也需要增加营养物质的吸收。这就依赖于微生态制剂,调节肠道菌群,更好地利用营养物质。研究结果表明,T2DMTB患者应用微生态制剂与肠内营养剂联合治疗1个月后效果显著。微生态制剂与肠内营养可改善电解质平衡,纠正电解质紊乱。铁参与维持人体正常的免疫功能,同时参与抗体的产生以及药物在肝脏中的代谢。研究表明,应用肠内营养剂后,患者血清铁升高,可促进T2DMTB患者提高免疫力。另外,应用微生态制剂与肠内营养剂可使得Mg2+含量升高。镁参与体内代谢,包括葡萄糖的应用、脂肪/蛋白质和核酸的合成等。感染和疾病会增加体内镁的消耗,导致代谢异常。因此,应用微生态制剂与肠内营养剂有助于T2DMTB患者恢复代谢水平,促进疾病转归。但本研究结果并未发现患者血清中各离子水平的明显差异。
众所周知,结核病感染源主要是痰涂片或细菌培养阳性率,尤其是涂片阳性患者具有较强的传染性。痰涂片转阴是抗结核治疗的主要结果。本研究表明,营养支持(肠内营养剂)会加速这一过程。这可能是由于结核分枝杆菌感染时,身体免疫功能降低,并在抗结核治疗过程中食欲不振,蛋白或微量营养素摄入不足导致营养不良。因此,持续提供营养支持(蛋白质、微量营养素的摄入)可增强免疫应答功能[13]。
结核病可能导致营养缺乏,从而抑制免疫功能延迟恢复,营养支持可以促进结核病患者康复。同时,这些营养成分被肠道菌群代谢,产生有效的代谢、免疫调节剂等。肠道菌群的免疫、代谢、调节潜力解释了在健康和疾病中的重要性[14]。值得注意的是,营养支持是安全的,耐受性好,本研究中并未出现任何全身不良事件。因此,微生态制剂与肠内营养联合对于T2DMTB患者治疗是比较理想的,能够增强患者的免疫力,能够使抗结核药物发挥最大的疗效,更快消除结核。
本研究不足之处是对于抗结核治疗方案的不同是否会对营养支持治疗效果有所影响,今后需进一步研究分析。
